名校
1 . 元素周期表是化学史上重要的里程碑之一,下表是现行长式周期表的一部分。结合下表用化学用语回答问题:
(1)上表元素①~⑦中,非金属性最强的是___________ 。
(2)元素⑦为铁元素,其在周期表中的位置为___________ ,写出其单质与⑤的单质反应的化学方程式___________ 。
(3)可以用元素③的氢化物的水溶液溶蚀玻璃生产磨砂玻璃,写出反应的化学方程式___________ 。
(4)元素②④⑥简单离子半径由大到小为___________ 。
(5)元素④与元素①形成化合物X,写出X的电子式___________ ,其化学键类型为___________ ,X在野外能做生氢剂,其与水反应生氢的反应中,氧化剂为___________ 。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ||||||||||||||||
| ⑥ | ⑦ | ||||||||||||||||
(2)元素⑦为铁元素,其在周期表中的位置为
(3)可以用元素③的氢化物的水溶液溶蚀玻璃生产磨砂玻璃,写出反应的化学方程式
(4)元素②④⑥简单离子半径由大到小为
(5)元素④与元素①形成化合物X,写出X的电子式
您最近一年使用:0次
名校
2 . 如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题。
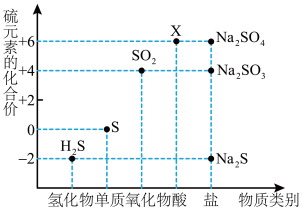
(1)X 的浓溶液与碳在一定条件下可以发生反应,体现了 X 的_______ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有_______ (填化学式)。
(3)将 H2S 与 SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为_______ 。
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目______ 。
Na2S+_______Na2SO3+_______H2SO4=_______Na2SO4+_______S↓+_______H2O
(5)下列关于硫及其化合物的叙述正确的是
(6)设 NA为阿伏加德罗常数的值。下列说法正确的是
为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:
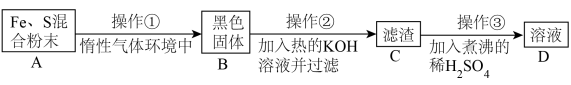
请回答以下问题:
(7)操作②的作用是_______ ,也可改用_______ 。
(8)混合粉末 A 中硫粉过量的原因是_______ 。
(9)下列溶液中通入SO2一定不会产生沉淀的是
(10)区别浓H2SO4和稀H2SO4,既简单又可靠的方法是

(1)X 的浓溶液与碳在一定条件下可以发生反应,体现了 X 的
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有
(3)将 H2S 与 SO2混合可生成淡黄色沉淀。该反应中氧化产物与还原产物的物质的量之比为
(4)配平下列反应,并用单线桥法标出电子转移的方向和数目
Na2S+_______Na2SO3+_______H2SO4=_______Na2SO4+_______S↓+_______H2O
(5)下列关于硫及其化合物的叙述正确的是
| A.试管内壁残留的硫可用酒精洗涤 | B.SO2的水溶液长期放置,酸性会增强 |
| C.SO2有毒,不可以做食品添加剂 | D.浓硫酸在空气中敞口放置,质量会减小 |
| A.1mol 铁单质与足量的硫单质充分反应,转移电子的数目为3NA |
| B.常温下,22.4LSO2与足量的O2反应,生成的SO3分子数为NA |
| C.常温下,将5.6g铁片投入足量的浓硫酸中,铁失去的电子数为0.3NA |
| D.1 molNa2O2与足量H2O反应,转移的电子数为NA |
为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:

请回答以下问题:
(7)操作②的作用是
(8)混合粉末 A 中硫粉过量的原因是
(9)下列溶液中通入SO2一定不会产生沉淀的是
| A.Ba(OH)2 | B.澄清石灰水 | C.Na2S | D.BaCl2 |
| A.各取少许溶液分别放入铜片 | B.分别与石蕊试液作用 |
| C.用玻璃棒各蘸少许液涂在纸上 | D.观察溶液的颜色 |
您最近一年使用:0次
名校
3 . 生活中我们都会发现,煮鸡蛋时间太久或放置时间过长,蛋黄上会产生一层“黑膜”,该黑膜的成分是硫化亚铁。这是由于鸡蛋里的蛋白质受热分解成小分子的氨基酸,有的氨基酸含硫元素,会形成硫化氢,而蛋黄中富含铁元素,当硫化氢遇到铁元素就形成了硫化亚铁,也就是蛋黄上覆盖的那层“黑膜”。

某同学由此联想到铁与硫单质的反应,为了验证铁与硫单质反应产物中铁元素的化合价,该同学设计了以下实验:

已知:①FeS固体难溶于水,可与稀盐酸、稀硫酸发生反应:FeS+2H+=Fe2++H2S↑。
②3S+6NaOH 2Na2S+Na2SO3+3H2O。
2Na2S+Na2SO3+3H2O。
请回答以下问题:
(1)混合粉末A中硫粉必须过量的原因是_______ 。
(2)反应在“惰性环境”中进行的原因是_______ 。
(3)操作②的作用是_______ ,也可改用_______ 。
(4)操作③稀硫酸煮沸的目的是_______ 。
(5)为检验产物中铁元素的价态,对D溶液的实验操作最好是_______ 。

某同学由此联想到铁与硫单质的反应,为了验证铁与硫单质反应产物中铁元素的化合价,该同学设计了以下实验:

已知:①FeS固体难溶于水,可与稀盐酸、稀硫酸发生反应:FeS+2H+=Fe2++H2S↑。
②3S+6NaOH
 2Na2S+Na2SO3+3H2O。
2Na2S+Na2SO3+3H2O。请回答以下问题:
(1)混合粉末A中硫粉必须过量的原因是
(2)反应在“惰性环境”中进行的原因是
(3)操作②的作用是
(4)操作③稀硫酸煮沸的目的是
(5)为检验产物中铁元素的价态,对D溶液的实验操作最好是
您最近一年使用:0次
2023-03-06更新
|
371次组卷
|
2卷引用:河南省郑州外国语学校2022-2023学年高一下学期第一次月考化学试题



