解题方法
1 . 硫酸是重要的化工原料,可用于生产化肥、农药、炸药、染料和盐类。我国工业上一般以黄铁矿为原料来制备硫酸。工业制硫酸涉及到下列反应:
① ;②
;②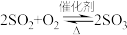 ;③
;③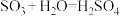 。
。
生产中用浓硫酸代替水吸收 ,制得发烟硫酸(
,制得发烟硫酸(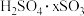 ),将发烟硫酸稀释后可制得密度为
),将发烟硫酸稀释后可制得密度为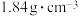 、质量分数为
、质量分数为 的浓硫酸。下列有关硫及其化合物的性质与用途具有对应关系的是
的浓硫酸。下列有关硫及其化合物的性质与用途具有对应关系的是
①
 ;②
;②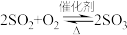 ;③
;③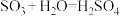 。
。生产中用浓硫酸代替水吸收
 ,制得发烟硫酸(
,制得发烟硫酸(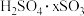 ),将发烟硫酸稀释后可制得密度为
),将发烟硫酸稀释后可制得密度为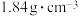 、质量分数为
、质量分数为 的浓硫酸。下列有关硫及其化合物的性质与用途具有对应关系的是
的浓硫酸。下列有关硫及其化合物的性质与用途具有对应关系的是| A.硫具有还原性,可用硫黄处理洒落的汞单质 |
| B.二氧化硫具有氧化性,可用作葡萄酒的抗氧化剂 |
| C.稀硫酸具有酸性,可用于去除铁锈 |
| D.浓硫酸具有脱水性,可用于干燥二氧化硫 |
您最近一年使用:0次
2021-06-30更新
|
391次组卷
|
2卷引用:江苏省南通市2020-2021学年高一下学期期末考试化学试题
名校
解题方法
2 . 下列说法中不正确的是( )
| A.硫单质与金属铁反应生成FeS,体现了硫单质的氧化性 |
| B.SO2能使酸性KMnO4、氯水褪色,说明SO2具有漂白作用 |
| C.SO2既有还原性,又有氧化性 |
| D.医疗上常用BaSO4作X射线透视的“钡餐” |
您最近一年使用:0次
2020-06-06更新
|
1565次组卷
|
4卷引用:宁夏大学附属中学2020-2021学年高一上学期期末考试化学试题
名校
3 . 含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-2价、0价、+4价、+6价四种,其不同价态的物质间可相互转化,完成下列填空:
(1)写出硫与铁反应的化学方程式___ 。
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,其中硫化氢呈现___ (选填“氧化性”、“还原性”)
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是___ 。
(4)将二氧化硫通入含酚酞的NaOH溶液,红色褪去,体现二氧化硫___ (性质)。
(5)硫酸盐的种类很多且应用广泛,医疗上采用___ 作X射线透视肠胃的内服药剂。
(1)写出硫与铁反应的化学方程式
(2)将硫化氢气体与二氧化硫气体在集气瓶中混合发生反应,其中硫化氢呈现
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是
(4)将二氧化硫通入含酚酞的NaOH溶液,红色褪去,体现二氧化硫
(5)硫酸盐的种类很多且应用广泛,医疗上采用
您最近一年使用:0次
4 . 下列关于S及硫的化合物的叙述正确的是
| A.SO2可用于漂白纸浆 |
| B.附着有硫的试管可以用水进行洗涤 |
| C.浓H2SO4滴在湿润的蓝色石蕊试纸,试纸先变红,然后褪色,最后变黑,说明浓硫酸具有酸性、氧化性和脱水性 |
| D.硫与铜在加热条件下反应生成CuS |
您最近一年使用:0次
名校
解题方法
5 . 物质的类别和核心元素的化合价是研究物质性质的两个基本视角。请根据如图所示,回答下列问题:

(1)Y是形成酸雨的主要物质之一,它溶于水反应的化学方程式为_____ ;另一类硝酸型酸雨主要由人类活动产生的NOx造成的,写出NO2与水反应的化学方程式为______ ;酸雨的pH______ (填范围)。
(2)Y能使品红溶液褪色,它与一种黄绿色气体等体积通入水中得到的溶液却几乎没有漂白性,反应的离子方程式为_______ ;Y也能使酸性高锰酸钾溶液褪色,写出该反应的离子方程式,并用单线桥法标明电子转移的方向和数目_____ ,体现了Y的_____ 性。
(3)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为_____ 。
(4)现用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸500mL,回答下列问题:
①所需浓硫酸的体积为______ mL。
②将浓硫酸沿烧杯内壁缓缓注入盛水的烧杯中,不断搅拌的目的是_____ ,若搅拌过程中有液体溅出,会导致最终所配溶液浓度_____ (填“偏大”、“偏小”或“无影响”,下同)。
③在转入容量瓶前,烧杯中的液体应先_____ ,否则会使浓度_____ 。
(5)已知S的氧化性较弱,则硫粉与铜加热反应的化学方程式为_____ 。
(6)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析,合理的是_____ (填序号)。
A.Na2S+S B.Na2SO3+S C.Na2SO3+Na2SO4 D.SO2+Na2SO4

(1)Y是形成酸雨的主要物质之一,它溶于水反应的化学方程式为
(2)Y能使品红溶液褪色,它与一种黄绿色气体等体积通入水中得到的溶液却几乎没有漂白性,反应的离子方程式为
(3)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
(4)现用98%的浓硫酸(ρ=1.84g/cm3)配制成浓度为0.5mol/L的稀硫酸500mL,回答下列问题:
①所需浓硫酸的体积为
②将浓硫酸沿烧杯内壁缓缓注入盛水的烧杯中,不断搅拌的目的是
③在转入容量瓶前,烧杯中的液体应先
(5)已知S的氧化性较弱,则硫粉与铜加热反应的化学方程式为
(6)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析,合理的是
A.Na2S+S B.Na2SO3+S C.Na2SO3+Na2SO4 D.SO2+Na2SO4
您最近一年使用:0次
2020-03-23更新
|
277次组卷
|
2卷引用:北京市海淀区中关村中学2021-2022学年高三上学期10月月考化学试题
名校
解题方法
6 . 中国的中医中药博大精深。中医用药讲究十八反和十八畏,其中有“硫黄原是火中精硝一见便相争”,硫黄即硫单质。下列说法中正确的是
| A.硫是一种淡黄色的能溶于水的固体 |
| B.试管内壁上的硫黄可用二硫化碳清洗 |
| C.过量的硫与铁反应生成Fe2S3,表现了硫单质的氧化性 |
| D.硫在空气中燃烧生成二氧化硫,硫在过量氧气中燃烧生成三氧化硫 |
您最近一年使用:0次
2022-12-21更新
|
300次组卷
|
2卷引用:湖北省武汉大学附属中学2021-2022学年高二上学期开学考试化学试题
7 . 根据实验操作或现象得出的结论不正确 的是
| 选项 | 实验操作和现象 | 结论 |
| A | 饱和NaHCO3溶液中滴入1mol/LCaCl2溶液,出现白色沉淀 | 饱和NaHCO3溶液中含有CO |
| B | 用铂丝蘸取X溶液进行焰色试验,透过蓝色钴玻璃观察,火焰显紫色 | X溶液为钾盐 |
| C | 铁分别与氯气和硫反应生成FeCl3和FeS | Cl2的氧化性强于S |
| D | 为探究Cl2中是否含有HCl,将气体通入AgNO3溶液中,产生白色沉淀 | 不能说明含有HCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
20-21高一下·浙江·阶段练习
名校
解题方法
8 . 硫的氧化性不如氧气强,在下列叙述中不能说明这一事实的是
A.S+O2 SO2,O2是氧化剂、S是还原剂 SO2,O2是氧化剂、S是还原剂 |
| B.S是淡黄色固体,O2是无色气体 |
| C.氢硫酸放置在空气中易变浑浊(2H2S+O2=2S↓+2H2O) |
| D.S和Cu反应只能生成Cu2S(硫化亚铜),而O2与Cu反应生成CuO |
您最近一年使用:0次
2021-04-12更新
|
493次组卷
|
5卷引用:【浙江新东方】高中化学20210429—009【2021】【高一下】
(已下线)【浙江新东方】高中化学20210429—009【2021】【高一下】黑龙江省双鸭山市第一中学2020-2021学年高一下学期第一次月考化学试题(已下线)课后-5.1.1 硫和二氧化硫-人教2019必修第二册黑龙江省牡丹江市第三高级中学2021-2022学年高一下学期开学考试化学试题浙江省杭州师范大学附属中学2022-2023学年高一下学期4月期中考试化学试题
名校
解题方法
9 . 下列说法中正确的是( )
| A.硫是一种淡黄色的能溶于水的固体 | B.试管内壁上的硫黄可用二硫化碳清洗 |
| C.过量的硫跟铁反应生成Fe2S3,表现了硫单质的氧化性 | D.硫在空气中燃烧生成二氧化硫,硫在过量氧气中燃烧生成三氧化硫 |
您最近一年使用:0次
2018-12-29更新
|
1020次组卷
|
9卷引用:(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第一节 硫及其化合物
(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第一节 硫及其化合物黑龙江省哈尔滨师范大学附属中学2020-2021学年高一下学期4月月考化学试题黑龙江省哈尔滨师范大学附属中学2020-2021学年高一下学期4月月考化学试题陕西省渭南中学2018-2019学年高一上学期第三次月考化学试题鲁科版(2019)高一必修第一册第三章第2节 硫的转化 课时1 自然界中的硫高一必修第一册(苏教2019版)专题4 第二单元 硫及其化合物的相互转化 课时1 硫单质的性质与用途高一必修第一册(苏教2019)专题4 第一单元 含硫化合物的性质1云南省梁河县第一中学2021-2022学年高一下学期开学考试化学试题5.1.1硫和二氧化硫 随堂练习
名校
解题方法
10 . 下列有关硫及其化合物性质的说法中,正确的是
| A.铜粉和硫粉混合加热可制得CuS |
| B.久置酸雨酸性增强,原因是水的挥发 |
| C.SO2通入石蕊试液中,溶液颜色先变红,再褪色 |
| D.亚硫酸钠暴露在空气中容易被氧化成硫酸钠 |
您最近一年使用:0次
2019-12-31更新
|
443次组卷
|
5卷引用:专题4 本专题达标检测-高中化学苏教2019版必修第一册



