名校
解题方法
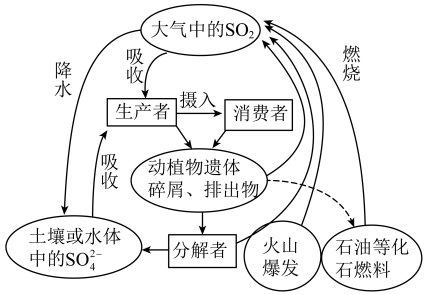
1 . 硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,在循环过程中S的价态变化在-2价至+6价之间,请分析此图并回答有关问题:______ 。
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢可在空气中燃烧生成二氧化硫
(2)大中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是___________ (用化学方程式表示)。
(3)研究发现,空气中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不符的是___________。
(4)在制葡萄酒时可以人工添加SO2,有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入SO2,请用离子方程式表示该反应原理___________ 。发酵酒卫生标准中对葡萄酒中的二氧化硫含量有要求:总SO2小于250mg/L,若在室温下。每升溶液中最多通入___________ mL SO2.(室温下Vm=24.5L/mol,结果保留3位有效数字,体积变化忽略不计)
(5)明代《徐光启手迹》记载了用硫酸盐制备硝酸的方法,其主要流程(部分产物已省略)如下:___________ 。
②关于整个制备过程,下列说法正确的是___________ 。
A.本流程涉及复分解反应
B.由H2SO4制HNO3利用了强酸制弱酸原理
C.制备使用的铁锅易损坏
(6)工业上为了防止制硫酸过程中产生污染,可以利用氧化亚铁硫杆菌(T·f)对硫铁矿进行催化脱硫,该过程如图所示:___________ 。
②脱硫过程中产生的 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式___________ 。
③从氧化还原角度分析,若要制备Na2S2O3应选择___________ (填字母)。
A.SO2+Na2SO4 B.Na2S+S C.Na2SO3+Na2SO4 D.Na2SO3+S
A.硫化氢分子很稳定,受热难分解
B.硫化氢分子中所有原子的最外层都达到8电子结构
C.将硫化氢通入硫酸亚铁溶液,产生沉淀
D.硫化氢中硫元素为-2价,因此只有还原性,没有氧化性
E.硫化氢可在空气中燃烧生成二氧化硫
(2)大中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是
(3)研究发现,空气中少量的NO2也能参与硫酸型酸雨的形成,反应过程如下:
①SO+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2
NO2在上述过程中的作用,与H2SO4在下列变化中的作用不符的是___________。
| A.潮湿的氯气通过盛有浓H2SO4的洗气瓶 |
| B.硫化氢通入浓H2SO4中 |
| C.浓H2SO4滴入萤石中,加热 |
| D.向盐酸中加入浓硫酸产生白雾 |
(4)在制葡萄酒时可以人工添加SO2,有两个目的:抗氧化和抗菌,实验室模拟二氧化硫抗氧化过程,向溴水中通入SO2,请用离子方程式表示该反应原理
(5)明代《徐光启手迹》记载了用硫酸盐制备硝酸的方法,其主要流程(部分产物已省略)如下:

②关于整个制备过程,下列说法正确的是
A.本流程涉及复分解反应
B.由H2SO4制HNO3利用了强酸制弱酸原理
C.制备使用的铁锅易损坏
(6)工业上为了防止制硫酸过程中产生污染,可以利用氧化亚铁硫杆菌(T·f)对硫铁矿进行催化脱硫,该过程如图所示:
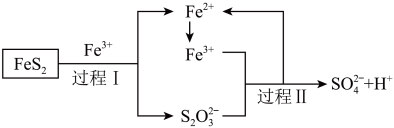
②脱硫过程中产生的
 在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式
在酸性溶液中会形成淡黄色沉淀并产生刺激性气味的气体,写出其离子方程式③从氧化还原角度分析,若要制备Na2S2O3应选择
A.SO2+Na2SO4 B.Na2S+S C.Na2SO3+Na2SO4 D.Na2SO3+S
您最近一年使用:0次



