1 .  具有氧化性、还原性和漂白性,某同学在实验室利用
具有氧化性、还原性和漂白性,某同学在实验室利用 做相关验证和探究实验。回答下列问题:
做相关验证和探究实验。回答下列问题:
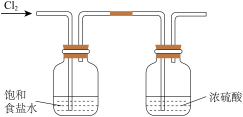
(1)用如图1装置(夹持仪器已省略)验证 具有氧化性。
具有氧化性。 的名称为
的名称为___________ 。
②装置甲试管中反应的离子方程式为___________ 。
③说明 具有氧化性的现象为
具有氧化性的现象为___________ 。
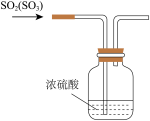
(2)该同学设计如图2所示装置(夹持仪器已省略)制备 (难溶解于水中)。
(难溶解于水中)。 的作用是
的作用是___________ 。
②三颈烧瓶中反应的化学方程式为___________ 。
(3)该实验体现了 的性质是
的性质是___________ 。
(4)实验表明,将纯净的 缓缓地通入到
缓缓地通入到 溶液中,得到
溶液中,得到 沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
假设Ⅰ:溶液中的 ;
;
假设Ⅱ:溶解在水中的氧气。
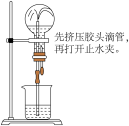
①验证假设Ⅰ(配制溶液前已将蒸馏水煮沸并密封冷却)。
实验i现象为___________ ,实验ii的现象为___________ 。
②验证假设Ⅱ。请完成下列表格:
实验iv的步骤为___________ ,实验目的是___________ 。
 具有氧化性、还原性和漂白性,某同学在实验室利用
具有氧化性、还原性和漂白性,某同学在实验室利用 做相关验证和探究实验。回答下列问题:
做相关验证和探究实验。回答下列问题:(1)用如图1装置(夹持仪器已省略)验证
 具有氧化性。
具有氧化性。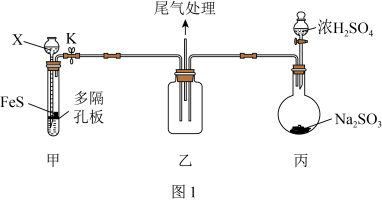
 的名称为
的名称为②装置甲试管中反应的离子方程式为
③说明
 具有氧化性的现象为
具有氧化性的现象为(2)该同学设计如图2所示装置(夹持仪器已省略)制备
 (难溶解于水中)。
(难溶解于水中)。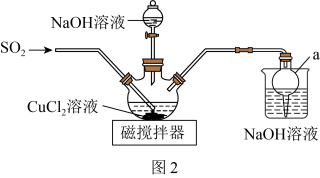
 的作用是
的作用是②三颈烧瓶中反应的化学方程式为
(3)该实验体现了
 的性质是
的性质是(4)实验表明,将纯净的
 缓缓地通入到
缓缓地通入到 溶液中,得到
溶液中,得到 沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:
沉淀。为了探究该反应中的氧化剂,该同学提出以下假设:假设Ⅰ:溶液中的
 ;
;假设Ⅱ:溶解在水中的氧气。
①验证假设Ⅰ(配制溶液前已将蒸馏水煮沸并密封冷却)。
| 实验步骤 | 实验操作 | 实验现象 | 结论 |
实验 | 向 溶液中缓慢通入纯净的 溶液中缓慢通入纯净的 气体 气体 | 假设I成立 | |
实验 | 向 溶液的烧杯中缓慢通入纯净的 溶液的烧杯中缓慢通入纯净的 气体 气体 |
②验证假设Ⅱ。请完成下列表格:
| 实验步骤 | 实验现象 | 实验目的 | |
| 实验iii | 同实验 步骤 步骤 | 同实验 的相关现象 的相关现象 | 作对照实验 |
| 实验iv | 产生白色沉淀 | ||
您最近一年使用:0次
2024-02-23更新
|
648次组卷
|
8卷引用:黑龙江省牡丹江市第一高级中学2023-2024学年高一下学期5月期中考试化学试题
黑龙江省牡丹江市第一高级中学2023-2024学年高一下学期5月期中考试化学试题江西省部分学校2023-2024学年高三上学期2月月考化学试题(已下线)专题03 常见气体的实验室制取(考题猜想)(6大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)四川省绵阳中学2023-2024学年高三下学期2月开学考理科综合-高中化学(已下线)大题02 化学实验综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)2024届内蒙古自治区乌海市第六中学高三下学期第三次模拟考试理综试题-高中化学河南省郑州市第五高级中学2023-2024学年高三2月开学考理综试题-高中化学四川省广元市川师大万达中学2023-2024学年高一下学期3月月考化学试题
2 . 实验室可用如图装置(略去部分夹持仪器)制取 并验证其性质。
并验证其性质。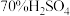 溶液的仪器名称为
溶液的仪器名称为_______ 。
(2)装置 的作用之一是通过观察产生气泡的多少判断
的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择_______(填字母)。
生成的快慢,其中的液体最好选择_______(填字母)。
(3) 试管中的试剂可以验证二氧化硫的氧化性,现象为
试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。经测定,产物中还有一种相对分子质量为104的酸式盐,则该反应的离子方程式为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管 中的溶液分成三份,分别进行如下实验:
中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管 中
中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(5)装置 的作用是
的作用是_______ 。装置 中为
中为_______ 溶液。
 并验证其性质。
并验证其性质。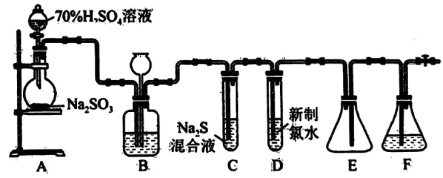
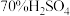 溶液的仪器名称为
溶液的仪器名称为(2)装置
 的作用之一是通过观察产生气泡的多少判断
的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择_______(填字母)。
生成的快慢,其中的液体最好选择_______(填字母)。| A.蒸馏水 | B.饱和 溶液 溶液 | C.饱和 溶液 溶液 | D.饱和 溶液 溶液 |
 试管中的试剂可以验证二氧化硫的氧化性,现象为
试管中的试剂可以验证二氧化硫的氧化性,现象为(4)为验证二氧化硫的还原性,充分反应后,取试管
 中的溶液分成三份,分别进行如下实验:
中的溶液分成三份,分别进行如下实验:方案Ⅰ:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。上述方案中能达到实验目的的是方案
 中
中 发生反应的离子方程式为
发生反应的离子方程式为(5)装置
 的作用是
的作用是 中为
中为
您最近一年使用:0次
名校
解题方法
3 . 实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。____ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择______ (填代号)。
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案____ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为_____ 。
(5)装置E的作用是______ 。装置F中为_____ 溶液。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案
(5)装置E的作用是
您最近一年使用:0次
2024-04-04更新
|
125次组卷
|
2卷引用:四川省德阳外国语学校2023-2024学年高一下学期期中考试化学试题
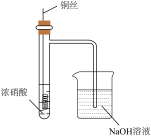
4 . 如下图所示,某同学利用Na2SO3和浓H2SO4制取SO2并探究其性质。

(1)装置A中盛浓硫酸的仪器名称是_______ ,写出装置A中发生反应的化学方程式:_______ 。
(2)装置C中的实验现象是_______ ,该实验现象说明SO2具有_______ 性。
(3)能验证SO2具有酸性氧化物的通性的实验现象是_______ 。
(4)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象_______ 。
(5)探究H2SO3的酸性强于HClO,该同学用如下图所示装置达成实验目的。
a. 小苏打溶液b.
小苏打溶液b. 品红溶液
品红溶液
c. 酸性KMnO4溶液d.
酸性KMnO4溶液d. 漂白粉溶液
漂白粉溶液
装置的连接顺序为纯净SO2→_______ (选填字母);d中反应的离子方程式为_______ 。

(1)装置A中盛浓硫酸的仪器名称是
(2)装置C中的实验现象是
(3)能验证SO2具有酸性氧化物的通性的实验现象是
(4)装置E的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象
(5)探究H2SO3的酸性强于HClO,该同学用如下图所示装置达成实验目的。
a.
 小苏打溶液b.
小苏打溶液b. 品红溶液
品红溶液c.
 酸性KMnO4溶液d.
酸性KMnO4溶液d. 漂白粉溶液
漂白粉溶液装置的连接顺序为纯净SO2→
您最近一年使用:0次
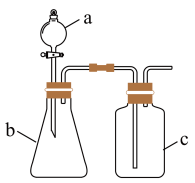
5 . Ⅰ.甲、乙、丙三位同学分别用如下实验装置及化学药品(碱石灰为氢氧化钠和生石灰的混合物)制取氨气。请你参与探究,并回答问题:
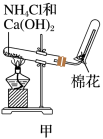
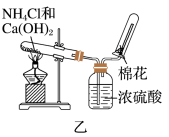
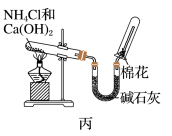
(1)他们制取氨气的化学方程式为:______ 。
(2)三位同学都用向下排空气法收集氨气,其原因是______ 。
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(实验操作都正确),你认为没有收集到氨气的同学是_____ 填(“甲”、“乙”或“丙”)。
(4)检验氨气是否收集满的方法是:(简述操作方法、现象和结论)______ 。
(5)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的的是______ (填“甲”、“乙”或“丙”),该装置中的NH4HCO3固体能否用NH4Cl固体代替?_____ (填“能”或“不能”)。
Ⅱ.已知二氧化硫可使高锰酸钾溶液褪色反应的化学方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4。如图为验证浓硫酸与木炭在加热条件下,反应产物中是否含有SO2和CO2的部分装置。
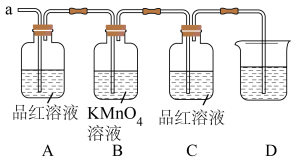
(6)B瓶中KMnO4的作用:______ 。
(7)可观察到A瓶的溶液的现象是______ 。
(8)D瓶溶液为Ca(OH)2溶液,当看到______ 说明生成物中有CO2。



(1)他们制取氨气的化学方程式为:
(2)三位同学都用向下排空气法收集氨气,其原因是
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(实验操作都正确),你认为没有收集到氨气的同学是
(4)检验氨气是否收集满的方法是:(简述操作方法、现象和结论)
(5)三位同学都认为他们的实验装置还可用于加热碳酸氢铵固体来制取纯净的氨气,你判断能够达到实验目的的是
Ⅱ.已知二氧化硫可使高锰酸钾溶液褪色反应的化学方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4。如图为验证浓硫酸与木炭在加热条件下,反应产物中是否含有SO2和CO2的部分装置。

(6)B瓶中KMnO4的作用:
(7)可观察到A瓶的溶液的现象是
(8)D瓶溶液为Ca(OH)2溶液,当看到
您最近一年使用:0次
名校
解题方法
6 . 根据要求完成下列各小题实验目的。a、b为弹簧夹,(加热及固定装置已略去)。

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是______ 。装置A中试剂可以是_____ 。(用a,b,c填空)
a.品红溶液 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
②能说明碳的非金属性比硅强的实验现象是_____ 。
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
①在(1)操作后打开b,关闭a。
②一段时间后,H2S溶液中的现象是_____ ,化学方程式是_____ 。
(3)BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入表中相应位置。

(1)验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是
a.品红溶液 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
②能说明碳的非金属性比硅强的实验现象是
(2)验证SO2的氧化性、还原性和酸性氧化物的通性。
①在(1)操作后打开b,关闭a。
②一段时间后,H2S溶液中的现象是
(3)BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入表中相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
您最近一年使用:0次
解题方法
7 . 如图所示,某同学利用Na2SO3和浓H2SO4制取SO2并探究其性质。
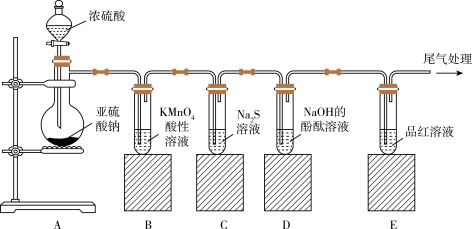
(1)装置A中装浓硫酸的仪器名称:______ 。
(2)装置B中的离子方程式是_____ ,该反应说明SO2具有_____ 性。
(3)装置C中的实验现象是_____ ,该实验现象说明SO2具有_____ 性。
(4)装置E中的现象是_____ ,尾气处理所用的试剂是____ 。
(5)某同学制取的SO2气体中混有CO2气体,请你设计实验证明混合气体中既有SO2气体,又有CO2气体。可以选择如图洗气装置设计实验:
洗气装置中的溶液是。
A.浓硫酸 B.氢氧化钠溶液 C.硫酸铜溶液 D.品红溶液 E.澄清石灰水 F.酸性高锰酸钾溶液 G.碳酸氢钠溶液
为达到实验目的,按气流方向从左到右,上述装置所装试剂的连接顺序是_____ (用字母表示,所给试剂可以重复使用,有些试剂也可以不用)。

(1)装置A中装浓硫酸的仪器名称:
(2)装置B中的离子方程式是
(3)装置C中的实验现象是
(4)装置E中的现象是
(5)某同学制取的SO2气体中混有CO2气体,请你设计实验证明混合气体中既有SO2气体,又有CO2气体。可以选择如图洗气装置设计实验:

洗气装置中的溶液是。
A.浓硫酸 B.氢氧化钠溶液 C.硫酸铜溶液 D.品红溶液 E.澄清石灰水 F.酸性高锰酸钾溶液 G.碳酸氢钠溶液
为达到实验目的,按气流方向从左到右,上述装置所装试剂的连接顺序是
您最近一年使用:0次
名校
解题方法
8 . 下列装置和操作不能达到实验目的的是。
|
|
|
|
A.净化浓盐酸与 反应制得的 反应制得的 | B.验证氨气极易溶于水 | C.除去 中的 中的 杂质 杂质 | D.观察浓硝酸与铜反应的现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-03更新
|
746次组卷
|
5卷引用:四川省达州市万源中学2023-2024学年高一下学期4月期中考试化学试题
四川省达州市万源中学2023-2024学年高一下学期4月期中考试化学试题广东省茂名市第一中学2022-2023学年高三上学期期末化学诊断检测题(已下线)江苏省南京市、盐城市2021-2022学年高三第一次模拟考试(选择题6-10)(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(选择题1-5)重庆市2023届高三第一次联合诊断检测(一模)(康德卷)化学试题
名校
解题方法
9 . 用如图所示的装置进行实验(夹持及尾气处理仪器略去),能达到实验目的的是
选项 | a中试剂 | b中试剂 | c中试剂 | 实验目的 | 装置 |
A | 氨水 | CaO | 无 | 制备并收集氨气 |
|
B | 浓盐酸 | MnO2 | 饱和NaCl溶液 | 制备纯净的Cl2 | |
C | 醋酸 | Na2CO3 | 苯酚钠溶液 | 比较碳酸、醋酸、苯酚的酸性强弱 | |
D | 浓硫酸 | Na2SO3 | KMnO4酸性溶液 | 验证SO2具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)
(1)A中反应的化学方程式是_______ 。
(2)C中白色沉淀是_______ (填化学式,下同),C中液面上方生成的浅棕色气体是_______ 。
(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是_______ ;乙在A、B间增加洗气瓶D,D中盛放的试剂是_______ 。
②进行实验,B中现象:
检验白色沉淀,发现均不溶于稀盐酸,请写出乙中产生少量白色沉淀的离子方程式:_______ 。
(4)合并(3)中两同学的方案进行试验。B中无沉淀生成,而C中产生白色沉淀,根据甲、乙同学的实验目的可得出的结论是_______ 。
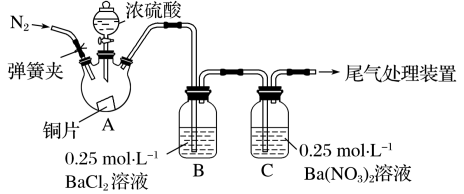
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 尚未发现白色沉淀溶解 |
(2)C中白色沉淀是
(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是
②进行实验,B中现象:
| 甲 | 大量白色沉淀 |
| 乙 | 少量白色沉淀 |
(4)合并(3)中两同学的方案进行试验。B中无沉淀生成,而C中产生白色沉淀,根据甲、乙同学的实验目的可得出的结论是
您最近一年使用:0次
2021-08-02更新
|
675次组卷
|
4卷引用:重庆市第八中学2020-2021学年高一下学期期中考试化学试题