1 . 为研究含硫化合物的性质,某兴趣小组在老师的指导下设计了如下实验。
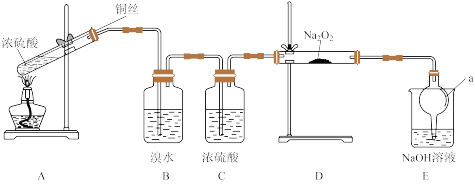
回答以下问题:
(1)A装置试管中主要反应的化学方程式是_______ 。反应中,浓硫酸表现出的性质是_______ (填正确选项的字母)。
A.酸性 B.氧化性 C.脱水性 D.吸水性
(2)仪器a的名称是_______ ,在本实验中的作用是_______ 。
(3)B中溴水出现的现象是_______ ,说明SO2具有的性质是_______ 。
(4)D中Na2O2与SO2反应生成Na2SO4,反应的化学方程式是_______
(5)实验中,取一定质量铜片和一定体积18mol·L-1硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是_______ 。
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是_______ (填字母)。
a.铁粉 b.BaCl2溶液 c.银粉 d.Na2CO3溶液

回答以下问题:
(1)A装置试管中主要反应的化学方程式是
A.酸性 B.氧化性 C.脱水性 D.吸水性
(2)仪器a的名称是
(3)B中溴水出现的现象是
(4)D中Na2O2与SO2反应生成Na2SO4,反应的化学方程式是
(5)实验中,取一定质量铜片和一定体积18mol·L-1硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是
a.铁粉 b.BaCl2溶液 c.银粉 d.Na2CO3溶液
您最近一年使用:0次
解题方法
2 . 下列关于金属或其化合物的说法中不正确的是
| A.工业上在高温下可用CO还原含Fe2O3的铁矿石炼铁 |
| B.过氧化钠具有强氧化性,可以用作漂白剂 |
| C.铝制容器一般不能装酸性或碱性试剂 |
| D.氯化铁溶液有较强氧化性,故可用作净水剂 |
您最近一年使用:0次
2020-12-03更新
|
136次组卷
|
2卷引用:陕西省西安市雁塔区第二中学2021-2022学年高一下学期第一次月考化学试题
名校
解题方法
3 . 下列实验操作后所得实验结论正确的是
| 实验操作 | 实验结论 | |
| A | 将X气体通入溶有 的 的 溶液中,出现白色沉淀 溶液中,出现白色沉淀 | X气体具有氧化性 |
| B | 向 溶液中加入少量的 溶液中加入少量的 粉末,产生红褐色沉淀 粉末,产生红褐色沉淀 | 硫酸亚铁溶液已变质 |
| C | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,金属铝熔化而不滴落下来 | 金属铝熔点比氧化铝低 |
| D | 向浓硫酸催化脱脂棉水解后的溶液中加入新制 浊液,加热,没有砖红色沉淀生成 浊液,加热,没有砖红色沉淀生成 | 水解的产物中不含还原性糖 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 为了探究过氧化钠的强氧化性,某小组设计了如图所示的实验装置。实验步骤及现象如图:
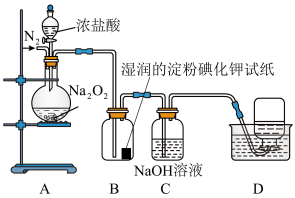
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,装置A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,关闭分液漏斗的活塞,再通一段时间N2,直至装置中气体变为无色。
回答下列问题:
(1)装置A中盛装浓盐酸的仪器是____ 。
(2)装置C的作用是____ 。
(3)装置D中收集到的无色气体能使带火星的木条复燃,解释产生该气体的原因是____ (用化学方程式表示)。
(4)装置B中湿润的淀粉碘化钾试纸变蓝。甲同学根据A中气体的颜色推测试纸变蓝时发生的反应可能是____ (写离子方程式)。

①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,装置A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,关闭分液漏斗的活塞,再通一段时间N2,直至装置中气体变为无色。
回答下列问题:
(1)装置A中盛装浓盐酸的仪器是
(2)装置C的作用是
(3)装置D中收集到的无色气体能使带火星的木条复燃,解释产生该气体的原因是
(4)装置B中湿润的淀粉碘化钾试纸变蓝。甲同学根据A中气体的颜色推测试纸变蓝时发生的反应可能是
您最近一年使用:0次
5 . 某化学课外活动小组通过实验探究NO能否与Na2O2反应以及反应后的产物,该小小组同学设计了如图所示装置(夹持仪器、连接用的乳胶管均已省略)。

经查阅资料知:①NO是不成盐氧化物;②2NO2+2NaOH=NaNO3+NaNO2+H2O
回答下列问题:
(1)写出木炭与浓硝酸反应的化学方程式:________________ 。
(2)为了完成实验,选择上图中的装置,其连接顺序为a→_______ (按气流方向,用小写字母表示);有同学认为该装置存在缺陷,则该缺陷是______________ 。
(3)连接好仪器,_____________ ,装入药品后,要通入一段时间的氮气,在滴入浓硝酸,点燃酒精灯,通入氮气的主要目的是_______________ 。
(4)装置E的作用是________________ ;能说明NO与Na2O2发生反应的实验现象是_____________ 。
(5)探究NO与Na2O2反应的产物。
假设1:产物只有NaNO3;假设2:_________________ ;
假设3:产物为NaNO3和NaNO2的混合物。
为验证反应产物,该小组同学准确称取反应后的固体3.50g,用煮沸并冷却后的蒸馏水配成100.00mL溶液,取10.00mL溶液于锥形瓶中,用0.1000mol·L-1KMnO4溶液(硫酸酸化)滴定,共消耗KMnO4溶液20mL。滴定过程中发生反应的离子方程式为___________________ ,反应产物中NaNO2的质量分数为_____ (保留四位有效数字)

经查阅资料知:①NO是不成盐氧化物;②2NO2+2NaOH=NaNO3+NaNO2+H2O
回答下列问题:
(1)写出木炭与浓硝酸反应的化学方程式:
(2)为了完成实验,选择上图中的装置,其连接顺序为a→
(3)连接好仪器,
(4)装置E的作用是
(5)探究NO与Na2O2反应的产物。
假设1:产物只有NaNO3;假设2:
假设3:产物为NaNO3和NaNO2的混合物。
为验证反应产物,该小组同学准确称取反应后的固体3.50g,用煮沸并冷却后的蒸馏水配成100.00mL溶液,取10.00mL溶液于锥形瓶中,用0.1000mol·L-1KMnO4溶液(硫酸酸化)滴定,共消耗KMnO4溶液20mL。滴定过程中发生反应的离子方程式为
您最近一年使用:0次
2017-04-01更新
|
418次组卷
|
2卷引用:陕西省吴起高级中学2019届高三上学期期中考试化学试题
名校
解题方法
6 . 下列说法正确的是( )
| A.因为SO2具有漂白性,所以它能使溴水、石蕊试液褪色 |
| B.湿润的氯气具有漂白作用,它能使石蕊试液先变红色再褪色 |
| C.SO2和Cl2都能使品红溶液褪色,两者等体积混合可以增强漂白能力 |
| D.Na2O2是碱性氧化物,具有强氧化性可用于杀菌消毒 |
您最近一年使用:0次
2020-05-12更新
|
125次组卷
|
2卷引用:陕西省咸阳市实验中学2020-2021学年高一上学期第四次月考化学试题
名校
解题方法
7 . 某实验小组设计以下实验装置来模仿防毒面具中的供氧原理,并收集氧气,回答下列问题。
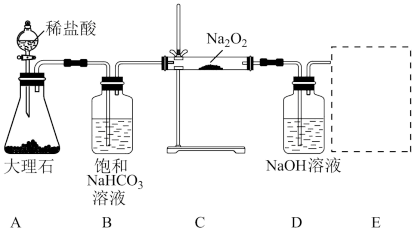
(1)请用离子方程式表示B装置中饱和NaHCO3溶液的作用:_______ ,请写出装置C中发生的两个化学反应方程式_______ 、_______
(2)装置C中发生反应的还原剂为_______ (写化学式),每生成1molO2,转移电子_______ 个。
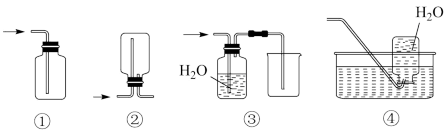
(3)E装置为氧气收集装置,如图4套气体收集装置中,合理的是_______ (填序号)
(4)Na2CO3溶液与NaCl溶液外观高度相似,请设计实验鉴别这两种溶液,写出实验操作和现象_______

(1)请用离子方程式表示B装置中饱和NaHCO3溶液的作用:
(2)装置C中发生反应的还原剂为
(3)E装置为氧气收集装置,如图4套气体收集装置中,合理的是

(4)Na2CO3溶液与NaCl溶液外观高度相似,请设计实验鉴别这两种溶液,写出实验操作和现象
您最近一年使用:0次



