2011·上海青浦·一模
解题方法
1 . 某学生用NaHCO3和KHCO3组成的某混合物与盐酸进行实验,测得下表数据(盐酸的物质的量浓度相等,体积均为50 mL)。
(1)则该学生所用盐酸的物质的量浓度是________________ mol/L;
(2)50 mL该盐酸恰好能溶解上述组成的混合物的质量是_________ g;
(3)上述固体混合物中NaHCO3的质量分数是_____________ (用小数表示,保留2位小数)。
实验编号 | Ⅰ | Ⅱ | Ⅲ |
盐酸的体积 | 50.0 mL | 50.0 mL | 50.0 mL |
m(混合物) | 9.2 g | 15.7 g | 27.6 g |
V(CO2)(标准状况) | 2.24 L | 3.36 L | 3.36 L |
(1)则该学生所用盐酸的物质的量浓度是
(2)50 mL该盐酸恰好能溶解上述组成的混合物的质量是
(3)上述固体混合物中NaHCO3的质量分数是
您最近一年使用:0次
2 . 某化学兴趣小组同学用实验室中一瓶久置的NaOH固体做了以下实验:先称取13.3 g NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入浓度为4 mol/L的盐酸,再根据生成CO2的体积计算出Na2CO3的质量,从而进一步计算出样品中变质NaOH的质量。
请回答下列问题:
(1)该实验的目的是_________________ 。
(2)已知20 ℃时,Na2CO3溶解度为21.7 g ,NaOH溶解度为108.3 g。若要将所称取的样品恰好溶解,最多需要蒸馏水____________ g,溶解样品所需的仪器是________________ 。
(3)实验测得加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:

则13.3 g 该样品中未变质的NaOH的质量为____________ ;NaOH的变质程度为_________ (用质量分数表示);与NaOH反应消耗的盐酸体积为________ mL。
(4)根据“与NaOH反应消耗盐酸的体积”,并对照上述图象,他们从实验中还发现了什么问题?_____________________ ,并由此得出了什么结论?____________________________ 。
请回答下列问题:
(1)该实验的目的是
(2)已知20 ℃时,Na2CO3溶解度为21.7 g ,NaOH溶解度为108.3 g。若要将所称取的样品恰好溶解,最多需要蒸馏水
(3)实验测得加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:

则13.3 g 该样品中未变质的NaOH的质量为
(4)根据“与NaOH反应消耗盐酸的体积”,并对照上述图象,他们从实验中还发现了什么问题?
您最近一年使用:0次
2019高三上·全国·专题练习
解题方法
3 . (1)研究性学习小组的同学,为测定某纯碱样品(含少量的氯化钠)中碳酸钠的质量分数,设计下列两种不同实验方案进行探究。
①方案1:取mg纯碱样品,溶于水加入过量的氯化钙溶液,过滤、用蒸馏水洗涤、烘干、称重得ag固体,计算出纯碱样品纯度。写出方案1发生反应的离子方程式___________ ;如何洗涤沉淀,方法是______________________ 。
②方案2:取mg纯碱样品,加入过量的盐酸,充分反应后,蒸发,灼烧,称重得bg固体,计算出纯碱样品纯度为___________________ 。
(2)将CO2通入NaOH和KOH的混合溶液中,恰好得到等物质的量混合的NaHCO3和 KHCO3的混合物ag,再将其与100mL 盐酸反应。(题中涉及的气体体积以标准状况计,填空时可以用带字母的数学式表示,不必化简)。
①该混合物中NaHCO3和KHCO3的质量比为_________________ 。
②如果反应后盐酸不足量,要计算生成CO2的体积,还需知道_________ 。
③若该混合物与盐酸恰好完全反应,则盐酸的物质的量浓度为_________ 。
④若NaHCO3和KHCO3不是以等物质的量混合,则ag固体混合物与足量的盐酸完全反应时,生成CO2的体积的取值范围是_____________ 。
①方案1:取mg纯碱样品,溶于水加入过量的氯化钙溶液,过滤、用蒸馏水洗涤、烘干、称重得ag固体,计算出纯碱样品纯度。写出方案1发生反应的离子方程式
②方案2:取mg纯碱样品,加入过量的盐酸,充分反应后,蒸发,灼烧,称重得bg固体,计算出纯碱样品纯度为
(2)将CO2通入NaOH和KOH的混合溶液中,恰好得到等物质的量混合的NaHCO3和 KHCO3的混合物ag,再将其与100mL 盐酸反应。(题中涉及的气体体积以标准状况计,填空时可以用带字母的数学式表示,不必化简)。
①该混合物中NaHCO3和KHCO3的质量比为
②如果反应后盐酸不足量,要计算生成CO2的体积,还需知道
③若该混合物与盐酸恰好完全反应,则盐酸的物质的量浓度为
④若NaHCO3和KHCO3不是以等物质的量混合,则ag固体混合物与足量的盐酸完全反应时,生成CO2的体积的取值范围是
您最近一年使用:0次
11-12高三·河南信阳·阶段练习
4 . 小苏打、胃舒平、达喜都是常用的中和胃酸的药物。
(1)小苏打每片含0.50gNaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是 mol
(2)胃舒平每片含0.245gAl(OH)3.中和胃酸时,6片小苏打相当于胃舒平 片
(3)达喜的化学成分是铝和镁的碱式盐:
取该碱式盐3.01g,加入2.0mol/L盐酸使其溶解,当加入盐酸42.5mL时开始产生CO2,加入盐酸至45.0mL时正好完全反应,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比
(1)小苏打每片含0.50gNaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是 mol
(2)胃舒平每片含0.245gAl(OH)3.中和胃酸时,6片小苏打相当于胃舒平 片
(3)达喜的化学成分是铝和镁的碱式盐:
取该碱式盐3.01g,加入2.0mol/L盐酸使其溶解,当加入盐酸42.5mL时开始产生CO2,加入盐酸至45.0mL时正好完全反应,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比
您最近一年使用:0次
11-12高三上·山西·阶段练习
5 . 小苏打、胃舒平、达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.42 gNaHCO3,2片小苏打片和胃酸完全中和,被中和的氢离子是
_______ mol。
(2)胃舒平每片含0.135 g Al(OH)3。中和胃酸时,6片小苏打片相当于胃舒平_____ 片。
(3)达喜的化学成分是铝和镁的碱式碳酸盐。
①取该碱式碳酸盐2.20g,加入2.0 mol·L-1盐酸使其溶解,当加入盐酸30 mL时开始产生CO2,加入盐酸至35 mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比_________ 。
②在上述碱式盐溶于盐酸后的溶液中加入过量氢氧化钠,过滤,沉淀物进行干燥后重1.16g,试推测该碱式盐的化学式_________ 。
(1)小苏打片每片含0.42 gNaHCO3,2片小苏打片和胃酸完全中和,被中和的氢离子是
(2)胃舒平每片含0.135 g Al(OH)3。中和胃酸时,6片小苏打片相当于胃舒平
(3)达喜的化学成分是铝和镁的碱式碳酸盐。
①取该碱式碳酸盐2.20g,加入2.0 mol·L-1盐酸使其溶解,当加入盐酸30 mL时开始产生CO2,加入盐酸至35 mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比
②在上述碱式盐溶于盐酸后的溶液中加入过量氢氧化钠,过滤,沉淀物进行干燥后重1.16g,试推测该碱式盐的化学式
您最近一年使用:0次
10-11高三上·辽宁沈阳·阶段练习
6 . 取物质的量浓度相等的NaOH溶液两份甲和乙,每份50 mL,分别向甲、乙中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的HCl溶液,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如下图所示,试回答下列问题:
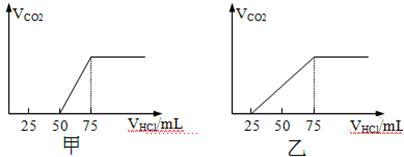
试分析NaOH在吸收CO2气体后,在甲所得溶液中存在的溶质是_________ ,其物质的量之比是_________ , 产生的CO2气体体积(标况)是___________ . 在乙所得溶液中存在的溶质是_________ ,其物质的量之比是___________ , 产生的CO2气体体积(标况)是_________ .

试分析NaOH在吸收CO2气体后,在甲所得溶液中存在的溶质是
您最近一年使用:0次
7 . 小苏打、胃舒、平达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.5g NaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是___________ mol。
(2)胃舒平每片含0.245g Al(OH)3。中和胃酸时,6片小苏打片相当于胃舒平_____ 片。
(3)达喜的化学成分是铝和镁的碱式盐。
①取该碱式盐3.01g,加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比。________
②在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后重1.74g,若该碱式盐中氢元素的质量分数为0.040,试推测该碱式盐的化学式。
________
(1)小苏打片每片含0.5g NaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是
(2)胃舒平每片含0.245g Al(OH)3。中和胃酸时,6片小苏打片相当于胃舒平
(3)达喜的化学成分是铝和镁的碱式盐。
①取该碱式盐3.01g,加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比。
②在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后重1.74g,若该碱式盐中氢元素的质量分数为0.040,试推测该碱式盐的化学式。
您最近一年使用:0次



