解题方法
1 .  和
和 是中学化学中常见的物质,在生产生活中有重要的用途。
是中学化学中常见的物质,在生产生活中有重要的用途。
i.某小组同学依据性质差异,采用比较的方法设计实验鉴别 和
和 。
。
(1)实验Ⅰ中,分别向两支试管中滴加几滴水,A中温度计示数略有降低,B中温度计示数升高。说明固体b与水作用的过程中_______ (填“放出”或“吸收”)热量,可判断固体b为 。
。
(2)实验Ⅱ中,向试管C和D中分别加入5mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。判断固体d为_______ (填化学式)。
(3)25℃时,在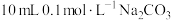 溶液中逐滴加入
溶液中逐滴加入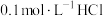 溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数(某微粒x的物质的量分数
溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数(某微粒x的物质的量分数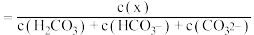
 )变化如图所示。请写出OAB段的离子方程式
)变化如图所示。请写出OAB段的离子方程式_______ 。

ii.实验室用 固体配制500 mL 0.10 mol/L的
固体配制500 mL 0.10 mol/L的 溶液,回答下列问题:
溶液,回答下列问题:
(4)称量的 固体质量应为
固体质量应为_______ g。
(5)实验操作的正确顺序是_______ 。(填序号)
①将称量好的 中加适量蒸馏水溶解在小烧杯中。
中加适量蒸馏水溶解在小烧杯中。
②将①所得溶液冷却到室温后,小心转入_______ (填仪器名称)中。
③将容量瓶瓶塞塞紧,充分摇匀。
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次。
⑤继续加蒸馏水至液面距刻度线1~2cm处,改用_______ (填仪器名称),小心滴加蒸馏水至溶液凹液面最低点与刻度线相切。
(6)取出100mL配制好的溶液,加蒸馏水稀释至 。则稀释后溶液的体积为
。则稀释后溶液的体积为_______ 。
(7)下列操作会使所配溶液的物质的量浓度偏低的是_______。(填字母序号)
 和
和 是中学化学中常见的物质,在生产生活中有重要的用途。
是中学化学中常见的物质,在生产生活中有重要的用途。i.某小组同学依据性质差异,采用比较的方法设计实验鉴别
 和
和 。
。| 实验Ⅰ | 实验Ⅱ |
 |  |
 。
。(2)实验Ⅱ中,向试管C和D中分别加入5mL水,充分振荡,试管C中固体有剩余,试管D中固体完全溶解。判断固体d为
(3)25℃时,在
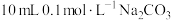 溶液中逐滴加入
溶液中逐滴加入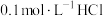 溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数(某微粒x的物质的量分数
溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数(某微粒x的物质的量分数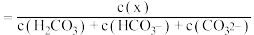
 )变化如图所示。请写出OAB段的离子方程式
)变化如图所示。请写出OAB段的离子方程式
ii.实验室用
 固体配制500 mL 0.10 mol/L的
固体配制500 mL 0.10 mol/L的 溶液,回答下列问题:
溶液,回答下列问题:(4)称量的
 固体质量应为
固体质量应为(5)实验操作的正确顺序是
①将称量好的
 中加适量蒸馏水溶解在小烧杯中。
中加适量蒸馏水溶解在小烧杯中。②将①所得溶液冷却到室温后,小心转入
③将容量瓶瓶塞塞紧,充分摇匀。
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次。
⑤继续加蒸馏水至液面距刻度线1~2cm处,改用
(6)取出100mL配制好的溶液,加蒸馏水稀释至
 。则稀释后溶液的体积为
。则稀释后溶液的体积为(7)下列操作会使所配溶液的物质的量浓度偏低的是_______。(填字母序号)
| A.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外 |
| B.定容时,俯视容量瓶上的刻度线 |
| C.加水定容时,水量超过了刻度线 |
| D.洗涤步骤中,洗涤液没有转入容量瓶 |
您最近一年使用:0次
解题方法
2 . 下列说法不正确的是
| A.物质的用途:碳酸钠可用于造纸;碳酸氢钠可以制作胃药 |
| B.离子的性质:金属阳离子只有氧化性,非金属阴离子只有还原性 |
C.物质的鉴别:用稀盐酸可一次性鉴别NaOH、 ,和 ,和 三种溶液 三种溶液 |
| D.物质的性质:还原剂转移电子给氧化剂 |
您最近一年使用:0次
2021-11-26更新
|
200次组卷
|
2卷引用:重庆市缙云教育联盟2022届高三第二次诊断性检测化学试题
解题方法
3 . [化学-选修2:化学与技术]碳酸钠的用途很广,可用做冶金、纺织、漂染等工业的基本原料。请根据题意回答下列问题:
Ⅰ.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法。其流程如下:
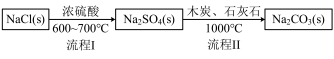
(1)流程I的另一产物是____ ,流程Ⅱ的反应分步进行:a. Na2SO4+C Na2S+CO↑
Na2S+CO↑
b.Na2S与石灰石发生复分解反应,总反应方程式可表示为__________________ 。
Ⅱ.1862年,比利时人索尔维(ErnestSolvay)用氨碱法生产碳酸钠。反应原理如下:
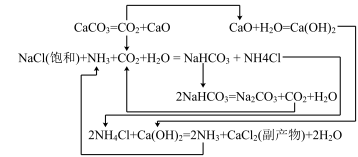
20℃时一些物质在水中的溶解度/g•(100gH2O)
(2)氨碱法生成纯碱的原料是____________ ,可循环利用的物质有____________ 。
(3)饱和NaCl溶液通NH3和CO2能生成NaHCO3的原因有:_________ 、__________ 、_________ 。
Ⅲ.我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原
料利用率。
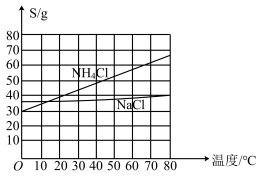
(4)生产中需向分离出NaHCO3后所得的溶液中加入NaCl固体并通入NH3,在________ (填温度范围)下析出________ (填化学式)。
Ⅰ.世界最早工业生产碳酸钠的方法是路布兰(N.Leblanc)法。其流程如下:

(1)流程I的另一产物是
 Na2S+CO↑
Na2S+CO↑ b.Na2S与石灰石发生复分解反应,总反应方程式可表示为
Ⅱ.1862年,比利时人索尔维(ErnestSolvay)用氨碱法生产碳酸钠。反应原理如下:

20℃时一些物质在水中的溶解度/g•(100gH2O)
| NaCl | NH4Cl | NaHCO3 | NH4HCO3 | Na2CO3 |
| 35.9 | 37.2 | 9.6 | 21.7 | 21.5 |
(3)饱和NaCl溶液通NH3和CO2能生成NaHCO3的原因有:
Ⅲ.我国化工专家侯德榜研究出联合制碱法,其反应原理和氨碱法类似,但将制氨和制碱联合,提高了原
料利用率。

(4)生产中需向分离出NaHCO3后所得的溶液中加入NaCl固体并通入NH3,在
您最近一年使用:0次
2016-12-09更新
|
268次组卷
|
2卷引用:2016届重庆市一中高三下学期模拟考试理综化学试卷



