名校
1 . 某金属与盐酸反应时,生成H2的质量与消耗金属的质量的关系如图所示,此金属可能是
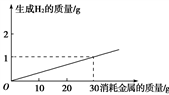

| A.纯锌 | B.纯铁 | C.镁铝合金 | D.铜铁合金 |
您最近一年使用:0次
2017-12-14更新
|
321次组卷
|
7卷引用:甘肃省兰州第一中学2017-2018学年高一12月月考化学试题
甘肃省兰州第一中学2017-2018学年高一12月月考化学试题(已下线)3.2.2 新型合金 物质的量在化学方程式计算中的应用练习(1)——《高中新教材同步备课》(人教版 必修第一册)广东省2020-2021学年高一12月大联考化学试题河北省秦皇岛一中2020-2021学年高一上学期期末考试化学试题贵州省毕节市赫章县2021-2022学年高一上学期期末考试化学试题云南省玉溪市通海县第一中学2022-2023学年高一上学期期中考试化学试题福建省德化一中、永安一中、漳平一中三校协作2022-2023学年高一下学期5月联考化学试题
名校
2 . 向体积和物质的量浓度都相等的盐酸和氢氧化钠溶液中投入足量的铝粉,放出的氢气在同温同压下的体积之比为
| A.1︰1 | B.1︰3 | C.3︰1 | D.1︰2 |
您最近一年使用:0次
2017-12-13更新
|
212次组卷
|
4卷引用:2015-2016学年贵州省贵阳市高一上学期期末化学试卷
3 . 两种金属的合金10g投入足量的稀硫酸中, 得到标况下氢气11.2L此合金可能是
| A.铁锌合金 | B.镁铁合金 | C.铝铁合金 | D.镁锌合金 |
您最近一年使用:0次
4 . 钠和铝均是重要的金属。
(1) 铝的原子结构示意图是___________________ 。
(2) 铝与NaOH溶液反应的离子方程式为
铝与NaOH溶液反应的离子方程式为______________________________ ;
(3)同温同压下,在体积和浓度均为100 mL 0.2 mol·L-1的盐酸及NaOH溶液中各加入等质量的Al, 产生气体的体积之比为5∶6,则所加Al的质量为______________ 。
(4) 过氧化钠可做呼吸面具的供氧剂,其中Na2O2与CO2反应的化学方程式为________________ 。
(1) 铝的原子结构示意图是
(2)
 铝与NaOH溶液反应的离子方程式为
铝与NaOH溶液反应的离子方程式为(3)同温同压下,在体积和浓度均为100 mL 0.2 mol·L-1的盐酸及NaOH溶液中各加入等质量的Al, 产生气体的体积之比为5∶6,则所加Al的质量为
(4) 过氧化钠可做呼吸面具的供氧剂,其中Na2O2与CO2反应的化学方程式为
您最近一年使用:0次
名校
5 . 下列说法错误的是
| A.铝制餐具不宜用来蒸煮或长时间存放酸性、碱性或咸的食物 |
| B.钛及钛合金用于飞机、火箭、导弹、人造卫星和宇宙飞船等领域 |
| C.明矾可以用作净水剂除去悬浮于水中的泥沙 |
| D.单质硅是现代光学及光纤制品的基本原料 |
您最近一年使用:0次
6 . 等物质的量且足量的两份铝分别与等浓度等体积的HCl与NaOH溶液充分反应后所得相同条件气体的体积比( )
| A.1:1 | B.1:3 | C.3:1 | D.1:2 |
您最近一年使用:0次
2017-11-29更新
|
374次组卷
|
2卷引用:河南省商丘市九校2017-2018学年高一上学期期中联考化学试题
7 . 将各为0.2mol的钠、镁和铝的固体相混合,分别加入到120mL的下列溶液中,充分反应后,放出氢气最多的是
| A.4mol/LHCl | B.4 mol/LHNO3 | C.8 mol/LNaOH | D.18 mol/LH2SO4 |
您最近一年使用:0次
名校
8 . 草酸铝是一种不溶于水和醇,溶于强酸的白色粉末,是重要的媒染剂。某化学兴趣小组设计实验从废弃铝—空气海水电池中回收铝并制备草酸铝晶体。
【实验过程】
(一)铝的回收
①称取16.0g废弃电池原料;
②用98.3%的硫酸进行酸浸、稀释、除杂、过滤;
③将滤液蒸干得到硫酸铝固体mlg。
(二)草酸铝的制备
④配制250mL0.20mol/L的硫酸铝溶液;
⑤量取0.10mol/L的草酸铵溶液20.00mL,并加入一定量的分散剂,缓缓加入配制的硫酸铝溶液25.00mL,搅拌lh;
⑥沉化、抽滤、洗涤、干燥、称量固体质量为m2g。
【问题讨论】
(1)在用98.3%的硫酸进行酸浸时,浸出率与条件的关系如图所示:
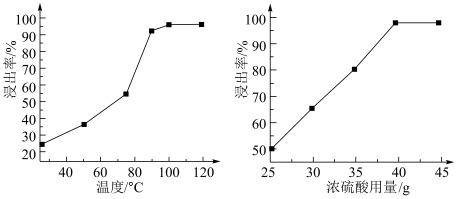
由图可知浓硫酸为浸取剂的最佳条件为________ 。
(2)步骤③蒸干溶液所需的仪器有带铁圈的铁架台、酒精灯、_______ 、_______ 。
(3)铝的回收率为_______ (回收率=回收铝的质量/原料的质量)。
(4)步骤⑥中洗涤晶体时先用蒸馏水再用乙醇洗涤,这样洗涤的原因是_______ 。
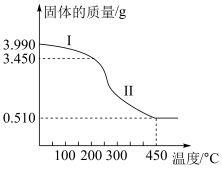
(5)该研究小组在实验过程中发现,若用0.90mol/L草酸铵进行实验,会导致沉淀的质量远超过实际草酸铝的质量。经分析,结晶生成物为(NH4)xAly(C2O4)z·nH2O。 现称取3.990g该结晶水合物进行热分解,得到剩余固体的质量随温度变化的曲线如下图所示。已知450℃时剩余固体只有Al2O3。第II阶段共产生气体2.016L (标准状况),该气体通入足量的石灰水中产生3.000g沉淀。请计算求出该结晶水合物的化学式为______ 。
【实验过程】
(一)铝的回收
①称取16.0g废弃电池原料;
②用98.3%的硫酸进行酸浸、稀释、除杂、过滤;
③将滤液蒸干得到硫酸铝固体mlg。
(二)草酸铝的制备
④配制250mL0.20mol/L的硫酸铝溶液;
⑤量取0.10mol/L的草酸铵溶液20.00mL,并加入一定量的分散剂,缓缓加入配制的硫酸铝溶液25.00mL,搅拌lh;
⑥沉化、抽滤、洗涤、干燥、称量固体质量为m2g。
【问题讨论】
(1)在用98.3%的硫酸进行酸浸时,浸出率与条件的关系如图所示:

由图可知浓硫酸为浸取剂的最佳条件为
(2)步骤③蒸干溶液所需的仪器有带铁圈的铁架台、酒精灯、
(3)铝的回收率为
(4)步骤⑥中洗涤晶体时先用蒸馏水再用乙醇洗涤,这样洗涤的原因是
(5)该研究小组在实验过程中发现,若用0.90mol/L草酸铵进行实验,会导致沉淀的质量远超过实际草酸铝的质量。经分析,结晶生成物为(NH4)xAly(C2O4)z·nH2O。 现称取3.990g该结晶水合物进行热分解,得到剩余固体的质量随温度变化的曲线如下图所示。已知450℃时剩余固体只有Al2O3。第II阶段共产生气体2.016L (标准状况),该气体通入足量的石灰水中产生3.000g沉淀。请计算求出该结晶水合物的化学式为

您最近一年使用:0次
2017-11-13更新
|
336次组卷
|
2卷引用:河南省郑州市第一中学2018届高三上学期期中考试化学试题
9 . Mg、Al、Fe 三种金属的混合物与足量的稀硫酸反应,生成 2.8L H2(标准状况)则三种金属的物 质的量之和不可能是( )
| A.0.12 mol | B.0.15 mol | C.0.08 mol | D.0.1 mol |
您最近一年使用:0次
名校
10 . 钠和铝都是常见的金属元素,下列关于钠和铝的叙述错误的是
| A.钠原子最外层只有一个电子 |
| B.钠在空气中充分燃烧的产物是Na2O |
| C.铝是地壳中含量最多的金属元素 |
| D.铝既能与盐酸反应,又能与NaOH溶液反应 |
您最近一年使用:0次
2017-11-03更新
|
200次组卷
|
2卷引用:吉林省长春外国语学校2017-2018学年高二上学期期中考试(文)化学试题



