名校
1 . 下列有关硫元素及其化合物的说法或描述不正确的是
A.在燃煤中加入石灰石可减少 排放,发生的反应为 排放,发生的反应为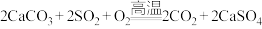 |
| B.浓硫酸可用铝罐车运输,是因为常温下铝和浓硫酸发生了钝化反应 |
| C.浓硫酸使纸张变黑,体现了脱水性 |
D. 具有还原性,浓硫酸具有强氧化性,所以不能用浓硫酸干燥 具有还原性,浓硫酸具有强氧化性,所以不能用浓硫酸干燥 |
您最近一年使用:0次
名校
2 . 下列有关物质的性质与应用相对应的是( )
| A.Na2O2具有强氧化性,可用作潜水艇的供氧剂 |
| B.SO2具有漂白性,能使紫色KMnO4溶液褪色 |
| C.K2FeO4具有还原性,可用于自来水的杀菌消毒 |
| D.浓硝酸在常温下能使铝钝化,可用铝槽车运输浓硝酸 |
您最近一年使用:0次
名校
解题方法
3 . 下列有关物质的性质与用途具有对应关系的是
| A.Al2O3具有两性,可用作耐高温材料 |
| B.NaHCO3溶液呈碱性,可用于制备纯碱 |
| C.铝具有良好导热性,可用作贮运浓硝酸 |
| D.FeCl3溶液具有氧化性,可用作蚀刻铜电路板 |
您最近一年使用:0次
2020-07-22更新
|
278次组卷
|
5卷引用:河北省唐山市第一中学2019-2020学年高一上学期12月质量检测化学试题
名校
4 . 下列实验操作、现象和结论均正确的是
| 实验操作 | 现象 | 结论 | |
| A | 将SO2通入溴水中 | 溴水褪色 | 体现了SO2的漂白性 |
| B | 将过量的过氧化钠投入滴有酚酞试液的水中 | 最终得红色溶液 | 过氧化钠与水反应生成碱性物质 |
| C | 铝丝用砂纸打磨后,放在冷的浓硝酸中浸泡一段时间后,放入CuSO4溶液中 | 铝丝表面变红色 | 铝可从铜盐溶液中置换出铜 |
| D | 将KI溶液和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-04-22更新
|
172次组卷
|
2卷引用:甘肃省天水市第一中学2017-2018学年高一下学期第一学段考试(理)化学试题
5 . 下列物质性质与应用不存在对应关系的是
| A.K2FeO4具有强氧化性,可用作水处理剂 |
| B.氢氧化铝具有弱碱性,可用作制胃酸中和剂 |
| C.碳具有还原性,可用作锌锰干电池的正极材料 |
| D.常温下浓硫酸能使铝发生钝化,可用铝制容器贮运浓硫酸 |
您最近一年使用:0次
名校
6 . 下列有关实验操作、现象和解释或结论都正确的是
| 实验操作 | 现象 | 解释或结论 | |
| ① | 过量的 粉中加入稀硝酸,充分反应后,滴入 粉中加入稀硝酸,充分反应后,滴入 溶液 溶液 | 溶液显红色 | 稀硝酸将 氧化为 氧化为 |
| ② | 浓硝酸久置或光照 | 变黄色 |  不稳定易分解 不稳定易分解 |
| ③ |  箔插入稀硝酸中 箔插入稀硝酸中 | 无现象 |  箔表面被 箔表面被 氧化,形成致密的氧化膜 氧化,形成致密的氧化膜 |
| ④ | 用玻璃棒蘸取浓硝酸点到蓝色石蕊试纸上 | 试纸先变红色后褪色 | 浓硝酸具有酸性和强氧化性 |
| A.①②③ | B.②④ | C.②③④ | D.③④ |
您最近一年使用:0次
2022-05-11更新
|
1375次组卷
|
4卷引用:福建省上杭县第一中学2022-2023学年高三上学期9月考试化学试题
7 . 下列有关实验操作、现象和解释或结论都正确的是
| 编号 | 实验操作 | 现象 | 解释或结论 |
| ① | 过量的Fe粉中加入稀硝酸,充分反应后滴入KSCN溶液 | 溶液呈红色 | 稀硝酸将Fe氧化为Fe3+ |
| ② | 浓硝酸久置或光照 | 变黄色 | HNO3不稳定易分解 |
| ③ | Al箔插入稀硝酸中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| ④ | 用玻璃棒蘸取浓硫酸点到蓝色石蕊试纸上 | 试纸先变红色后变黑 | 浓硫酸有酸性和强氧化性 |
| A.①② | B.③④ | C.②③④ | D.② |
您最近一年使用:0次
名校
8 . 对下列实验事实的结论表述正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向Na2CO3溶液中加入浓盐酸,将产生的气体直接通入硅酸钠溶液中 | 产生白色浑浊 | 酸性: 盐酸>碳酸>硅酸 |
| B | 将常温下用冷的浓硝酸处理过的铝片插入硫酸铜溶液中 | 铝片表面无明显现象 | 用硝酸处理后,铝的金属性减弱 |
| C | 取少量Na2SO3样品溶于蒸馏水,加入足量稀盐酸,再加入足量BaCl2溶液 | 有白色沉淀产生 | 样品已经变质 |
| D | 向黄色的Fe(NO3)3溶液中滴加氢碘酸,再加入四氯化碳 | 溶液变为紫红色 | 氧化性:Fe3+>I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-07-13更新
|
229次组卷
|
3卷引用:安徽省舒城中学2021-2022学年高二上学期第一次月考化学试题
9 . 下列对于N、S的化合物的性质解释错误的是
| A.浓H2SO4与铜片共热的反应中,浓H2SO4既表现出强氧化性,又表现出酸性 |
| B.常温下能够用铁、铝等容器盛放浓H2SO4,是因为浓H2SO4的强氧化性使其钝化 |
| C.NH4HCO3化肥需密封储存是因为NH4HCO3易分解 |
| D.把足量铜粉投入到含2 mol H2SO4的浓硫酸中,反应后得到标准状况下气体体积为22.4 L |
您最近一年使用:0次
10 . 下列对浓硫酸和浓硝酸的叙述中,正确的是
| A.常温下不能用铁、铝容器盛放浓硫酸和浓硝酸,因为铁、铝是活泼金属 |
| B.浓硫酸具有漂白性,可以使紫色石蕊褪色 |
| C.浓硝酸在空气中变黄,因为被空气中O2氧化 |
| D.浓硝酸和铜片反应,既表现了酸性,又表现出强氧化性 |
您最近一年使用:0次



