名校
1 . 硫酸铁是一种重要的化工原料,用铁矿石(主要成分为 ,还含有少量的FeO、
,还含有少量的FeO、 、
、 、有机杂质)制备硫酸铁的流程如下:
、有机杂质)制备硫酸铁的流程如下: 既不与酸反应,也不与水反应。
既不与酸反应,也不与水反应。
(1)请写出“浸出”过程中 与
与 反应的离子方程式:
反应的离子方程式:_______ ;浸出时,一边加入稀硫酸,一边搅拌的目的是_______ 。
(2)“滤渣X”的成分为_______ 。
(3)“氧化”的目的是_______ ;过程中发生的离子方程式为_______ 。
(4)证明滤液中 已沉淀完全的实验操作和结论为
已沉淀完全的实验操作和结论为_______ 。
(5)用相似的工艺还可以制取另一种含铁硫酸盐晶体——绿矾。绿矾产品可以制取摩尔盐,摩尔盐是一种重要的化工原料,广泛应用于医药冶金等领域,其化学组成可表示为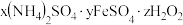 。为确定摩尔盐的组成,进行如下实验:
。为确定摩尔盐的组成,进行如下实验:
步骤一:称取一定量的新制摩尔盐,溶于水配制成100.00mL溶液A。
步骤二:准确量取10.00mL溶液A,加入足量 溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。
溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。
步骤三:另取10.00mL溶液A,加入0.0500
 酸性溶液,发生反应:
酸性溶液,发生反应: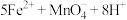
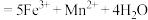 ,当两者恰好完全反应时,消耗
,当两者恰好完全反应时,消耗 溶液的体积为40.00mL。
溶液的体积为40.00mL。
通过计算确定摩尔盐中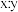 的值:
的值:_______ (写出计算过程)。
 ,还含有少量的FeO、
,还含有少量的FeO、 、
、 、有机杂质)制备硫酸铁的流程如下:
、有机杂质)制备硫酸铁的流程如下: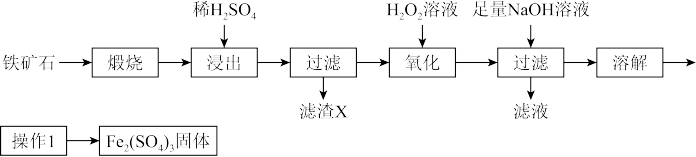
 既不与酸反应,也不与水反应。
既不与酸反应,也不与水反应。(1)请写出“浸出”过程中
 与
与 反应的离子方程式:
反应的离子方程式:(2)“滤渣X”的成分为
(3)“氧化”的目的是
(4)证明滤液中
 已沉淀完全的实验操作和结论为
已沉淀完全的实验操作和结论为(5)用相似的工艺还可以制取另一种含铁硫酸盐晶体——绿矾。绿矾产品可以制取摩尔盐,摩尔盐是一种重要的化工原料,广泛应用于医药冶金等领域,其化学组成可表示为
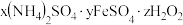 。为确定摩尔盐的组成,进行如下实验:
。为确定摩尔盐的组成,进行如下实验:步骤一:称取一定量的新制摩尔盐,溶于水配制成100.00mL溶液A。
步骤二:准确量取10.00mL溶液A,加入足量
 溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。
溶液,充分反应后过滤、洗涤、干燥,得白色固体4.660g。步骤三:另取10.00mL溶液A,加入0.0500

 酸性溶液,发生反应:
酸性溶液,发生反应: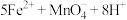
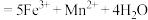 ,当两者恰好完全反应时,消耗
,当两者恰好完全反应时,消耗 溶液的体积为40.00mL。
溶液的体积为40.00mL。通过计算确定摩尔盐中
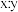 的值:
的值:
您最近一年使用:0次
2022-02-23更新
|
372次组卷
|
4卷引用:吉林省梅河口市第五中学2021-2022学年高一上学期期末联考化学试题
吉林省梅河口市第五中学2021-2022学年高一上学期期末联考化学试题吉林省松原市重点高中2021-2022学年高一3月联考化学试题辽宁省朝阳市凌源市2021-2022学年高一上学期期末考试化学试题(已下线)综合突破02 期末压轴80题之非选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
名校
解题方法
2 . 粉煤灰是燃煤产生的重要污染物,主要成分有Al2O3、Fe2O3、MgO和SiO2等物质。用硫酸铵固体等试剂提取粉煤灰中Al2O3并制取铝的工艺流程如图:

回答下列问题:
(1)已知烟气中含有NH3,煅烧工序中Al2O3参与反应的化学方程式为___ 。
(2)“滤渣Ⅰ”和“滤渣Ⅲ”主要成分的化学式分别为__ 、__ 。
(3)将“滤液Ⅱ”通过__ 、过滤、洗涤、干燥后得到的晶体可返回__ 工序中循环利用。
(4)向“滤液Ⅲ”中通入过量CO2,生成沉淀的离子方程式为__ 。
(5)电解Al2O3制备Al需要冰晶石(Na3AlF6)作助熔剂。Na3AlF6可由Al(OH)3、Na2CO3和HF反应制得,反应的化学方程式为__ 。
(6)某工厂利用上述流程从m吨粉煤灰中制得n吨Al2O3,则原粉煤灰中铝的质量分数为__ 。

回答下列问题:
(1)已知烟气中含有NH3,煅烧工序中Al2O3参与反应的化学方程式为
(2)“滤渣Ⅰ”和“滤渣Ⅲ”主要成分的化学式分别为
(3)将“滤液Ⅱ”通过
(4)向“滤液Ⅲ”中通入过量CO2,生成沉淀的离子方程式为
(5)电解Al2O3制备Al需要冰晶石(Na3AlF6)作助熔剂。Na3AlF6可由Al(OH)3、Na2CO3和HF反应制得,反应的化学方程式为
(6)某工厂利用上述流程从m吨粉煤灰中制得n吨Al2O3,则原粉煤灰中铝的质量分数为
您最近一年使用:0次
2020-06-18更新
|
464次组卷
|
2卷引用:吉林省长春外国语学校2021-2022学年高二下学期期末考试化学试题



