1 . 取一定体积的下列两种试剂(浓度均为 )进行反应,改变两种试剂的滴加顺序,反应产生的现象相同的是
)进行反应,改变两种试剂的滴加顺序,反应产生的现象相同的是
 )进行反应,改变两种试剂的滴加顺序,反应产生的现象相同的是
)进行反应,改变两种试剂的滴加顺序,反应产生的现象相同的是A. 溶液、稀盐酸 溶液、稀盐酸 | B. 溶液、氨水 溶液、氨水 |
C. 溶液、溴水 溶液、溴水 | D. 溶液、酸性 溶液、酸性 溶液 溶液 |
您最近一年使用:0次
解题方法
2 . 某同学用如图所示装置进行实验,预测现象与实际不相符的是
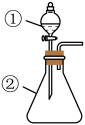

| ①中物质 | ②中物质 | 预期现象 | |
| A | 乙醇 | 酸性KMnO4溶液 | 紫色溶液颜色变浅或退去 |
| B | H2S溶液 | Na2SO3溶液 | 溶液变浑浊、产生气泡 |
| C | H2O2溶液 | 淀粉KI溶液 | 溶液变蓝 |
| D | 浓氨水 | AlCl3溶液 | 生成白色沉淀后又溶解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-03-19更新
|
1034次组卷
|
3卷引用:山东省烟台市、德州市、滨州市2023届高三一模考试化学试题
解题方法
3 . 2019年度诺贝尔化学奖奖励锂电池的发明者,锂离子电池已经彻底改变了我们的生活。如果废旧电池处理不当就会对环境造成严重污染,影响人们的健康生活。一种以废旧锂离子电池的正极材料(主要含LiCoO2、Al、C等)为原料制备CoC2O4·2H2O的流程如下:
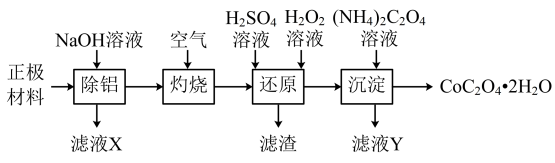
(1)除铝时发生反应的离子方程式为______________
(2)灼烧的主要目的是___________ ,实验室中灼烧实验用到最重要的仪器是_________
(3)还原步骤在70℃左右,LiCoO2发生反应的化学方程式为_____________ ,若用盐酸代替H2SO4和H2O2,也可以达到目的,但其缺点是___________________
(4)沉淀时,证明Co2+已经沉淀完全的实验操作与现象是__________________
(5)已知:NH3·H2O NH4++OH- Kb=1.8×10-5
NH4++OH- Kb=1.8×10-5
H2C2O4 H++HC2O4- Ka1=5.4×10-2
H++HC2O4- Ka1=5.4×10-2
HC2O4- H++C2O42- Ka2=5.4×10-5
H++C2O42- Ka2=5.4×10-5
则该流程中所用(NH4)2C2O4溶液的pH___ 7(填“>”或“<”或“=”)
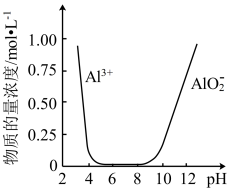
(6)已知含铝元素微粒的浓度与pH的关系如图所示,设计由滤液X制备纯净的Al2O3的实验方案________ (实验中必需使用的试剂:H2SO4溶液、BaCl2溶液、蒸馏水)

(1)除铝时发生反应的离子方程式为
(2)灼烧的主要目的是
(3)还原步骤在70℃左右,LiCoO2发生反应的化学方程式为
(4)沉淀时,证明Co2+已经沉淀完全的实验操作与现象是
(5)已知:NH3·H2O
 NH4++OH- Kb=1.8×10-5
NH4++OH- Kb=1.8×10-5H2C2O4
 H++HC2O4- Ka1=5.4×10-2
H++HC2O4- Ka1=5.4×10-2HC2O4-
 H++C2O42- Ka2=5.4×10-5
H++C2O42- Ka2=5.4×10-5则该流程中所用(NH4)2C2O4溶液的pH
(6)已知含铝元素微粒的浓度与pH的关系如图所示,设计由滤液X制备纯净的Al2O3的实验方案

您最近一年使用:0次
4 . A、B、C、D四种物质之间的转化关系如图所示(部分产物已略去),下列说法正确的是( )


| A.若A为AlCl3溶液,B可能为氨水,反应①的离子方程式为:A13++4NH3·H2O=AlO2−+ 4NH4++2H2O |
| B.若A为Fe,B可能为稀硝酸,反应②的离子方程式为: 3Fe+8H++2NO3−=3Fe2++2NO↑+4H2O |
| C.若A为NaOH溶液,B可能为CO2,可用Ca(OH)2溶液鉴别C、D溶液 |
| D.若A为Cl2,B可能为NH3,实验室可用加热固体C的方法制取NH3 |
您最近一年使用:0次
2017-03-11更新
|
517次组卷
|
5卷引用:山东省实验中学2018届高三上学期第二次诊断考试化学试题
2011·山东日照·一模
5 . 下列叙述正确的是
| A.氯化铝溶液中加入过量氨水的反应实质是:Al3++ 3NH3·H2O ===Al (OH)3↓ + 3NH4+ |
| B.常温常压下,22.4L乙烯中含C—H键的数目为4NA (NA表示阿伏加德罗常数的值) |
| C.加入KSCN溶液显红色的溶液中,Na+、Ca2+、HCO3-、I-可以大量共存 |
| D.标准状况下,2.24 L NH3溶于1L水中制得氨水,则c(NH3·H2O)=0.1mol·L-1 |
您最近一年使用:0次



