1 . 某学校化学学习小组为探究二氧化氮的性质,按如图所示装置进行实验。
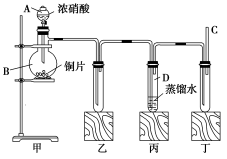
回答下列问题:
(1)装置甲中盛放浓硝酸的仪器A的名称是_____ ,该装置中发生反应的化学方程式为___ 。
(2)实验过程中,装置乙、丙中出现的现象分别是__________ 、____________ ;装置丙中的试管内发生反应的离子方程式为________________ (不是离子反应的不写)。
(3)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为________ 色,为了证明铁元素在该反应中的产物,可以再向溶液中滴加KSCN溶液,溶液变为________ 色。

回答下列问题:
(1)装置甲中盛放浓硝酸的仪器A的名称是
(2)实验过程中,装置乙、丙中出现的现象分别是
(3)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为
您最近一年使用:0次
2018-09-08更新
|
323次组卷
|
2卷引用:2018-2019学年高中化学鲁科版必修1 章末综合测评3
2 . 把表面有氧化物的铜片和铁片一起放入盐酸中充分反应后铁片未完全溶解,在该溶液中的金属离子应是( )
| A.只有Fe2+ | B.Fe3+和Cu2+ |
| C.Fe2+和Cu2+ | D.Fe3+和Fe2+ |
您最近一年使用:0次
3 . 某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
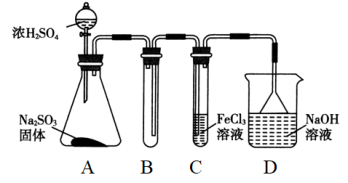
(1)通入足量SO2时C中观察到的现象是______________________ 。
(2)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:_______________________ ;
②请设计实验方案检验有Fe2+生成:_________________________ ;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法_____ (填“合理”或“不合理”),理由是______ 。
(3)D装置中倒置漏斗的作用是__________________________ 。
(4)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有________ (填字母)。
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液

(1)通入足量SO2时C中观察到的现象是
(2)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:
②请设计实验方案检验有Fe2+生成:
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法
(3)D装置中倒置漏斗的作用是
(4)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液
您最近一年使用:0次
2018-09-08更新
|
420次组卷
|
3卷引用:2018-2019学年高中化学鲁科版必修1 模块综合测评
名校
4 . 下列实验设计及其对应的离子方程式均正确的是( )
| A.把铁片插入CuSO4溶液中,验证古代湿法治铜:2Fe+3Cu2+===2Fe3++3Cu |
| B.某溶液中滴入KSCN溶液显红色,说明含Fe3+ |
| C.FeCl3溶液中加入铜粉:Fe3++Cu===Fe2++Cu |
| D.若要求用两种单质和一种溶液来测定Zn、Cu、Ag三种金属的活动性顺序,可用Zn、Cu和AgNO3溶液:Zn+2Ag+===Zn2++2Ag |
您最近一年使用:0次
2018-09-08更新
|
316次组卷
|
2卷引用:2018-2019学年高中化学鲁科版必修1 模块综合测评



