解题方法
1 . 某同学欲探究铁及其化合物的性质,下列实验方案可行的是
| A.将铁粉加入热的浓硫酸中:探究铁的活泼性 |
B.将热的NaOH溶液滴入 溶液中:制备 溶液中:制备 胶体 胶体 |
C.将铜粉加入 溶液中:验证 溶液中:验证 的氧化性强于 的氧化性强于 |
D.在蒸发皿中加热蒸干 溶液:制备 溶液:制备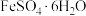 晶体 晶体 |
您最近半年使用:0次
2 . 下列技术应用中,其工作原理不涉及氧化还原 反应的是
 |  | 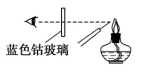 |  |
A.用 溶液浸泡 溶液浸泡 | B.用 和 和 合成 合成 | C.焰色试验 | D.用氧化铁冶炼铁 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
3 . 现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F、G,它们之间能发生如图反应(图中某些反应的产物及条件没有全部标出)
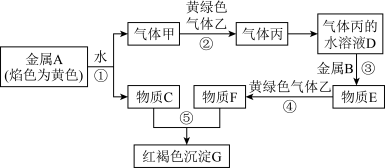
(1)物质G可以形成胶体和沉淀两种形式的分散系,实验室鉴别G的胶体和F的溶液,除了可通过观察颜色以外,还有的方法是_______ 。
(2)物质C中加入单质Al的离子反应方程式为_______________ ;
(3)向E的溶液加入NaOH溶液并且搅拌溶液,观察到的现象是______ ,请写出沉淀转化的化学方程式:________________ 。
(4)写出④离子反应方程式:________________ 。
(5)写出①发生的化学反应方程式的双线桥________ 。
(6)检验溶液F中阳离子实验方法是____________ 。
(7)向盛有H2O2溶液的试管中加入几滴酸化的物质E,溶液变成棕黄色,发生反应的离子方程式为__________________ 。

(1)物质G可以形成胶体和沉淀两种形式的分散系,实验室鉴别G的胶体和F的溶液,除了可通过观察颜色以外,还有的方法是
(2)物质C中加入单质Al的离子反应方程式为
(3)向E的溶液加入NaOH溶液并且搅拌溶液,观察到的现象是
(4)写出④离子反应方程式:
(5)写出①发生的化学反应方程式的双线桥
(6)检验溶液F中阳离子实验方法是
(7)向盛有H2O2溶液的试管中加入几滴酸化的物质E,溶液变成棕黄色,发生反应的离子方程式为
您最近半年使用:0次
名校
4 . 铁是人体必需的微量元素之一。黑木耳中的含铁量较高,为检验和测定干黑木耳样品中的铁元素,设计实验如下。回答下列问题:
Ⅰ.铁元素的检验

(1)“操作”是指________ ;上述流程中需要用到的仪器有托盘天平、烧杯、玻璃棒、酒精灯、漏斗,还有下图中的________ (填写仪器名称)。

(2)检验待测液中是否含有 、
、
Ⅱ.铁元素含量的测定
利用 标准溶液测定干黑木耳样品中铁元素的含量
标准溶液测定干黑木耳样品中铁元素的含量
步骤Ⅰ:取 待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
步骤Ⅱ:向步骤Ⅰ所得的溶液中加入适量稀 溶液,用
溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液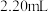 。
。
(3)步骤Ⅰ加入过量铜粉的目的是_________________________________ 。
(4)步骤Ⅱ滴加 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为_____________________ 。
(5)用 标准溶液滴定至终点的标志是:
标准溶液滴定至终点的标志是:___________ 。
(6)黑木耳中铁的含量为________ mg/100g(即每100g黑木耳中含铁元素质量)。
(7)若步骤Ⅰ过滤后未洗涤将使测定结果________ (填“偏大”或“偏小”或“无影响”)。
Ⅰ.铁元素的检验

(1)“操作”是指

(2)检验待测液中是否含有
 、
、
| 检验试剂 | 现象 | 结论 |
| KSCN溶液 | 溶液变为红色 | 滤液中含有 |
| ① | ② | 滤液中含有 |
Ⅱ.铁元素含量的测定
利用
 标准溶液测定干黑木耳样品中铁元素的含量
标准溶液测定干黑木耳样品中铁元素的含量步骤Ⅰ:取
 待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
待测液,加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。步骤Ⅱ:向步骤Ⅰ所得的溶液中加入适量稀
 溶液,用
溶液,用 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液
溶液 。
。(3)步骤Ⅰ加入过量铜粉的目的是
(4)步骤Ⅱ滴加
 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为(5)用
 标准溶液滴定至终点的标志是:
标准溶液滴定至终点的标志是:(6)黑木耳中铁的含量为
(7)若步骤Ⅰ过滤后未洗涤将使测定结果
您最近半年使用:0次
2024-04-03更新
|
133次组卷
|
2卷引用:天津市宁河区芦台第一中学2024届高三下学期适应性模拟训练(3月)化学试题
解题方法
5 . 下列实验设计不能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 检验溶液中FeSO4是否被氧化 | 取少量待测液,滴加KSCN溶液,观察溶液颜色变化 |
| B | 除去CO2中的HCl | 通过饱和NaHCO3溶液洗气后干燥 |
| C | 测定HClO溶液的pH | 将待测液滴在湿润的pH试纸上,与标准比色卡对照 |
| D | 除去Na2CO3固体中的NaHCO3 | 将固体加热至恒重 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
6 . 下列离子组一定能大量共存的是
A.含Fe3+的溶液中:SCN-、Cl-、 、Na+ 、Na+ |
B.石蕊呈蓝色的溶液中:Na+、[Al(OH)4]-、 、 、 |
C.饱和氯水中:K+、Cl-、Fe2+、 |
D.与Al反应产生氢气的溶液中: 、Cl-、K+、Na+ 、Cl-、K+、Na+ |
您最近半年使用:0次
名校
解题方法
7 . 下列方程式正确 的是
A.硫酸与氢氧化钡溶液混合: |
| B.铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
C.碳酸钙与盐酸反应: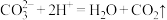 |
D.用 溶液腐蚀铜箔制造印刷电路板: 溶液腐蚀铜箔制造印刷电路板: |
您最近半年使用:0次
2024-03-25更新
|
53次组卷
|
2卷引用:天津市第八中学2023-2024学年高一上学期第一次大单元教学(9月月考)化学试题
8 . 下列叙述中,不正确的是
| A.高温下,铁和水蒸气反应可以生成氢气 |
| B.将饱和氯化铁溶液滴入沸水中,煮沸至红褐色,可以制得氢氧化铁胶体 |
| C.在硫酸铁溶液中,加入铜粉至完全溶解后,又加入一定量的铁粉,充分反应后有残余固体,则残余固体可能为铁、铜混合物 |
D.加入氯化钡溶液有白色沉淀生成,再加稀盐酸,沉淀不消失,一定有 |
您最近半年使用:0次
9 . 回答下列问题
(1)电子工业常用的30%的 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.刻蚀印刷电路板涉及的离子方程式为
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.刻蚀印刷电路板涉及的离子方程式为______ ,检验溶液中还有 的试剂
的试剂______ .
(2)工业上制取漂白粉的化学反应方程式为______ ;
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为______ .
(1)电子工业常用的30%的
 溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.刻蚀印刷电路板涉及的离子方程式为
溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板.刻蚀印刷电路板涉及的离子方程式为 的试剂
的试剂(2)工业上制取漂白粉的化学反应方程式为
(3)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为
您最近半年使用:0次
解题方法
10 . 铁及其化合物与生产、生活关系密切
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为__________
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是__________ (用化学方程式表示)
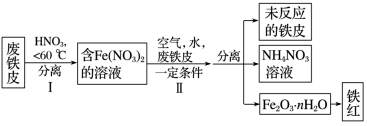
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:
①步骤Ⅰ若要检验是否有Fe3+生成,方法是__________
②步骤Ⅱ中发生反应: ,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是
,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是__________ (任写一项)。
(4) Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4
______ Fe2O3+______NaClO+______KOH ______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
①K2FeO4中铁元素的化合价__________ ;配平上述反应__________ 。此过程中氧化剂是__________ (填化学式)。
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是__________ 、__________ 。
(1)生铁(以赤铁矿为例)是通过高炉冶炼而得,用化学方程式表示其原理为
(2)在钢铁厂的生产中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理,不得留有水,原因是
(3)用废铁皮制取铁红(Fe2O3)的部分流程示意图如下:

①步骤Ⅰ若要检验是否有Fe3+生成,方法是
②步骤Ⅱ中发生反应:
 ,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是
,反应产生的HNO3又将废铁皮中的铁转化为Fe(NO3)2,能体现“绿色化学”思想的是(4) Fe2O3可制取新型、高效水处理剂高铁酸钾K2FeO4
______ Fe2O3+______NaClO+______KOH
 ______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O
______ K2FeO4(高铁酸钾)+ _____NaCl+_____H2O①K2FeO4中铁元素的化合价
②高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用是
您最近半年使用:0次



