1 . 由下列实验方案、现象得出的结论不正确的是
实验方案 | 现象 | 结论 | |
| A | 向FeCl3溶液中加入几滴KSCN溶液 | 溶液立即变红 | KSCN溶液可用来检验Fe3+ |
| B | 用毛皮摩擦过的带电橡胶靠近CF2Cl2液流 | 液流方向改变 | CF2Cl2是正四面体结构,为非极性分子 |
| C | 在碘水中加入CCl4,振荡 | 分层,下层紫红色 | I2在水中的溶解度小于在CCl4中的溶解度 |
| D | [Cu(NH3)4]SO4溶液中加入乙醇 | 析出深蓝色固体 | [Cu(NH3)4]SO4在乙醇中溶解度小 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-22更新
|
126次组卷
|
2卷引用:广西百色市田东县''贵百河“2023-2024学年高二下学期4月月考化学试题
名校
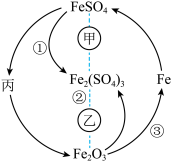
2 . 在一定条件下,某些物质具有如图所示的转化关系。丙为白色固体,其悬浊液在空气中会迅速变为灰绿色,最终变为红褐色。请回答下列问题:
(1)根据分析可知丙为________________ (填化学式);甲可能是__________ (填标号,下同),乙可能是__________ 。
A.稀硝酸 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液
(2)实验室保存 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量___________ (填药品名称);可以用______________ (填化学式)溶液来检验 溶液中的
溶液中的 是否被氧化。
是否被氧化。
(3)丙的悬浊液在空气中变色的原因为____________________ (填化学方程式);工业上高炉炼铁可以实现③的转化,所得到的炽热的铁水注入模具之前,模具必须进行充分的干燥处理,原因是____________________ (填化学方程式)。
(1)根据分析可知丙为
A.稀硝酸 B.
 溶液 C.
溶液 C. D.
D. 溶液
溶液(2)实验室保存
 溶液时,为了防止其被氧化,可以往溶液中加入适量
溶液时,为了防止其被氧化,可以往溶液中加入适量 溶液中的
溶液中的 是否被氧化。
是否被氧化。(3)丙的悬浊液在空气中变色的原因为
您最近半年使用:0次
2024-04-21更新
|
94次组卷
|
2卷引用:广西壮族自治区百所名校2023-2024学年高一下学期3月联合考试化学试题
名校
解题方法
3 . 下列离子能够在指定溶液中大量共存的是
A.在强碱性溶液中: 、 、 、 、 、 、 |
B.在酸性溶液中: 、 、 、 、 、 、 |
C.在澄清透明溶液中: 、 、 、 、 、 、 |
D.在pH=1的溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
名校
解题方法
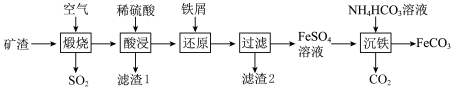
4 . 利用金属矿渣(含有FeS2、SiO2及Cu2O)制备FeCO3的实验流程如下。已知煅烧过程中FeS2和Cu2O转化为Fe2O3和CuO。______ (写化学式),该物质是工业制备高纯度硅的原料,写出硅与氯化氢在高温条件下发生的化学方程式:________ 。
(2)FeS2在空气中煅烧的化学方程式为______ 。
(3)在“还原”步骤,在向酸浸后溶液加入过量铁屑,除了能将 转化为
转化为 外,还能
外,还能______ 。若将6 g铁粉加入200 mL  和CuSO4的混合溶液中,充分反应得到200 mL
和CuSO4的混合溶液中,充分反应得到200 mL  FeSO4溶液和5.2 g固体沉淀物。
FeSO4溶液和5.2 g固体沉淀物。
①5.2 g固体沉淀物的成份为_______ (写化学式)。
②原 溶液的物质的量浓度是
溶液的物质的量浓度是_______ 。
(4)检验 是否完全被还原的实验操作是
是否完全被还原的实验操作是_______ 。
(5)制备FeCO3,写出“沉铁”步骤发生反应的离子方程式:_______ 。
(2)FeS2在空气中煅烧的化学方程式为
(3)在“还原”步骤,在向酸浸后溶液加入过量铁屑,除了能将
 转化为
转化为 外,还能
外,还能 和CuSO4的混合溶液中,充分反应得到200 mL
和CuSO4的混合溶液中,充分反应得到200 mL  FeSO4溶液和5.2 g固体沉淀物。
FeSO4溶液和5.2 g固体沉淀物。①5.2 g固体沉淀物的成份为
②原
 溶液的物质的量浓度是
溶液的物质的量浓度是(4)检验
 是否完全被还原的实验操作是
是否完全被还原的实验操作是(5)制备FeCO3,写出“沉铁”步骤发生反应的离子方程式:
您最近半年使用:0次
5 . 用FeCl3溶液腐蚀覆铜板产生的腐蚀废液可回收利用,实验流程如下。下列有关说法错误的是
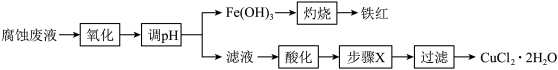

| A.“氧化”步骤中可用的试剂为氯气 |
| B.“调pH”后,检验Fe3+是否沉淀完全的操作为:取少量上层清液于试管中,滴加几滴酸性KMnO4溶液,观察溶液紫色是否褪去 |
| C.进行“灼烧”操作时需用到的仪器有坩埚和酒精灯 |
| D.“步骤X”包含的操作有蒸发浓缩、冷却结晶 |
您最近半年使用:0次
6 . 下列说法错误的是
A. 既有氧化性也有还原性 既有氧化性也有还原性 |
| B.化合反应一定是氧化还原反应 |
C.保存 溶液时加入Fe粉防止 溶液时加入Fe粉防止 被氧化 被氧化 |
D.除去 溶液中的 溶液中的 ,可加入氯水 ,可加入氯水 |
您最近半年使用:0次
7 . 下列实验方案能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 除去Fe2O3固体中的Al2O3 | 加入足量NaOH溶液、过滤、洗涤、干燥 |
| B | 检验溶液中是否含有 | 向溶液中加入 溶液,产生白色浑浊 溶液,产生白色浑浊 |
| C | 证明铁比铜还原性强 | 用 溶液腐蚀 溶液腐蚀 刻制印刷电路板 刻制印刷电路板 |
| D | 验证非金属性Cl>C | 向Na2CO3溶液中滴加足量HCl,观察有无气泡产生 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
8 . 某小组同学探究久置 固体变质的情况,并测定其中铁元素的质量分数。将
固体变质的情况,并测定其中铁元素的质量分数。将 固体用蒸馏水溶解,配成
固体用蒸馏水溶解,配成 待测液,进行实验。
待测液,进行实验。
资料: 中S元素的化合价为-2价:酸性条件下,
中S元素的化合价为-2价:酸性条件下, 的还原产物为
的还原产物为 。
。
(1)实验一:
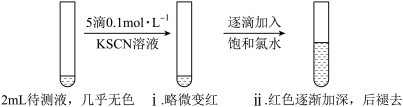
①i中溶液略微变红,说明待测液中存在___________ 。
②ii中溶液颜色逐渐加深的原因是___________ 。
③由实验一推测 固体变质的情况是
固体变质的情况是___________ (填字母序号)。
a.未变质 b.部分变质 c.完全变质
(2)实验二:探究ii中“红色褪去”的原因。
针对“红色褪去”的现象,小组同学猜想可能的原因是___________ ,并通过如下实验证实了猜想。将褪色后的溶液分两份分别进行实验,请补全①中的操作和②中的现象。
(3)实验三:将 固体用蒸馏水溶解,配成
固体用蒸馏水溶解,配成 待测液,进行实验,测定久置
待测液,进行实验,测定久置 固体中铁元素的含量。设计实验方案如图:
固体中铁元素的含量。设计实验方案如图:
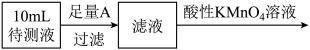
①可选作A的物质是___________ (填字母序号)。
a. b.
b. c.
c. d.
d.
②若消耗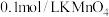 溶液
溶液 ,则久置
,则久置 固体中铁元素的质量分数是
固体中铁元素的质量分数是___________ 。
 固体变质的情况,并测定其中铁元素的质量分数。将
固体变质的情况,并测定其中铁元素的质量分数。将 固体用蒸馏水溶解,配成
固体用蒸馏水溶解,配成 待测液,进行实验。
待测液,进行实验。资料:
 中S元素的化合价为-2价:酸性条件下,
中S元素的化合价为-2价:酸性条件下, 的还原产物为
的还原产物为 。
。(1)实验一:

①i中溶液略微变红,说明待测液中存在
②ii中溶液颜色逐渐加深的原因是
③由实验一推测
 固体变质的情况是
固体变质的情况是a.未变质 b.部分变质 c.完全变质
(2)实验二:探究ii中“红色褪去”的原因。
针对“红色褪去”的现象,小组同学猜想可能的原因是
| 序号 | 操作 | 现象 |
| ① | 产生红褐色沉淀 | |
| ② | 滴加 溶液 溶液 |
(3)实验三:将
 固体用蒸馏水溶解,配成
固体用蒸馏水溶解,配成 待测液,进行实验,测定久置
待测液,进行实验,测定久置 固体中铁元素的含量。设计实验方案如图:
固体中铁元素的含量。设计实验方案如图:
①可选作A的物质是
a.
 b.
b. c.
c. d.
d.
②若消耗
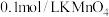 溶液
溶液 ,则久置
,则久置 固体中铁元素的质量分数是
固体中铁元素的质量分数是
您最近半年使用:0次
9 . 下列实验操作和现象所得结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向某无色溶液中滴加稀盐酸 | 溶液变浑浊 | 原溶液中一定存在 |
B | 将铜片投入到 溶液中,然后加入稀硫酸 溶液中,然后加入稀硫酸 | 铜片投入到 溶液中无明显现象,加入稀硫酸后,铜片溶解 溶液中无明显现象,加入稀硫酸后,铜片溶解 | 铜能溶于稀硫酸 |
C | 向某含铁溶液中加入适量的NaOH溶液 | 得到红褐色沉淀 | 原溶液中含有 不含有 不含有 |
D | 向含有酚酞的氢氧化钠稀溶液中慢慢通入 | 溶液红色褪去 | 体现了 的酸性 的酸性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
10 . 铝和铁是地壳中含量较多的金属元素,其单质和化合物广泛应用于日常生活中。回答下列问题:
(1)工业制印刷电路板的原理为用 做腐蚀液,将覆铜板上不需要的铜腐蚀。写出相关反应的离子方程式:
做腐蚀液,将覆铜板上不需要的铜腐蚀。写出相关反应的离子方程式:_______ 。
(2)向 溶液中加入
溶液中加入 溶液时,生成的
溶液时,生成的_______ 色絮状沉淀最终变为_______ 色的_______ (填化学式)。
(3)甲、乙两烧杯中分别盛有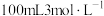 盐酸和
盐酸和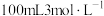 氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2(同温同压下),则加入铝粉的质量为
氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2(同温同压下),则加入铝粉的质量为_______ g。
(4)如图是从铝土矿(主要成分为 ,还含有少量
,还含有少量 等杂质)中提取
等杂质)中提取 并生产
并生产 的工艺流程:
的工艺流程:
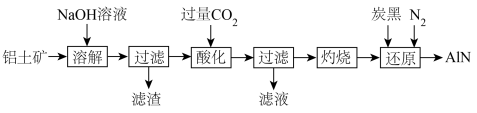
①“滤渣”的主要成分为_______ (填化学式,下同),滤液中溶液的主要成分为_______ 。
②向“滤渣”中加入稀硫酸后,检验反应后溶液中存在 的试剂为
的试剂为_______ (填字母)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
③过滤操作中需要用到的玻璃仪器有_______ 。
④“还原”时,炭黑在高温下被氧化为 ,该还原过程中发生的化学反应方程式为
,该还原过程中发生的化学反应方程式为_______ 。
(1)工业制印刷电路板的原理为用
 做腐蚀液,将覆铜板上不需要的铜腐蚀。写出相关反应的离子方程式:
做腐蚀液,将覆铜板上不需要的铜腐蚀。写出相关反应的离子方程式:(2)向
 溶液中加入
溶液中加入 溶液时,生成的
溶液时,生成的(3)甲、乙两烧杯中分别盛有
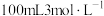 盐酸和
盐酸和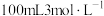 氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2(同温同压下),则加入铝粉的质量为
氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得甲、乙两烧杯中产生的气体体积之比为1:2(同温同压下),则加入铝粉的质量为(4)如图是从铝土矿(主要成分为
 ,还含有少量
,还含有少量 等杂质)中提取
等杂质)中提取 并生产
并生产 的工艺流程:
的工艺流程:
①“滤渣”的主要成分为
②向“滤渣”中加入稀硫酸后,检验反应后溶液中存在
 的试剂为
的试剂为A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液③过滤操作中需要用到的玻璃仪器有
④“还原”时,炭黑在高温下被氧化为
 ,该还原过程中发生的化学反应方程式为
,该还原过程中发生的化学反应方程式为
您最近半年使用:0次



