1 . 某兴趣小组利用下列试剂:铁粉、锌粉、0.1 mol·L-1 FeCl2溶液、KSCN溶液、新制氯水,探究Fe2+、Fe3+的氧化性、还原性,并利用实验结论解决一些问题。
(1)用所给试剂写出体现Fe2+具有还原性的反应的离子反应方程式:___________ 。
(2)设计实验方案,完成下列表格。
(3)该兴趣小组未说明“Fe2+具有氧化性”,提出了向FeCl2溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为___________ 。
(4)某反应中反应物与生成物有Fe2+ 、Fe3+、 、H2O、H+和一种未知离子X。
、H2O、H+和一种未知离子X。
①已知氧化性: >Fe3+ ,则X离子是
>Fe3+ ,则X离子是___________ 。
②该反应的离子方程式是___________ 。
(1)用所给试剂写出体现Fe2+具有还原性的反应的离子反应方程式:
(2)设计实验方案,完成下列表格。
| 探究内容 | 实验方案 | 实验现象 |
| 探究Fe3+的化学性质 | 取少量0.1 mol ·L-1 FeCl3溶液,往溶液中加入 足量铁粉,再加入少量KSCN溶液 | 加入铁粉后 ,溶液颜色为 加入KSCN溶液后,溶液颜色 |
| 结论:Fe3+具有 | ||
(4)某反应中反应物与生成物有Fe2+ 、Fe3+、
 、H2O、H+和一种未知离子X。
、H2O、H+和一种未知离子X。①已知氧化性:
 >Fe3+ ,则X离子是
>Fe3+ ,则X离子是②该反应的离子方程式是
您最近一年使用:0次
2 . 下列依据实验操作及现象所得出的结论不正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向CCl4中滴入少量浓溴水,振荡,静置 | 溶液分层,上层几乎无色,下层为橙红色 | Br2在CCl4中的溶解度比在水中的大 |
| B | FeCl3溶液滴在淀粉一KI试纸上 | 试纸变蓝 | 2Fe2++2I-=2Fe2++I2 |
| C | 向浓度均为0.1 mol/L NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 将 SO2通入含氨水的BaCl2溶液中 | 产生白色沉淀 | 白色沉淀为BaSO4 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 铁是人体必需的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物,“速力菲”(主要成分为的琥珀酸亚铁,即丁二酸亚铁)是市场上一种常用的补铁药物,它难溶于水,但在人体胃酸的作用下可以释放出Fe2+,从而被人体吸收。
(1)某同学为了检验其中的Fe2+,将药物研磨、水溶后过滤。
①如图是某学生的过滤操作示意图,其操作不规范的是___ (填标号)
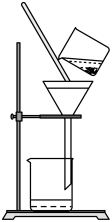
a.玻璃棒用作引流
b.漏斗末端颈尖未紧靠烧杯壁
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中搅动以加快过滤速度
②取少量所得滤液,分别加入 K3Fe(CN)6溶液(一种检验Fe2+的试剂)和KSCN溶液(一种检验Fe3+的试剂),均未出现明显现象。其主要原因是___ 。
(2)取酸性环境下“速力菲”溶解过滤后的滤液敞口放置在空气中一段时间,然后滴入KSCN溶液,溶液立即呈现血红色说明有Fe3+生成,说明Fe2+___ 。
(3)医生通常会建议:与维生素C同时服用,能增强“速力菲”的补铁效果。此举是利用了维生素C的___ 。(填“氧化性”、“还原性”或“碱性”)
(1)某同学为了检验其中的Fe2+,将药物研磨、水溶后过滤。
①如图是某学生的过滤操作示意图,其操作不规范的是

a.玻璃棒用作引流
b.漏斗末端颈尖未紧靠烧杯壁
c.将滤纸湿润,使其紧贴漏斗壁
d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中搅动以加快过滤速度
②取少量所得滤液,分别加入 K3Fe(CN)6溶液(一种检验Fe2+的试剂)和KSCN溶液(一种检验Fe3+的试剂),均未出现明显现象。其主要原因是
(2)取酸性环境下“速力菲”溶解过滤后的滤液敞口放置在空气中一段时间,然后滴入KSCN溶液,溶液立即呈现血红色说明有Fe3+生成,说明Fe2+
(3)医生通常会建议:与维生素C同时服用,能增强“速力菲”的补铁效果。此举是利用了维生素C的
您最近一年使用:0次



