解题方法
1 . 某合作学习小组将铜片放进氯化铁溶液中,观察到溶液呈无色,产生红褐色固体,铜片表面有白色物质。
Ⅰ.探究红褐色固体成分
(1)过滤得到红褐色固体,所需的仪器有___________ (填标号)。___________ 溶液,溶液变血红色,证明是氢氧化铁。
②产生氢氧化铁的原因可能是___________ (用化学方程式表示)。
Ⅱ.查阅资料:CuCl是白色难溶物
(3)探究产生白色物质的原因。设计实验方案如下:
①由以上实验可知,产生白色物质的条件是___________ 。
②实验2生成白色物质的化学方程式为:___________ 。
③请你从氧化还原反应规律角度分析实验1中未产生白色物质的原因___________ 。
(4)以石墨为电极电解 溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为
溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为___________ 。
(5)基于上述分析,用 溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用
溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用 、KCl、盐酸混合物腐蚀覆铜板,原理为:
、KCl、盐酸混合物腐蚀覆铜板,原理为: 。
。
①基态 的价电子轨道表示式为
的价电子轨道表示式为___________ 。
②KCl的作用是___________ 。
(6)氧化还原反应的应用十分广泛。写出一种氧化剂在生活中的应用___________ 。
Ⅰ.探究红褐色固体成分
(1)过滤得到红褐色固体,所需的仪器有
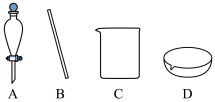
②产生氢氧化铁的原因可能是
Ⅱ.查阅资料:CuCl是白色难溶物
(3)探究产生白色物质的原因。设计实验方案如下:
| 实验 | 铜粉/g | 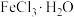 /g /g | 蒸馏水/mL | 实验现象 |
| 1 | 0.1 | 1.8 | 2 | 棕黄色溶液变为墨绿色 |
| 2 | 0.5 | 1.8 | 2 | 棕黄色溶液变为白色浊液 |
②实验2生成白色物质的化学方程式为:
③请你从氧化还原反应规律角度分析实验1中未产生白色物质的原因
(4)以石墨为电极电解
 溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为
溶液,发现在石墨上析出的铜在切断电源后消失。从电化学角度进行分析,铜消失的原因为(5)基于上述分析,用
 溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用
溶液腐蚀覆铜板效果不理想。查阅资料:工业上常用 、KCl、盐酸混合物腐蚀覆铜板,原理为:
、KCl、盐酸混合物腐蚀覆铜板,原理为: 。
。①基态
 的价电子轨道表示式为
的价电子轨道表示式为②KCl的作用是
(6)氧化还原反应的应用十分广泛。写出一种氧化剂在生活中的应用
您最近半年使用:0次
解题方法
2 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 铁粉样品中加足量稀硫酸溶解后,滴入两滴 溶液不变红 溶液不变红 | 铁粉未变质 |
| B | 用 试纸测定 试纸测定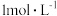 的 的 和 和 溶液的 溶液的 ,前者的试纸颜色比后者深 ,前者的试纸颜色比后者深 | 非金属性: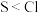 |
| C | 充分加热铁粉和硫粉的混合物,冷却后取少量固体于试管中,加入足量稀硫酸,再滴入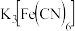 溶液,产生蓝色沉淀 溶液,产生蓝色沉淀 | 铁被硫氧化至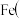 Ⅱ Ⅱ |
| D | 向新制硫酸亚铁溶液中滴加邻二氮菲 | 与邻二氮菲配位能力: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
3 . 下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 用 | 氧化性: |
B |
|
|
C | 液氨可用作制冷剂 | 氨气极易溶于水 |
D | Na着火不能用水扑灭 | Na可与水反应产生 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
4 .  在生产和生活中用途广泛。
在生产和生活中用途广泛。
Ⅰ. 溶液的配制及浓度的标定
溶液的配制及浓度的标定
(1) 溶液的配制
溶液的配制
①配制100mL一定浓度的 溶液需用到的仪器有
溶液需用到的仪器有___________ (填字母)。 溶液时,需要将
溶液时,需要将 固体溶解在浓盐酸中,原因为
固体溶解在浓盐酸中,原因为___________ 。
(2) 溶液浓度的标定
溶液浓度的标定
量取10.00mL 溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用
溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用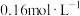
 标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗
标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗 标准溶液的体积为20.00mL,已知:
标准溶液的体积为20.00mL,已知: ,则该
,则该 溶液的浓度为
溶液的浓度为___________  。
。
Ⅱ. 与
与 反应的探究
反应的探究
(3)预测现象1:向 溶液中加入
溶液中加入 溶液,溶液由黄色变为浅绿色。作出该预测的原因为
溶液,溶液由黄色变为浅绿色。作出该预测的原因为___________ (用离子方程式表示)。
预测现象2:向 溶液中加入
溶液中加入 溶液,生成红褐色沉淀。
溶液,生成红褐色沉淀。
(4)实验验证:小组同学设计以下实验探究溶液中 浓度相同时
浓度相同时 的加入量对反应的影响,其中
的加入量对反应的影响,其中 溶液为Ⅰ中所配溶液,
溶液为Ⅰ中所配溶液, 溶液浓度为
溶液浓度为 。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
①请补充表格中的数据:a=___________ 。
②实验ⅱ~ⅳ中,反应后溶液的pH基本不变,其原因可能是___________ 。
③实验ⅵ和ⅶ的实验现象说明溶液中 的水解与
的水解与 的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:
的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:___________ 。
④甲同学认为实验ⅵ和ⅶ中, 与
与 除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,
除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,___________ (填实验操作与现象),则说明猜想成立。
(5)请举出一种水解反应在生产或生活中的应用:___________ 。
 在生产和生活中用途广泛。
在生产和生活中用途广泛。Ⅰ.
 溶液的配制及浓度的标定
溶液的配制及浓度的标定(1)
 溶液的配制
溶液的配制①配制100mL一定浓度的
 溶液需用到的仪器有
溶液需用到的仪器有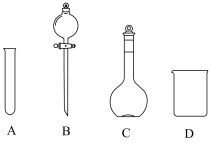
 溶液时,需要将
溶液时,需要将 固体溶解在浓盐酸中,原因为
固体溶解在浓盐酸中,原因为(2)
 溶液浓度的标定
溶液浓度的标定量取10.00mL
 溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用
溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用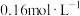
 标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗
标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗 标准溶液的体积为20.00mL,已知:
标准溶液的体积为20.00mL,已知: ,则该
,则该 溶液的浓度为
溶液的浓度为 。
。Ⅱ.
 与
与 反应的探究
反应的探究(3)预测现象1:向
 溶液中加入
溶液中加入 溶液,溶液由黄色变为浅绿色。作出该预测的原因为
溶液,溶液由黄色变为浅绿色。作出该预测的原因为预测现象2:向
 溶液中加入
溶液中加入 溶液,生成红褐色沉淀。
溶液,生成红褐色沉淀。(4)实验验证:小组同学设计以下实验探究溶液中
 浓度相同时
浓度相同时 的加入量对反应的影响,其中
的加入量对反应的影响,其中 溶液为Ⅰ中所配溶液,
溶液为Ⅰ中所配溶液, 溶液浓度为
溶液浓度为 。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
。静置6小时观察现象,测定反应后溶液的pH,并记录数据:| 序号 | ⅰ | ⅱ | ⅲ | ⅳ | ⅴ | ⅵ | ⅶ |
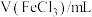 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 |
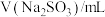 | 0 | 1.0 | 2.0 | 5.0 | a | 20.0 | 26.0 |
 | 38.0 | 37.0 | 36.0 | 33.0 | 23.0 | 18.0 | 12.0 |
| 现象 | 溶液接近无色透明 | 出现褐色沉淀 | |||||
| pH | 1.7 | 1.7 | 1.7 | 1.8 | 2.8 | 5.4 | 6.2 |
②实验ⅱ~ⅳ中,反应后溶液的pH基本不变,其原因可能是
③实验ⅵ和ⅶ的实验现象说明溶液中
 的水解与
的水解与 的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:
的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:④甲同学认为实验ⅵ和ⅶ中,
 与
与 除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,
除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,(5)请举出一种水解反应在生产或生活中的应用:
您最近半年使用:0次
5 . “科学探究与创新意识”是化学学科核心素养之一、某研究小组用下图装置进行探究实验。下列说法正确的是
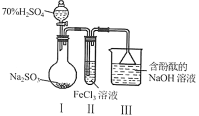
A.Ⅰ中70% 在反应中作氧化剂 在反应中作氧化剂 |
B.取少量反应后Ⅱ中溶液加入 溶液有蓝色沉淀生成 溶液有蓝色沉淀生成 |
C.Ⅱ中发生反应的离子方程式为: |
D.Ⅲ中溶液褪色,说明 具有漂白性 具有漂白性 |
您最近半年使用:0次
6 . 铁的单质及其化合物用途广泛,下列相关的离子方程式书写正确的是
A.用KSCN溶液检验 : : |
B.硫酸亚铁溶液中滴加双氧水: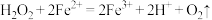 |
C.NaClO碱性条件下制备绿色消毒剂 : : |
D.用 溶液刻蚀Cu电路板: 溶液刻蚀Cu电路板: |
您最近半年使用:0次
7 . 工业废水处理是沙头角污水处理中心的重要业务。一种处理钢厂酸洗废水(含Fe3+、Fe2+、Al3+等)的工艺流程如下图所示:
回答下列问题:
(1)试剂1是___________ 。反应I的离子方程式为___________ 。
如何检验反应I后的溶液中是否含有Fe3+___________ 。
(2)加入少量氨水的目的是调节pH,操作时需控制pH值的范围为___________ 。
(3)“一系列操作”包括:蒸发浓缩,冷却结晶,___________ 。
(4)通入N2的目的是___________ 。
(5)制备Fe3O4纳米颗粒的离子方程式为___________ 。
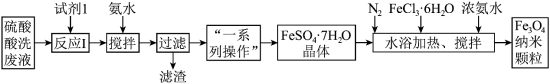
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(1)试剂1是
如何检验反应I后的溶液中是否含有Fe3+
(2)加入少量氨水的目的是调节pH,操作时需控制pH值的范围为
(3)“一系列操作”包括:蒸发浓缩,冷却结晶,
(4)通入N2的目的是
(5)制备Fe3O4纳米颗粒的离子方程式为
您最近半年使用:0次
8 . 已知A、B、C均为含铁化合物,请根据以下四种物质的转化过程回答相关问题:
Fe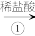 A
A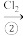 B
B C
C
(1)反应①、②、③中属于氧化还原反应的是 。
(2)关于B的溶液,说法正确的是 。
(3)选择合适的试剂也可以实现B转化为A,且考虑不能引入杂质,能实现该转化的方程式 。
Fe
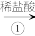 A
A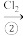 B
B C
C(1)反应①、②、③中属于氧化还原反应的是 。
| A.①② | B.①③ | C.②③ | D.①②③ |
| A.滴入几滴KSCN溶液后,可观察到溶液变血红色 |
| B.可与Fe反应,不能与Cu反应 |
| C.若加入NaOH溶液有红褐色沉淀生成 |
| D.Cl2 是氧化剂,可用双氧水替换 |
| A.2FeCl3+Fe=3FeCl2 | B.2FeCl3+Zn=2FeCl2+ZnCl2 |
| C.4Fe(OH)2+2H2O+O2=4Fe(OH)3 | D.2KI+2FeCl3=2KCl+2FeCl2+I2 |
您最近半年使用:0次
名校
9 . 下列实验方案不可行的是
| A.用碱石灰干燥氨气 | B.用蓝色石蕊试液检验酸性溶液 |
| C.通入Cl2除去FeCl3溶液中的FeCl2 | D.加入Fe粉除去Al3+溶液中的杂质Cu2+ |
您最近半年使用:0次
名校
解题方法
10 . 下列指定反应的离子方程式书写正确的是
A.过量SO2与“84”消毒液反应:ClO-+H2O+SO2=HSO +HClO +HClO |
| B.将SO2通入Ba(NO3)2溶液中:SO2+H2O+Ba2+=BaSO3↓+2H+ |
C.向稀硝酸中加入过量铁粉:Fe+NO +4H+=Fe3++NO↑+2H2O +4H+=Fe3++NO↑+2H2O |
D.用氨水吸收少量SO2:2NH3·H2O+SO2=2NH +SO +SO +H2O +H2O |
您最近半年使用:0次


 溶液刻蚀铜质电路板
溶液刻蚀铜质电路板
 可用于治疗胃酸过多
可用于治疗胃酸过多


