解题方法
1 . 氯化铁和氯化亚铁都是铁的重要化合物,下列说法错误的是
| A.饱和氯化铁溶液可制备氢氧化铁胶体 |
| B.氯化铁溶液可腐蚀覆铜板 |
| C.氯化亚铁可由化合反应制得 |
D.向5mL混有少量泥土的浑浊水中加入2mL饱和 溶液,静置5min,溶液变澄清 溶液,静置5min,溶液变澄清 |
您最近一年使用:0次
名校
解题方法
2 . 常温下,下列各组离子在指定溶液中能大量存在的是
A. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.滴入 溶液显红色的溶液中: 溶液显红色的溶液中: 、 、 、 、 、 、 |
C. 的溶液中: 的溶液中: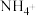 、 、 、 、 、 、 |
D. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
2024-03-07更新
|
144次组卷
|
2卷引用:广东省揭阳市惠来同仁北实高级中学2023-2024学年高三上学期期中考试化学试题
解题方法
3 . 下列各组离子在溶液中能大量共存的是
A.能使石蕊试液变红的溶液中: |
B. |
C.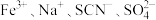 |
D.在常温下,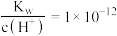 的溶液中: 的溶液中: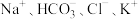 |
您最近一年使用:0次
名校
4 . 天然气是一种重要的化工原料和燃料,常含有少量H2S。一种在酸性介质中进行天然气脱硫的原理示意图如图所示。下列说法不正确的是

| A.脱硫过程中Fe2(SO4)3溶液的pH逐渐增大 |
| B.CH4是天然气脱硫过程的催化剂 |
| C.脱硫过程总反应方程式为:2H2S+O2=2S↓+2H2O |
| D.整个脱硫过程中参加反应的n(H2S):n(O2)=2:1 |
您最近一年使用:0次
2023-09-08更新
|
172次组卷
|
2卷引用:广东省揭阳市惠来县第一中学2022-2023学年高一下学期第二次月考化学试题
名校
解题方法
5 . 部分含铁物质及化合价关系如图所示,下列说法错误的是
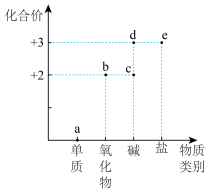

| A.工业上用热还原法冶炼a |
| B.b是黑色固体,在空气中加强热变为红色 |
| C.c可以通过化合反应生成d |
| D.e可以加快H2O2的分解 |
您最近一年使用:0次
2023-06-27更新
|
452次组卷
|
2卷引用:广东省揭阳市普宁市第二中学2020-2021学年高三下学期适应性考试(二)化学试题
6 . 下列实验的操作、现象、结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向NaBr溶液中滴入少量氯水和苯、振荡、静置 | 下层溶液呈橙红色 | 氧化性:Cl2>Br2 |
| B | 向某澄清溶液中滴加氯水,再滴加KSCN溶液 | 溶液变为血红色 | 该溶液中一定含Fe2+ |
| C | 加热装有氯化铵固体的试管,管口放有湿润的pH试纸 | 试纸变蓝 | 氯化铵分解产生氨气,氨气溶于水后溶液显碱性 |
| D | 向1mL0.1mol•L-1NaCl溶液里滴加少量AgNO3溶液产生白色沉淀,再滴加几滴0.1mol•L-1NaI溶液 | 白色沉淀转化为黄色沉淀 | KSP(AgCl)>KSP(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 工业上常用碳酸锰矿为主要原料来生产干电池的材料 ,为了去除碳酸锰矿中含有的少量金属离子(
,为了去除碳酸锰矿中含有的少量金属离子( 、
、 、
、 、
、 、
、 等)而获得
等)而获得 ,设计了如图所示的工艺流程:
,设计了如图所示的工艺流程:
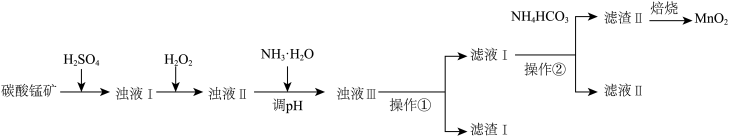
有关金属阳离子开始沉淀和沉淀完全的pH如下表:
回答下列问题:
(1)操作①和②的名称为___________ ,此操作需用到的玻璃仪器有___________ 。
(2)“滤渣I”中含有的物质是___________ 。
(3)加入 的作用为
的作用为___________ ,写出其发生反应的离子方程式:________ 。检验“浊液III”中是否含有 的方法:取少许浊液于试管中,静置;再取少许上层清液,滴入
的方法:取少许浊液于试管中,静置;再取少许上层清液,滴入_______ (填化学式)溶液,观察清液现象。
(4)写出加入 生成气体时发生反应的化学方程式:
生成气体时发生反应的化学方程式:___________ 。
(5)“滤液II”中可回收的物质为___________ (填化学式),其在农业上常用作___________ 。
 ,为了去除碳酸锰矿中含有的少量金属离子(
,为了去除碳酸锰矿中含有的少量金属离子( 、
、 、
、 、
、 、
、 等)而获得
等)而获得 ,设计了如图所示的工艺流程:
,设计了如图所示的工艺流程:
有关金属阳离子开始沉淀和沉淀完全的pH如下表:
| 金属阳离子 |  |  |  |  |  |  |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 8.0 | 8.3 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.8 | 9.8 |
(1)操作①和②的名称为
(2)“滤渣I”中含有的物质是
(3)加入
 的作用为
的作用为 的方法:取少许浊液于试管中,静置;再取少许上层清液,滴入
的方法:取少许浊液于试管中,静置;再取少许上层清液,滴入(4)写出加入
 生成气体时发生反应的化学方程式:
生成气体时发生反应的化学方程式:(5)“滤液II”中可回收的物质为
您最近一年使用:0次
8 . 铁是人体必需的微量元素之一,菠菜、黑木耳等食品中富含铁元素,其中菠菜中的铁元素至要以草酸亚铁 的形式存在,草酸亚铁粉末难溶于水。某小组设计实验检验和测定菠菜中的铁元素。
的形式存在,草酸亚铁粉末难溶于水。某小组设计实验检验和测定菠菜中的铁元素。
(1)草酸亚铁溶于稀硫酸的化学方程式是_______ 。
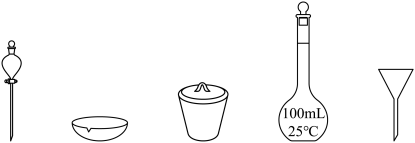
(2)菠菜的预处理

上述预处理流程中需要用到的仪器有烧杯、玻璃棒、酒精灯、_______ (从下图中选择,写出名称)。
(3)检验待测液中是否含有 、
、
(4)利用 标准溶液测定菠菜中铁元素的含量
标准溶液测定菠菜中铁元素的含量
步骤I:取10.00mL待测液于锥形瓶中,滴加 溶液至溶液显紫色。
溶液至溶液显紫色。
步骤II:向步骤I得到的混合液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
步骤III:向步骤II所得待测液中加入适量稀 溶液,用
溶液,用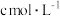 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液VmL。
溶液VmL。
①步骤I滴加 溶液的目的是
溶液的目的是_______ 。
②步骤III滴加 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为_______ 。
 的形式存在,草酸亚铁粉末难溶于水。某小组设计实验检验和测定菠菜中的铁元素。
的形式存在,草酸亚铁粉末难溶于水。某小组设计实验检验和测定菠菜中的铁元素。(1)草酸亚铁溶于稀硫酸的化学方程式是
(2)菠菜的预处理

上述预处理流程中需要用到的仪器有烧杯、玻璃棒、酒精灯、

(3)检验待测液中是否含有
 、
、
| 检验试剂 | 现象 | 结论 |
| ① | 溶液变为红色 | 滤液中含有 |
| ② | ③ | 滤液中含有 |
 标准溶液测定菠菜中铁元素的含量
标准溶液测定菠菜中铁元素的含量步骤I:取10.00mL待测液于锥形瓶中,滴加
 溶液至溶液显紫色。
溶液至溶液显紫色。步骤II:向步骤I得到的混合液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。
步骤III:向步骤II所得待测液中加入适量稀
 溶液,用
溶液,用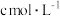 的
的 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 溶液VmL。
溶液VmL。①步骤I滴加
 溶液的目的是
溶液的目的是②步骤III滴加
 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为
您最近一年使用:0次
9 . 市场出售的某种麦片中含有微量、颗粒细小的还原铁粉,在人体胃酸(主要成分:盐酸)的作用下可发生反应进行补铁,实验室模拟胃酸与该麦片反应,下列操作可检验出反应生成补铁溶液的是
A.取样,加入少量 溶液 溶液 | B.取样,加入少量 溶液 溶液 |
| C.取样,加入少量KSCN溶液 | D.取样,加入少量 溶液 溶液 |
您最近一年使用:0次
10 . 下列依据相关实验得出的结论正确的是
| A.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
| B.向某黄色溶液中滴入几滴淀粉碘化钾溶液,溶液变蓝,则原溶液一定是氯水 |
C.某溶液中加硝酸银,出现白色沉淀,则该溶液中一定含有 |
D.某溶液中滴加KSCN溶液,溶液不变色,滴加氯水显红色,该溶液中一定含 |
您最近一年使用:0次
2023-06-07更新
|
69次组卷
|
2卷引用:广东省普宁市勤建学校2022-2023学年高一上学期期中考试化学试题



