名校
解题方法
1 . 还原铁粉与水蒸气的反应装置如图所示。取少量反应后的固体加入稀硫酸使其完全溶解得溶液a;另取少量反应后的固体加入稀硝酸使其完全溶解,得溶液b.下列说法正确的是
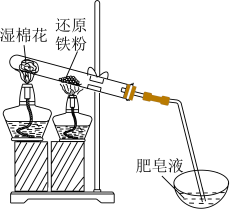
A.铁与水蒸气反应: |
B.肥皂液中产生气泡,不能证明铁与水蒸气反应生成 |
C.向溶液a中滴加 溶液,出现蓝色沉淀,说明铁粉未完全反应 溶液,出现蓝色沉淀,说明铁粉未完全反应 |
D.向溶液b中滴加 溶液,溶液变红,证实了固体中含有 溶液,溶液变红,证实了固体中含有 |
您最近半年使用:0次
今日更新
|
474次组卷
|
3卷引用:2024届河南省焦作市博爱县第一中学高三下学期三模化学试题
2024届河南省焦作市博爱县第一中学高三下学期三模化学试题北京市西城区2024届高三统一测试(一模)化学试题(已下线)题型6 元素及其化合物 化学实验基础(25题)-2024年高考化学常考点必杀300题(新高考通用)
2 . 下列实验对应的解释或结论正确的是
| 选项 | 实验 | 解释或结论 |
| A | 室温下,向含少量 的 的 溶液中加入铜屑,充分搅拌,过滤,得蓝色溶液 溶液中加入铜屑,充分搅拌,过滤,得蓝色溶液 | 杂质 被除去,得到纯净的 被除去,得到纯净的 溶液 溶液 |
| B |  晶体溶于稀硫酸,滴加 晶体溶于稀硫酸,滴加 溶液,溶液变红 溶液,溶液变红 |  晶体已变质 晶体已变质 |
| C | 向铅丹 中滴加浓盐酸,生成黄绿色气体 中滴加浓盐酸,生成黄绿色气体 | 氧化性: |
| D | 将铁的氧化物溶于过量稀盐酸中,再滴加几滴酸性 溶液,紫红色褪去 溶液,紫红色褪去 | 铁的氧化物含有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
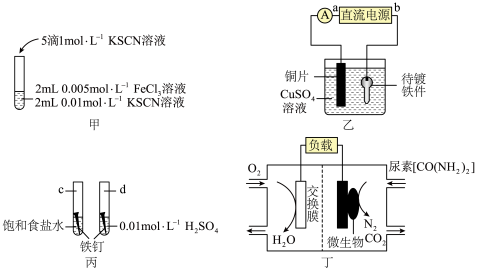
3 . 根据下列装置图,回答有关问题:___________ ,该反应为可逆反应,其离子方程式为___________ 。
(2)装置乙中,直流电源a为___________ 极(填“正”或“负”),阳极反应式为___________ 。
(3)装置丙中,d试管内铁钉除发生化学腐蚀外,还发生了___________ (填“析氢腐蚀”或“吸氧腐蚀”),其腐蚀速率比c试管中铁钉的腐蚀速率___________ (“快”“慢”或“相等”),c试管内正极的电极反应式为___________ 。
(4)装置丁中,从交换膜右侧向左侧迁移的离子是___________ ,负极的电极反应式为___________ 。
(2)装置乙中,直流电源a为
(3)装置丙中,d试管内铁钉除发生化学腐蚀外,还发生了
(4)装置丁中,从交换膜右侧向左侧迁移的离子是
您最近半年使用:0次
4 . 根据下列图示的操作及对应的现象,不能得出相应结论的是
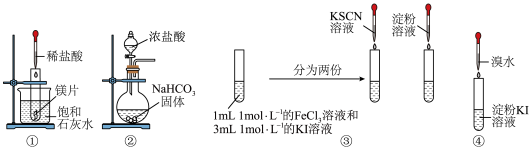
选项 | 操作 | 现象 | 结论 |
A | ① | 饱和石灰水变浑浊 | 镁与盐酸的反应是放热反应 |
B | ② | 硅酸钠溶液变浑浊 | 碳酸的酸性强于硅酸 |
C | ③ | 滴入KSCN溶液变红色,滴入淀粉溶液变蓝色 |  是可逆反应 是可逆反应 |
D | ④ | 淀粉KI溶液变蓝色 | 溴的得电子能力强于碘 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
5 . 根据实验操作及现象,下列结论中正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 用铂丝蘸取NaCl溶液,在酒精灯外焰上灼烧,火焰呈现黄色 | 灼烧过程中NaCl一定发生了化学变化 |
| B | 取少量某 溶液于试管中,滴入几滴KSCN溶液。溶液呈现红色 溶液于试管中,滴入几滴KSCN溶液。溶液呈现红色 | 该 溶液已经不含有 溶液已经不含有 |
| C | 在乙酸乙酯的制备实验中,将产生的蒸气导入足量的饱和碳酸钠溶液上方,充分反应后上层存在油状液体 | 该油状液体为乙酸乙酯 |
| D | 将一定量的铜片,加入试管中的某硝酸溶液中,可观察到有红棕色气体生成 | 所产生的气体中,只可能有 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
6 . 下列反应的离子方程式书写错误的是:
| A.用硫氰化钾溶液检验Fe3+:Fe3++3SCN-= Fe(SCN)3 |
| B.向海带灰浸出液中加入稀硫酸、双氧水:2I- + 2H+ + H2O2= I2 + 2H2O |
| C.磨口玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-= Na2SiO3+H2O |
D.NaHCO3溶液和少量Ba(OH)2溶液混合:2HCO +2OH-+Ba2+=H2O+BaCO3↓+CO +2OH-+Ba2+=H2O+BaCO3↓+CO |
您最近半年使用:0次
名校
解题方法
7 . 根据要求完成下列方程式。
(1)K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,其光解反应的化学方程式为:2K3[Fe(C2O4)3] 2FeC2O4 +3K2C2O4 +2CO2↑。
2FeC2O4 +3K2C2O4 +2CO2↑。
①草酸亚铁在隔绝空气的条件下加热会分解,可以制得黑色粉末状的氧化亚铁,写出该反应的化学方程式___________ 。
②氢氧化亚铁的制备过程中要注意隔绝空气,否则白色沉淀会迅速转化为灰绿色,最后得到红褐色物质,写出该转化过程的化学方程式___________ 。
③高铁酸钠是新型的净水剂,在强碱中氢氧化铁可以被氯气氧化生成紫色的高铁酸根,完成该反应的离子方程式___________ 。
(2)黄血盐(K4[Fe(CN)6] )是合法的食品添加剂,用作抗结剂;黄血盐在溶液中遇到Fe3+ ,生成普鲁士蓝沉淀。
①铊是一种剧毒化学品,若出现了中毒症状,应立即就医,在医学上,医生通常建议中毒者服用一种可溶性普鲁士蓝(KFe[Fe(CN)6])解毒,Tl+ 与K+ 性质接近,铊可置换普鲁士兰中的钾后,形成不溶性物质,随粪便排出,对治疗经口急慢性铊中毒有一定疗效,写出解铊毒反应的离子方程式___________ 。
②无水黄血盐可被浓硫酸分解,生成三种常见的盐和一种常见的无色无味气体,分析完成该反应的化学方程式___________ 。(提示:反应中价态不变)
(3)基于生成滕氏蓝的化学反应原理发展起来的晒制蓝图技术在复印机诞生之前广泛用于工程图纸的复制。赤血盐溶液遇到Fe2+ ,可以生成蓝色的滕氏蓝沉淀,写出得到滕氏蓝沉淀反应的离子方程式___________ 。(已知:氯气遇到黄血盐可以得到赤血盐)
(1)K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,其光解反应的化学方程式为:2K3[Fe(C2O4)3]
 2FeC2O4 +3K2C2O4 +2CO2↑。
2FeC2O4 +3K2C2O4 +2CO2↑。①草酸亚铁在隔绝空气的条件下加热会分解,可以制得黑色粉末状的氧化亚铁,写出该反应的化学方程式
②氢氧化亚铁的制备过程中要注意隔绝空气,否则白色沉淀会迅速转化为灰绿色,最后得到红褐色物质,写出该转化过程的化学方程式
③高铁酸钠是新型的净水剂,在强碱中氢氧化铁可以被氯气氧化生成紫色的高铁酸根,完成该反应的离子方程式
(2)黄血盐(K4[Fe(CN)6] )是合法的食品添加剂,用作抗结剂;黄血盐在溶液中遇到Fe3+ ,生成普鲁士蓝沉淀。
①铊是一种剧毒化学品,若出现了中毒症状,应立即就医,在医学上,医生通常建议中毒者服用一种可溶性普鲁士蓝(KFe[Fe(CN)6])解毒,Tl+ 与K+ 性质接近,铊可置换普鲁士兰中的钾后,形成不溶性物质,随粪便排出,对治疗经口急慢性铊中毒有一定疗效,写出解铊毒反应的离子方程式
②无水黄血盐可被浓硫酸分解,生成三种常见的盐和一种常见的无色无味气体,分析完成该反应的化学方程式
(3)基于生成滕氏蓝的化学反应原理发展起来的晒制蓝图技术在复印机诞生之前广泛用于工程图纸的复制。赤血盐溶液遇到Fe2+ ,可以生成蓝色的滕氏蓝沉淀,写出得到滕氏蓝沉淀反应的离子方程式
您最近半年使用:0次
8 . 下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 取某固体试样加入适量水,取少许于试管中,滴加NaOH溶液,并将湿润的红色石蕊试纸接近管口 | 湿润红色石蕊试纸无明显现象 | 该固体试样中一定不存在NH |
| B | 在橡胶塞侧面挖一个凹槽,嵌入下端卷成螺旋状的铜丝,向具支试管中加入2mL浓硝酸,用橡胶塞塞住试管口,使铜丝与硝酸接触,一段时间后,向上拉铜丝,终止反应 | 剧烈反应,铜丝表面放出红棕色的气泡,铜不断溶解,溶液变成绿色 | 浓硝酸具有强氧化性 |
| C | 取未知溶液于试管中,加入BaCl2溶液,有白色沉淀生成,再加足量稀盐酸 | 沉淀不溶解 | 溶液中一定含有SO |
| D | 向Fe(NO3)2溶液中滴加稀盐酸,再加入几滴KSCN溶液 | 溶液变为红色 | 稀盐酸可以将Fe2+氧化为Fe3+ |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
9 . 下列有关溶液中离子检验的说法正确的是
A.取样,加入硝酸酸化,再加入Ba(NO3)2溶液,若产生白色沉淀,则原溶液中存在 |
| B.取样,先加入少量氯水,再加入KSCN溶液,若溶液变红色,则原溶液中存在 Fe3+ |
| C.取样,加入硝酸酸化的AgNO3溶液:若无黄色沉淀,则原溶液中不存在I- |
| D.用洁净的铂丝蘸取溶液,在酒精灯外焰上灼烧,若火焰不呈紫色,则原溶液中不存在 K+ |
您最近半年使用:0次
2024-04-09更新
|
46次组卷
|
2卷引用:河南省周口市鹿邑县2023-2024学年高一下学期3月月考化学试题
解题方法
10 . 工业上用FeCl3溶液做印刷电路铜板的腐蚀液。化学小组设计如下流程对腐蚀废液(阳离子主要有H+、Fe3+、Fe2+和Cu2+)进行处理,实现FeCl3溶液再生并回收Cu。
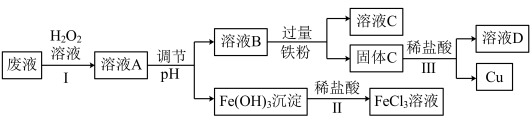
(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:_____________ ;
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为__________ ;
(3)步骤Ⅱ中发生反应的化学方程式为_____________ ;
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?_____________ ;
(5)固体C中的成分为________________ (填化学式);
(6)步骤Ⅲ中发生反应的离子方程式为___________ ,分离的操作名称为_______ 。

(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为
(3)步骤Ⅱ中发生反应的化学方程式为
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?
(5)固体C中的成分为
(6)步骤Ⅲ中发生反应的离子方程式为
您最近半年使用:0次



