1 . 根据下列图示的操作及对应的现象,不能得出相应结论的是
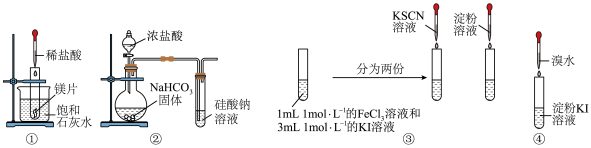
选项 | 操作 | 现象 | 结论 |
A | ① | 饱和石灰水变浑浊 | 镁与盐酸的反应是放热反应 |
B | ② | 硅酸钠溶液变浑浊 | 碳酸的酸性强于硅酸 |
C | ③ | 滴入KSCN溶液变红色,滴入淀粉溶液变蓝色 |  是可逆反应 是可逆反应 |
D | ④ | 淀粉KI溶液变蓝色 | 溴的得电子能力强于碘 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 写出一种Fe2+、Fe3+的检验办法:___________ 。
您最近一年使用:0次
3 . 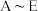 是中学常见的5种化合物,
是中学常见的5种化合物, 是氧化物,它们之间的转化关系如下图所示。则下列说法正确的是
是氧化物,它们之间的转化关系如下图所示。则下列说法正确的是
 是中学常见的5种化合物,
是中学常见的5种化合物, 是氧化物,它们之间的转化关系如下图所示。则下列说法正确的是
是氧化物,它们之间的转化关系如下图所示。则下列说法正确的是
A. 与 与 反应的化学方程式是: 反应的化学方程式是: |
B.检验 溶液中的金属阳离子的反应: 溶液中的金属阳离子的反应: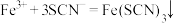 |
C.单质 在一定条件下能与水发生置换反应 在一定条件下能与水发生置换反应 |
| D.化合物C既能与酸反应,又能与碱反应,所以是两性化合物 |
您最近一年使用:0次
名校
4 . 向BaCl2溶液中通入SO2至饱和,此过程看不到现象,再向溶液中加入一种物质,溶液变浑浊,加入的这种物质不可能是
| A.FeCl3溶液 | B.AlCl3溶液 | C.Na2S溶液 | D.AgNO3溶液 |
您最近一年使用:0次
2024-02-19更新
|
310次组卷
|
2卷引用:河南省南阳市邓州市第六高级中学校2023-2024学年高二下学期开学测试化学试题
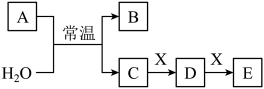
5 . 已知:A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。___________ 。
(2)若A为淡黄色粉末,X为非金属单质,通常为黑色粉末,则 与足量的
与足量的 充分反应时,转移电子总数为
充分反应时,转移电子总数为___________ ;若X为一种最常见的造成温室效应的气体。则鉴别等浓度的D、E两种溶液,可选择的试剂为___________ 。(填字母)
a. 溶液 b.氨水 c.澄清石灰水 d.
溶液 b.氨水 c.澄清石灰水 d. 溶液
溶液
(3)若A、B均为氮的常见氧化物,X是Fe,溶液D加入 溶液变红。
溶液变红。
①写出加热条件下C的浓溶液与X反应生成D的化学方程式___________ 。
②检验溶液D中还可能存在 的方法是
的方法是___________ 。
(2)若A为淡黄色粉末,X为非金属单质,通常为黑色粉末,则
 与足量的
与足量的 充分反应时,转移电子总数为
充分反应时,转移电子总数为a.
 溶液 b.氨水 c.澄清石灰水 d.
溶液 b.氨水 c.澄清石灰水 d. 溶液
溶液(3)若A、B均为氮的常见氧化物,X是Fe,溶液D加入
 溶液变红。
溶液变红。①写出加热条件下C的浓溶液与X反应生成D的化学方程式
②检验溶液D中还可能存在
 的方法是
的方法是
您最近一年使用:0次
2024-02-02更新
|
264次组卷
|
2卷引用:河南省南阳市2023-2024学年高一上学期1月期末化学试题
解题方法
6 . 在含有 和
和 的酸性溶液中,通入足量的
的酸性溶液中,通入足量的 后有白色沉淀生成,过滤后,向溶液中滴加
后有白色沉淀生成,过滤后,向溶液中滴加 溶液,无明显现象,下列说法正确的是
溶液,无明显现象,下列说法正确的是
 和
和 的酸性溶液中,通入足量的
的酸性溶液中,通入足量的 后有白色沉淀生成,过滤后,向溶液中滴加
后有白色沉淀生成,过滤后,向溶液中滴加 溶液,无明显现象,下列说法正确的是
溶液,无明显现象,下列说法正确的是A.白色沉淀是 和 和 | B.溶液的酸性减弱 |
C.白色沉淀是 | D. 全部被氧化为 全部被氧化为 |
您最近一年使用:0次
2024-02-02更新
|
259次组卷
|
3卷引用:河南省南阳市2023-2024学年高一上学期1月期末化学试题
名校
解题方法
7 . 利用“价—类”二维图研究物质的性质是一种有效的学习方法。铁及其部分化合物的“价—类”二维图如图所示。

(1)X、Y的化学式分别为___________ 、___________ 。
(2)图中只具有还原性的物质是___________ (填化学式)。
(3)类比推理是学习和研究化学物质及其变化的一种常用的思维方法。下列推理正确的是___________。
(4)某实验小组从亚铁盐的物质类别角度,预测其可能与某些金属、酸、碱、盐发生反应;从亚铁盐中铁元素的化合价,预测亚铁盐既具有氧化性,又具有还原性。请根据实验室提供的试剂完成下列实验。
实验室提供的试剂:锌片、铜片、 溶液、KSCN溶液、新制氯水、酸性高锰酸钾溶液、NaOH溶液。
溶液、KSCN溶液、新制氯水、酸性高锰酸钾溶液、NaOH溶液。
①探究 的氧化性:
的氧化性:
分别将铜片、锌片投入 溶液中,结果铜片没变化,锌片逐渐溶解。由此说明三种金属的还原性由强到弱的顺序为:
溶液中,结果铜片没变化,锌片逐渐溶解。由此说明三种金属的还原性由强到弱的顺序为:___________ 。
②探究亚铁盐与碱的反应;
向 溶液中滴加NaOH溶液,发现先生成白色沉淀,一段时间后沉淀基本变为红褐色,写出白色沉淀转化为红褐色沉淀的化学方程式:
溶液中滴加NaOH溶液,发现先生成白色沉淀,一段时间后沉淀基本变为红褐色,写出白色沉淀转化为红褐色沉淀的化学方程式:___________ 。
③探究 的还原性:
的还原性:
向 溶液滴加酸性高锰酸钾溶液,发生反应的离子方程式为:
溶液滴加酸性高锰酸钾溶液,发生反应的离子方程式为:___________ 。
(5)根据所提供的试剂,若要验证溶液中不含 而只含有
而只含有 ,正确的实验操作方法及现象是:
,正确的实验操作方法及现象是:___________ 。

(1)X、Y的化学式分别为
(2)图中只具有还原性的物质是
(3)类比推理是学习和研究化学物质及其变化的一种常用的思维方法。下列推理正确的是___________。
A.由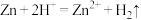 ,可推知 ,可推知 |
B.由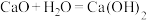 ,可推知 ,可推知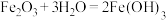 |
C.由 ,可推知 ,可推知 |
D.由 ,可推知 ,可推知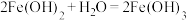 |
(4)某实验小组从亚铁盐的物质类别角度,预测其可能与某些金属、酸、碱、盐发生反应;从亚铁盐中铁元素的化合价,预测亚铁盐既具有氧化性,又具有还原性。请根据实验室提供的试剂完成下列实验。
实验室提供的试剂:锌片、铜片、
 溶液、KSCN溶液、新制氯水、酸性高锰酸钾溶液、NaOH溶液。
溶液、KSCN溶液、新制氯水、酸性高锰酸钾溶液、NaOH溶液。①探究
 的氧化性:
的氧化性:分别将铜片、锌片投入
 溶液中,结果铜片没变化,锌片逐渐溶解。由此说明三种金属的还原性由强到弱的顺序为:
溶液中,结果铜片没变化,锌片逐渐溶解。由此说明三种金属的还原性由强到弱的顺序为:②探究亚铁盐与碱的反应;
向
 溶液中滴加NaOH溶液,发现先生成白色沉淀,一段时间后沉淀基本变为红褐色,写出白色沉淀转化为红褐色沉淀的化学方程式:
溶液中滴加NaOH溶液,发现先生成白色沉淀,一段时间后沉淀基本变为红褐色,写出白色沉淀转化为红褐色沉淀的化学方程式:③探究
 的还原性:
的还原性:向
 溶液滴加酸性高锰酸钾溶液,发生反应的离子方程式为:
溶液滴加酸性高锰酸钾溶液,发生反应的离子方程式为:(5)根据所提供的试剂,若要验证溶液中不含
 而只含有
而只含有 ,正确的实验操作方法及现象是:
,正确的实验操作方法及现象是:
您最近一年使用:0次
名校
8 . 下列除杂方法正确的是
| 选项 | 混合物(括号中的物质为杂质) | 方法 |
| A | 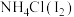 | 加热后冷却产生的气体 |
| B | 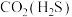 | 用酸性高锰酸钾溶液洗气 |
| C |  | 溶液( )通入氯气 )通入氯气 |
| D |  (水蒸气) (水蒸气) | 用 洗气 洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 物质的性质决定用途,下列物质的用途和性质不具有对应关系的是
| 选项 | 用途 | 性质 |
| A | 液氨用作制冷剂 | 液氨汽化吸收大量的热 |
| B |  用作供氧剂 用作供氧剂 |  与 与 或 或 反应生成 反应生成 |
| C |  溶液用于制作铜制电路板 溶液用于制作铜制电路板 |  溶液呈酸性 溶液呈酸性 |
| D |  用作葡萄酒的抗氧化剂 用作葡萄酒的抗氧化剂 |  具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 通过下列实验探究SO2与Fe3+的反应。将过量的SO2通入FeCl3溶液后,将溶液分为3份并进行以下实验:
实验1:第一份溶液中加入少量KMnO4溶液,溶液紫红色褪去
实验2:第二份溶液中滴加K3[Fe(CN)6]溶液,产生蓝色沉淀
实验3:第三份溶液中加入稀盐酸酸化的BaCl2溶液,产生白色沉淀
下列说法正确的是
实验1:第一份溶液中加入少量KMnO4溶液,溶液紫红色褪去
实验2:第二份溶液中滴加K3[Fe(CN)6]溶液,产生蓝色沉淀
实验3:第三份溶液中加入稀盐酸酸化的BaCl2溶液,产生白色沉淀
下列说法正确的是
| A.“实验1”中使KMnO4溶液褪色的一定是Fe2+ |
| B.“实验2”说明溶液中含有Fe2+,一定不含Fe3+ |
| C.“实验3”中产生的白色沉淀是BaSO3 |
D.SO2与Fe3+反应的离子方程式为2 +SO2+2H2O=2 +SO2+2H2O=2 + + +4H+ +4H+ |
您最近一年使用:0次



