名校
1 . 儿茶酸(Z)具有抗菌、抗氧化作用,常用于治疗烧伤、小儿肺炎等疾病,可采用如图所示路线合成。下列说法正确的是
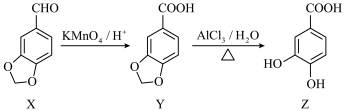
| A.X分子中所有原子可能共平面 | B.可用酸性 溶液鉴别X和Z 溶液鉴别X和Z |
| C.Y存在二元芳香酸的同分异构体 | D.Z与足量的溴水反应消耗3mol  |
您最近一年使用:0次
7日内更新
|
379次组卷
|
4卷引用:2024届河南省南阳市第一中学校高三下学期高考冲刺押题卷(二)理科综合试题-高中化学
2024届河南省南阳市第一中学校高三下学期高考冲刺押题卷(二)理科综合试题-高中化学广东省茂名市高州市2024届高三下学期高考适应性考试(三模)化学试题(已下线)山东省青岛市2023-2024学年高三下学期第三次模拟考试化学试题河北省衡水市部分示范性高中2024届高三下学期三模化学试题
名校
解题方法
2 . 锑白 是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为
是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为 ,含少量的
,含少量的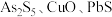 和
和 等)提取锑白的工艺流程如图所示:
等)提取锑白的工艺流程如图所示: ;
;
②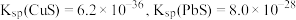 。
。
回答下列问题:
(1)“粉碎”辉锑矿的目的是___________ 。
(2)“滤渣Ⅰ”的主要成分除不溶性杂质外还有S、___________ (填化学式); 在“浸取”时发生反应的离子方程式为
在“浸取”时发生反应的离子方程式为___________ 。
(3)“除砷”时,反应中氧化剂与还原剂的物质的量之比为___________ (P转化为最高价态)。
(4)若浸取液中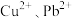 的浓度均为
的浓度均为 ,则c(S2-)≥
,则c(S2-)≥___________  才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时
才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时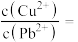
___________ 。
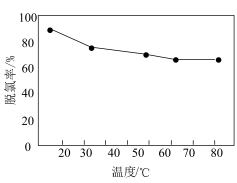
(5)“中和脱氯”时脱氯率与反应温度的关系如图所示:___________ 。
(6)锑可用于制备超亮光电极材料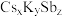 ,其晶胞结构如图所示,晶体a的化学式为
,其晶胞结构如图所示,晶体a的化学式为___________ ,晶体b中与 距离最近的
距离最近的 的个数为
的个数为___________ 。
 是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为
是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为 ,含少量的
,含少量的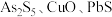 和
和 等)提取锑白的工艺流程如图所示:
等)提取锑白的工艺流程如图所示: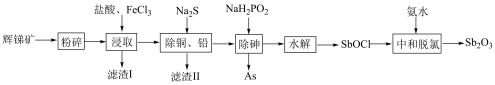
 ;
;②
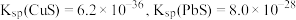 。
。回答下列问题:
(1)“粉碎”辉锑矿的目的是
(2)“滤渣Ⅰ”的主要成分除不溶性杂质外还有S、
 在“浸取”时发生反应的离子方程式为
在“浸取”时发生反应的离子方程式为(3)“除砷”时,反应中氧化剂与还原剂的物质的量之比为
(4)若浸取液中
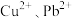 的浓度均为
的浓度均为 ,则c(S2-)≥
,则c(S2-)≥ 才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时
才能使二者完全沉淀(当离子浓度≤1×10-5mol/L时认为沉淀完全),此时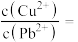
(5)“中和脱氯”时脱氯率与反应温度的关系如图所示:
(6)锑可用于制备超亮光电极材料
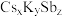 ,其晶胞结构如图所示,晶体a的化学式为
,其晶胞结构如图所示,晶体a的化学式为 距离最近的
距离最近的 的个数为
的个数为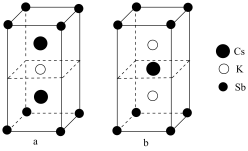
您最近一年使用:0次
名校
3 . 化合物M是一种功能高分子材料。实验室由A制备M的一种合成路线如图所示:
(1)A的结构简式为___________ (任写一种);B中所含手性碳的数目为___________ ;由C生成D时,C中碳原子的杂化方式是否改变:___________ (填“是”或“否”)。
(2)Q是E的同分异构体。同时满足下列条件的Q的结构有___________ 种(不考虑立体异构)。
i.含有2个酚羟基。
ii.核磁共振氢谱中有5组吸收峰。
(3)由G生成M的化学方程式为___________ 。
(4)根据化合物F的结构特征,分析预测其可能的化学性质,完成下表。
(5)参照上述合成路线和信息,以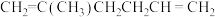 和甲醇为原料(其他试剂任选),分三步可合成化合物(
和甲醇为原料(其他试剂任选),分三步可合成化合物(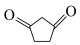 ),由此回答下列问题。
),由此回答下列问题。
①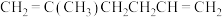 的化学名称为
的化学名称为___________ 。
②第二步反应生成的有机产物的结构简式为___________ 。
③第三步反应的化学方程式为___________ 。

已知:①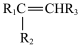
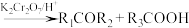 ;
;
②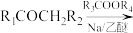
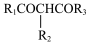 。
。
(1)A的结构简式为
(2)Q是E的同分异构体。同时满足下列条件的Q的结构有
i.含有2个酚羟基。
ii.核磁共振氢谱中有5组吸收峰。
(3)由G生成M的化学方程式为
(4)根据化合物F的结构特征,分析预测其可能的化学性质,完成下表。
| 序号 | 反应试剂、条件 | 有机产物的结构简式 | 反应类型 |
| a | 足量浓氢溴酸,加热 | ||
| b | 足量乙酸、浓硫酸,加热 |
(5)参照上述合成路线和信息,以
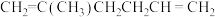 和甲醇为原料(其他试剂任选),分三步可合成化合物(
和甲醇为原料(其他试剂任选),分三步可合成化合物( ),由此回答下列问题。
),由此回答下列问题。①
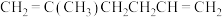 的化学名称为
的化学名称为②第二步反应生成的有机产物的结构简式为
③第三步反应的化学方程式为
您最近一年使用:0次
名校
解题方法
4 . 下列有关实验操作或试剂保存等的说法正确的是
| A.碱金属均可保存在煤油中 |
| B.碘化银固体保存在棕色细口瓶中 |
| C.实验室用石灰石和稀硫酸制备二氧化碳 |
D.用湿润的 试纸测定溶液的 试纸测定溶液的 不一定产生误差 不一定产生误差 |
您最近一年使用:0次
名校
5 . 常温下,用 的
的 溶液吸收
溶液吸收 中混有的
中混有的 ,所得溶液的
,所得溶液的 、溶液中
、溶液中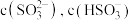 与混合气体体积(已折合为标准状况下体积)的关系如图所示(忽略溶液体积变化),已知
与混合气体体积(已折合为标准状况下体积)的关系如图所示(忽略溶液体积变化),已知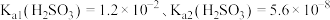 。下列说法正确的是
。下列说法正确的是
 的
的 溶液吸收
溶液吸收 中混有的
中混有的 ,所得溶液的
,所得溶液的 、溶液中
、溶液中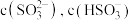 与混合气体体积(已折合为标准状况下体积)的关系如图所示(忽略溶液体积变化),已知
与混合气体体积(已折合为标准状况下体积)的关系如图所示(忽略溶液体积变化),已知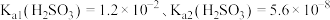 。下列说法正确的是
。下列说法正确的是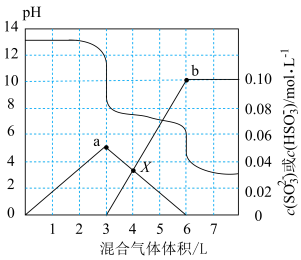
A.曲线a表示 与混合气体体积的关系 与混合气体体积的关系 |
| B.常温下,X点溶液显酸性 |
C.吸收过程中任意一点均存在: |
D.混合气体中 的体积分数约为75% 的体积分数约为75% |
您最近一年使用:0次
名校
6 .  是一种重要的工业化学品。某研究小组利用如图所示装置制备
是一种重要的工业化学品。某研究小组利用如图所示装置制备 ,并进行相关探究。
,并进行相关探究。
(1)装置A中发生反应的化学方程式为___________ 。
(2)装置B的作用为___________ ;干燥管中的试剂为___________ (任写一种)。
【查阅资料】Ⅰ.常温下镁和水反应现象不明显,镁和水反应会在镁条表面形成致密的 膜,阻碍反应进一步发生;
膜,阻碍反应进一步发生;
Ⅱ.镁与饱和 溶液剧烈反应产生大量气体和白色沉淀;
溶液剧烈反应产生大量气体和白色沉淀;
Ⅲ. 质地紧密,
质地紧密, 质地疏松,该实验条件下,
质地疏松,该实验条件下, 对
对 膜没有作用。
膜没有作用。
【预测】 溶液中的某种组分破坏了
溶液中的某种组分破坏了 与
与 反应生成的
反应生成的 膜。
膜。
【实验设计】用砂纸擦去镁条表面氧化膜,取表面积和质量相同的镁条(2cm)进行实验,测量产生气泡的速率。
(3)测得实验结果 ,得出结论:
,得出结论:___________ ;请结合必要的文字和化学用语解释得出该结论的原因为___________ 。
(4)另一同学经查阅资料发现 也能破坏
也能破坏 膜,于是进行如下探究:
膜,于是进行如下探究:
测得实验结果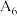
___________ 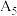 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(5)观察实验4和5发现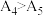 ,请解释其原因
,请解释其原因___________ 。
(6)加热 可以得到纯碱,写出纯碱在生产或生活中的一种应用:
可以得到纯碱,写出纯碱在生产或生活中的一种应用:___________ 。
 是一种重要的工业化学品。某研究小组利用如图所示装置制备
是一种重要的工业化学品。某研究小组利用如图所示装置制备 ,并进行相关探究。
,并进行相关探究。
(1)装置A中发生反应的化学方程式为
(2)装置B的作用为
【查阅资料】Ⅰ.常温下镁和水反应现象不明显,镁和水反应会在镁条表面形成致密的
 膜,阻碍反应进一步发生;
膜,阻碍反应进一步发生;Ⅱ.镁与饱和
 溶液剧烈反应产生大量气体和白色沉淀;
溶液剧烈反应产生大量气体和白色沉淀;Ⅲ.
 质地紧密,
质地紧密, 质地疏松,该实验条件下,
质地疏松,该实验条件下, 对
对 膜没有作用。
膜没有作用。【预测】
 溶液中的某种组分破坏了
溶液中的某种组分破坏了 与
与 反应生成的
反应生成的 膜。
膜。【实验设计】用砂纸擦去镁条表面氧化膜,取表面积和质量相同的镁条(2cm)进行实验,测量产生气泡的速率。
| 实验序号 | 实验装置 | 添加试剂及用量 | 产生气泡速率(mL/min) |
| 1 |
| 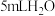 |  |
| 2 | 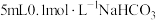 |  | |
| 3 | 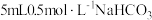 |  | |
| 4 | 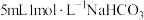 |  |
(3)测得实验结果
 ,得出结论:
,得出结论:(4)另一同学经查阅资料发现
 也能破坏
也能破坏 膜,于是进行如下探究:
膜,于是进行如下探究:| 实验序号 | 实验装置 | 添加试剂及用量 | 产生气泡速率(mL/min) |
| 5 |
| 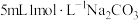 | 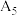 |
| 6 | 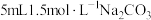 | 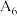 |
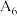
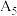 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(5)观察实验4和5发现
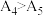 ,请解释其原因
,请解释其原因(6)加热
 可以得到纯碱,写出纯碱在生产或生活中的一种应用:
可以得到纯碱,写出纯碱在生产或生活中的一种应用:
您最近一年使用:0次
名校
解题方法
7 . X、Y、Z、W为原子半径依次增大的短周期p区元素,由四种元素形成的微粒Q可作为绿色催化剂和溶剂离子液体的阴离子,Q的结构如图所示,下列说法正确的是
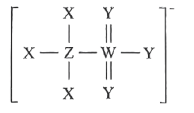
A.氢化物的沸点: |
B.电负性: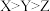 |
| C.W的氧化物对应的水化物属于强酸 |
| D.该阴离子中Y不满足8电子稳定结构 |
您最近一年使用:0次
名校
8 . 粗镍中含有 及少量
及少量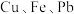 和
和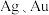 ,工业上,用如图所示的流动隔膜式电解槽精炼粗镍,以硫酸镍和少量氯化镍混合溶液作电解液,电解液中的
,工业上,用如图所示的流动隔膜式电解槽精炼粗镍,以硫酸镍和少量氯化镍混合溶液作电解液,电解液中的 能较有效地阻止电极钝化。已知:①实验条件下,
能较有效地阻止电极钝化。已知:①实验条件下,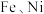 及少量
及少量 以离子形式进入极液;②金属性:
以离子形式进入极液;②金属性: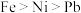 。下列说法正确的是
。下列说法正确的是
 及少量
及少量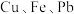 和
和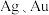 ,工业上,用如图所示的流动隔膜式电解槽精炼粗镍,以硫酸镍和少量氯化镍混合溶液作电解液,电解液中的
,工业上,用如图所示的流动隔膜式电解槽精炼粗镍,以硫酸镍和少量氯化镍混合溶液作电解液,电解液中的 能较有效地阻止电极钝化。已知:①实验条件下,
能较有效地阻止电极钝化。已知:①实验条件下,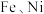 及少量
及少量 以离子形式进入极液;②金属性:
以离子形式进入极液;②金属性: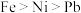 。下列说法正确的是
。下列说法正确的是
A.“净化”的目的主要是除去 |
| B.“隔膜”是阳离子交换膜,将两种极液隔开 |
| C.“粗镍”与电源正极相连,“纯镍”与电源负极相连 |
| D.电解相同时间,阴阳两极质量变化相等 |
您最近一年使用:0次
9 . 下列实验操作及现象不能得出相应实验结论的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向 溶液中通入与 溶液中通入与 等物质的量的 等物质的量的 ,再加入 ,再加入 ,振荡后静置,溶液分层,下层溶液变为红棕色 ,振荡后静置,溶液分层,下层溶液变为红棕色 | 还原性: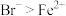 |
| B | 将 溶液和 溶液和 溶液混合,达到平衡后再滴加4滴 溶液混合,达到平衡后再滴加4滴 的 的 溶液,溶液红色变深 溶液,溶液红色变深 | 反应物浓度对化学平衡有影响 |
| C | 向滴有酚酞的 溶液中加入少量 溶液中加入少量 固体,溶液红色变浅并有白色沉淀生成 固体,溶液红色变浅并有白色沉淀生成 |  存在水解平衡 存在水解平衡 |
| D | 常温下,将 晶体研细后与 晶体研细后与 晶体置于烧杯中,快速搅拌混合物,并触摸杯壁,杯壁变冷,同时闻到刺激性气味 晶体置于烧杯中,快速搅拌混合物,并触摸杯壁,杯壁变冷,同时闻到刺激性气味 |  与 与 反应对应的 反应对应的 和 和 均大于0 均大于0 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式书写正确的是
| A.澄清的石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O |
| B.钠与水反应:Na+H2O=Na++OH-+H2↑ |
C.铜粉与浓硝酸反应:Cu+2H++NO =Cu2++NO2↑+H2O =Cu2++NO2↑+H2O |
| D.氢氧化铝中加入氢氧化钠溶液:Al(OH)3+OH-=[Al(OH)4]- |
您最近一年使用:0次
2024-05-09更新
|
172次组卷
|
2卷引用:河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题