名校
解题方法
1 . 下列离子方程式书写正确的是
| A.澄清的石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O |
| B.钠与水反应:Na+H2O=Na++OH-+H2↑ |
C.铜粉与浓硝酸反应:Cu+2H++NO =Cu2++NO2↑+H2O =Cu2++NO2↑+H2O |
| D.氢氧化铝中加入氢氧化钠溶液:Al(OH)3+OH-=[Al(OH)4]- |
您最近一年使用:0次
2024-05-09更新
|
181次组卷
|
2卷引用:河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题
名校
2 . 下列卤代烃中熔点最高的是
A. | B. | C.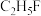 | D.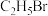 |
您最近一年使用:0次
2024-05-08更新
|
294次组卷
|
3卷引用:河南省南阳市六校联考2023-2024学年高二下学期4月期中考试化学试题
解题方法
3 . 已知:苯和卤代烃在催化剂作用下可生成烷基苯和卤化氢,例如:__________ ;G的结构简式为__________ 。
(2)在①~⑥反应中,步骤①的反应类型是__________ ,步骤③的反应类型是__________ 。
(3)写出B生成乙烯的化学方程式:__________ 。
(4)写出④的化学方程式:__________ 。
(5)写出⑥的化学方程式__________ 。
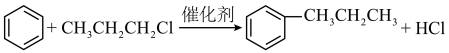

(2)在①~⑥反应中,步骤①的反应类型是
(3)写出B生成乙烯的化学方程式:
(4)写出④的化学方程式:
(5)写出⑥的化学方程式
您最近一年使用:0次
名校
解题方法
4 . 某校化学社团对铜与浓硫酸的反应进行相关研究。请回答下列问题:
(1)研究铜和浓硫酸反应的产物,实验装置如图所示。__________ 。
②铜与浓硫酸反应的化学方程式为__________ ,反应后试管中的溶液并未呈现蓝色而是几乎无色,请解释溶液不显蓝色的原因__________ 。
③若把氯气通入试管A、B、C、D中,其实验现象与上述现象不同的是__________ (选填A、B、C、D序号,气体颜色除外)。
(2)研究铜与浓硫酸反应时硫酸的最低浓度。甲组同学设计了方案一(实验装置如图一所示),乙组同学设计了方案二(实验装置如图二所示)。 能与
能与 结合生成红棕色沉淀,可用于检验溶液中微量的
结合生成红棕色沉淀,可用于检验溶液中微量的 。
。
①甲组同学的方案是:在图一圆底烧瓶中放入少量的铜片和 溶液,通过仪器M缓慢、逐滴地加入
溶液,通过仪器M缓慢、逐滴地加入 浓硫酸(记录滴加前后的读数,以确定所滴加浓硫酸的体积),至刚好出现红棕色沉淀时停止滴加浓硫酸,此时滴加浓硫酸的体积为b mL。计算反应所需硫酸的最低浓度为
浓硫酸(记录滴加前后的读数,以确定所滴加浓硫酸的体积),至刚好出现红棕色沉淀时停止滴加浓硫酸,此时滴加浓硫酸的体积为b mL。计算反应所需硫酸的最低浓度为__________  (
( 不发生副反应,假设混合溶液体积为两溶液的体积之和)。
不发生副反应,假设混合溶液体积为两溶液的体积之和)。
②乙组同学在图二的圆底烧瓶中放入足量铜粉和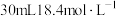 的浓硫酸,待反应结束,撤去酒精灯。打开a处的活塞,通入足量的空气,以确保生成的
的浓硫酸,待反应结束,撤去酒精灯。打开a处的活塞,通入足量的空气,以确保生成的 气体全部进入烧杯中完全被吸收。将烧杯取下,向其中加入足量盐酸酸化的双氧水(不考虑
气体全部进入烧杯中完全被吸收。将烧杯取下,向其中加入足量盐酸酸化的双氧水(不考虑 气体的逸出),再加入足量的
气体的逸出),再加入足量的 溶液,过滤、洗涤、干燥后称量沉淀的质量为
溶液,过滤、洗涤、干燥后称量沉淀的质量为 ,计算可得出该实验条件下能反应的硫酸浓度
,计算可得出该实验条件下能反应的硫酸浓度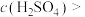
__________  (忽略反应中溶液的体积变化,保留1位小数),加入盐酸酸化的双氧水的目的是
(忽略反应中溶液的体积变化,保留1位小数),加入盐酸酸化的双氧水的目的是__________ (用离子方程式表示)。
(1)研究铜和浓硫酸反应的产物,实验装置如图所示。

②铜与浓硫酸反应的化学方程式为
③若把氯气通入试管A、B、C、D中,其实验现象与上述现象不同的是
(2)研究铜与浓硫酸反应时硫酸的最低浓度。甲组同学设计了方案一(实验装置如图一所示),乙组同学设计了方案二(实验装置如图二所示)。
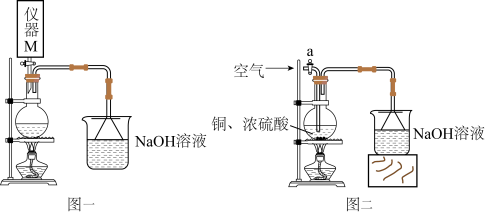
 能与
能与 结合生成红棕色沉淀,可用于检验溶液中微量的
结合生成红棕色沉淀,可用于检验溶液中微量的 。
。①甲组同学的方案是:在图一圆底烧瓶中放入少量的铜片和
 溶液,通过仪器M缓慢、逐滴地加入
溶液,通过仪器M缓慢、逐滴地加入 浓硫酸(记录滴加前后的读数,以确定所滴加浓硫酸的体积),至刚好出现红棕色沉淀时停止滴加浓硫酸,此时滴加浓硫酸的体积为b mL。计算反应所需硫酸的最低浓度为
浓硫酸(记录滴加前后的读数,以确定所滴加浓硫酸的体积),至刚好出现红棕色沉淀时停止滴加浓硫酸,此时滴加浓硫酸的体积为b mL。计算反应所需硫酸的最低浓度为 (
( 不发生副反应,假设混合溶液体积为两溶液的体积之和)。
不发生副反应,假设混合溶液体积为两溶液的体积之和)。②乙组同学在图二的圆底烧瓶中放入足量铜粉和
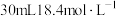 的浓硫酸,待反应结束,撤去酒精灯。打开a处的活塞,通入足量的空气,以确保生成的
的浓硫酸,待反应结束,撤去酒精灯。打开a处的活塞,通入足量的空气,以确保生成的 气体全部进入烧杯中完全被吸收。将烧杯取下,向其中加入足量盐酸酸化的双氧水(不考虑
气体全部进入烧杯中完全被吸收。将烧杯取下,向其中加入足量盐酸酸化的双氧水(不考虑 气体的逸出),再加入足量的
气体的逸出),再加入足量的 溶液,过滤、洗涤、干燥后称量沉淀的质量为
溶液,过滤、洗涤、干燥后称量沉淀的质量为 ,计算可得出该实验条件下能反应的硫酸浓度
,计算可得出该实验条件下能反应的硫酸浓度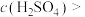
 (忽略反应中溶液的体积变化,保留1位小数),加入盐酸酸化的双氧水的目的是
(忽略反应中溶液的体积变化,保留1位小数),加入盐酸酸化的双氧水的目的是
您最近一年使用:0次
2024-05-03更新
|
95次组卷
|
3卷引用:河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题
名校
5 . 按要求回答下列问题
Ⅰ.利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:_______ ,Y为_______ 。(均填化学式)。
(2)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为_______ 。小登觉得可以设计实验验证这一推论,具体操作是_______ 。
Ⅱ.铝土矿的主要成分是 Al2O3和少量 Fe2O3、SiO2,是工业制备铝单质的原料。模拟铝土矿制备 Al2O3的工艺流程如下图所示。
(3)溶液 1 中的金属阳离子除Al3+外还包括_______ 。
(4)溶液 1 中加入过量NaOH 溶液的目的是_______ 。
(5)沉淀1的主要成分是_______ ,该成分可以和氢氟酸反应,请写出反应方程式_______ 。
(6)沉淀3转化为Al2O3的化学方程式为_______ 。
(7)将 1000 kg 含铝 13.5 %(质量分数)的铝土矿经过上述流程进行加工,最多可以生产_______ kg Al2O3固体。
Ⅰ.利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
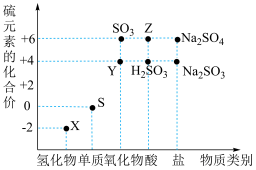
(2)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为
Ⅱ.铝土矿的主要成分是 Al2O3和少量 Fe2O3、SiO2,是工业制备铝单质的原料。模拟铝土矿制备 Al2O3的工艺流程如下图所示。
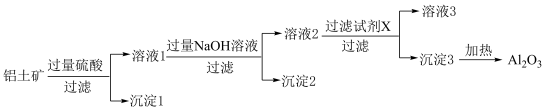
(3)溶液 1 中的金属阳离子除Al3+外还包括
(4)溶液 1 中加入过量NaOH 溶液的目的是
(5)沉淀1的主要成分是
(6)沉淀3转化为Al2O3的化学方程式为
(7)将 1000 kg 含铝 13.5 %(质量分数)的铝土矿经过上述流程进行加工,最多可以生产
您最近一年使用:0次
2024-05-03更新
|
195次组卷
|
2卷引用:河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
6 . 某些无机物的转化关系(部分反应物和生成物未列出)如图。已知化合物A为常见液体,气体E能使湿润的红色石蕊试纸变蓝。_____________ (填标号)。
a. b.
b.
(2)B、D在常温下难以发生反应,其主要原因为____________ 。
(3)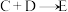 对人类的意义为
对人类的意义为_________________ (任写一点即可)。
(4)少量的E与氯气反应有白雾出现,写出该反应的化学方程式:______________ ;试推测过量的E与氯气反应的现象:_____________ 。
(5)用 溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:
溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:_________________ ,该反应中氧化产物与还原产物的物质的量之比为______________ 。
(6)常温常压下(气体摩尔体积为 ),将
),将 盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为
盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为______________  ,试管中所得溶液的物质的量浓度为
,试管中所得溶液的物质的量浓度为_____________  (用含
(用含 的代数式表示,假设溶质不向试管外扩散)。
的代数式表示,假设溶质不向试管外扩散)。
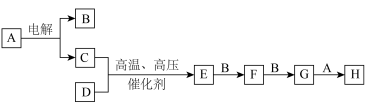
a.
 b.
b.
(2)B、D在常温下难以发生反应,其主要原因为
(3)
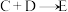 对人类的意义为
对人类的意义为(4)少量的E与氯气反应有白雾出现,写出该反应的化学方程式:
(5)用
 溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:
溶液可吸收F与G的混合气体,反应产物为水和一种钠盐,写出该反应的离子方程式:(6)常温常压下(气体摩尔体积为
 ),将
),将 盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为
盛满B、G混合气体(体积比为1:1)的试管倒立于水槽中,反应完全后,试管中剩余气体的体积为 ,试管中所得溶液的物质的量浓度为
,试管中所得溶液的物质的量浓度为 (用含
(用含 的代数式表示,假设溶质不向试管外扩散)。
的代数式表示,假设溶质不向试管外扩散)。
您最近一年使用:0次
2024-05-03更新
|
70次组卷
|
3卷引用:河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
7 . 硫元素的“价-类二维图”如图所示。下列有关叙述正确的是
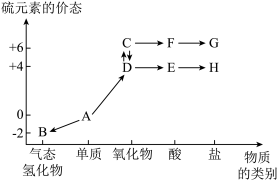
| A.硫元素的性质活泼,自然界中不存在物质A |
| B.气体D具有强还原性,不能用F的浓溶液干燥 |
| C.向H溶液中滴加G溶液并加热,可能生成气体D |
D.可用 溶液检验G中的阴离子 溶液检验G中的阴离子 |
您最近一年使用:0次
2024-05-03更新
|
210次组卷
|
3卷引用:河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题
名校
8 . 下列关于化学物质的用途或性质的叙述正确的说法有几个
①氨气极易溶于水,故可用做制冷剂
②单质硫易溶于 ,实验室可用
,实验室可用 清洗沾有硫单质的试管
清洗沾有硫单质的试管
③工业上用氢氟酸溶液腐蚀玻璃生产磨砂玻璃
④二氧化硅与氢氧化钠溶液、氢氟酸均反应,属两性氧化物
⑤足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化
⑥浓硫酸有强吸水性,可以干燥
⑦ 与
与 按
按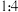 充满烧瓶,烧瓶倒置水中充分反应后,烧瓶内溶液的浓度接近
充满烧瓶,烧瓶倒置水中充分反应后,烧瓶内溶液的浓度接近
①氨气极易溶于水,故可用做制冷剂
②单质硫易溶于
 ,实验室可用
,实验室可用 清洗沾有硫单质的试管
清洗沾有硫单质的试管③工业上用氢氟酸溶液腐蚀玻璃生产磨砂玻璃
④二氧化硅与氢氧化钠溶液、氢氟酸均反应,属两性氧化物
⑤足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化

⑥浓硫酸有强吸水性,可以干燥

⑦
 与
与 按
按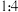 充满烧瓶,烧瓶倒置水中充分反应后,烧瓶内溶液的浓度接近
充满烧瓶,烧瓶倒置水中充分反应后,烧瓶内溶液的浓度接近
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次
2024-05-03更新
|
216次组卷
|
2卷引用:河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
9 . 某工厂拟综合处理含 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:下列说法正确的是
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:下列说法正确的是
 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:下列说法正确的是
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:下列说法正确的是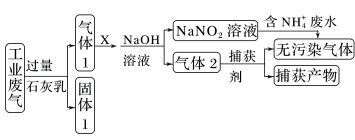
| A.固体1的主要成分为CaCO3、CaSO3 |
| B.X可以是空气,且需过量 |
| C.捕获剂所捕获的气体主要是CO |
D.处理含 废水时,发生的反应为 废水时,发生的反应为 +5NO +5NO +4H+=6NO↑+4H2O +4H+=6NO↑+4H2O |
您最近一年使用:0次
2024-04-27更新
|
111次组卷
|
3卷引用:河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
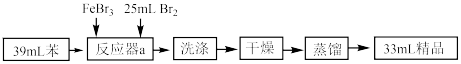
10 . 溴苯是一种重要的有机物,主要用于分析试剂和有机合成。实验室可以用苯、液溴为原料制备一定量的溴苯,制备过程及制备装置如图所示:
(1)虚线框中的仪器能明显提高原料的利用率,该仪器的名称是___________ ,仪器a最合适的容积是___________ (填字母)。
A. B.
B. C.
C. D.
D.
(2)仪器a中反应的化学方程式为___________ 。
(3)洗涤过程:水洗→ 溶液洗→水洗,第一次水洗的操作是
溶液洗→水洗,第一次水洗的操作是___________ ,进行分液。用 溶液洗涤的目的是
溶液洗涤的目的是___________ 。
(4)蒸馏时需要使用温度计。温度计的位置是___________ 。若该实验中溴足量,溴苯的产率为___________ %(结果保留三位有效数字)。

| 苯 | 溴 | 溴苯 | |
密度/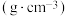 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
(1)虚线框中的仪器能明显提高原料的利用率,该仪器的名称是
A.
 B.
B. C.
C. D.
D.
(2)仪器a中反应的化学方程式为
(3)洗涤过程:水洗→
 溶液洗→水洗,第一次水洗的操作是
溶液洗→水洗,第一次水洗的操作是 溶液洗涤的目的是
溶液洗涤的目的是(4)蒸馏时需要使用温度计。温度计的位置是
您最近一年使用:0次



