1 . 不同价态硫元素之间有如图所示的转化关系:_______ ,A装置中发生反应的化学方程式为_______ 。
(2)装置B中的现象_______ ,检验SO2具有_______ 性,装置C的现象_______ ,检验SO2具有_______ 性。
(3)写出D装置中发生反应的离子方程式为_______ 。
(4)装置E作用是_______ 。
(5)下列有关硫及其化合物的叙述正确的是_______。
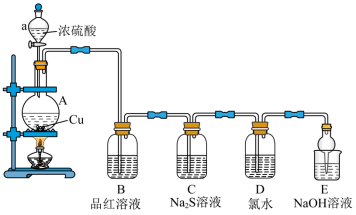
(2)装置B中的现象
(3)写出D装置中发生反应的离子方程式为
(4)装置E作用是
(5)下列有关硫及其化合物的叙述正确的是_______。
| A.硫在足量氧气中燃烧生成SO3 |
| B.向SO2水溶液中滴加Ba(NO3)2溶液,会生成BaSO4白色沉淀 |
| C.浓硫酸与蔗糖反应的实验仅体现了浓硫酸的脱水性 |
| D.除去SO2中含有的少量HCl气体,可以使气体通过饱和NaHSO3溶液 |
您最近一年使用:0次
名校
解题方法
2 . 研究化学能与热能、电能的转化具有重要价值。回答下列问题:
电能是现代社会中应用最广泛的二次能源。
(1)下列装置中能够实现化学能转化为电能的是_______(填字母)。
(2)(1)中的原电池装置中,正极反应方程是_______ 。
(3)若装置中转移了0.2mol电子,负极减少的质量是_______ 。
(4)有甲、乙两位同学均想利用原电池反应检测金属的活动性强弱,两人均使用镁片与铝片作电极,但甲同学将电极放入6mol•L-1的H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示:_______ 。
②乙中作负极材料是_______ ,总反应的离子方程式:_______ 。
③如果甲同学与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验得出的结论中,正确的是_______ (填标号)。
A.镁的金属性不一定比铝的金属性强
B.该实验说明金属活动性顺序表已过时,没有实用价值了
C.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质溶液
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析
(5)下列化学反应过程中的能量变化符合图示的是_______ (填序号)。
③金属钠与水反应 ④酒精燃烧
⑤灼热的碳与二氧化碳反应 ⑥ 与
与 反应
反应
(6)已知键能是表征化学键强度的物理量,可以用键断裂时所需的能量大小来衡量,键能越大,化学键越牢固,含有该键的分子越稳定。某些化学键的键能如下表所示( ):
):
①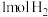 在
在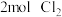 中燃烧,
中燃烧,_______ (填吸收或放出)的热量为_______  。
。
②表中所列化学键形成的单质分子中,最稳定的是_______ (填化学式)。
电能是现代社会中应用最广泛的二次能源。
(1)下列装置中能够实现化学能转化为电能的是_______(填字母)。
A.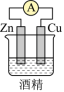 | B. | C.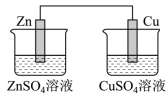 | D.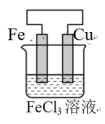 |
(3)若装置中转移了0.2mol电子,负极减少的质量是
(4)有甲、乙两位同学均想利用原电池反应检测金属的活动性强弱,两人均使用镁片与铝片作电极,但甲同学将电极放入6mol•L-1的H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示:
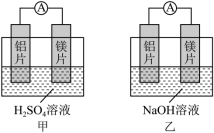
②乙中作负极材料是
③如果甲同学与乙同学均认为“构成原电池的电极材料都是金属时,则构成负极材料的金属应比构成正极材料的金属活泼”,由此他们会得出不同的实验结论,依据该实验得出的结论中,正确的是
A.镁的金属性不一定比铝的金属性强
B.该实验说明金属活动性顺序表已过时,没有实用价值了
C.利用原电池反应判断金属活动性顺序时应注意选择合适的电解质溶液
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此具体问题应具体分析
(5)下列化学反应过程中的能量变化符合图示的是
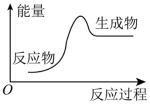
③金属钠与水反应 ④酒精燃烧
⑤灼热的碳与二氧化碳反应 ⑥
 与
与 反应
反应(6)已知键能是表征化学键强度的物理量,可以用键断裂时所需的能量大小来衡量,键能越大,化学键越牢固,含有该键的分子越稳定。某些化学键的键能如下表所示(
 ):
):| 共价键 |  |  |  |
| 键能 | 247 | 431 | 436 |
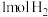 在
在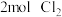 中燃烧,
中燃烧, 。
。②表中所列化学键形成的单质分子中,最稳定的是
您最近一年使用:0次
名校
3 . 钡和铊均在周期表中位于第六周期,铊与铝是同族元素,元素符号是Tl;钡与镁是同族元素,以下对钡和铊的性质的说法错误的是
| A.单质钡和铊是易导电的金属 | B. 是两性氢氧化物 是两性氢氧化物 |
| C.重金属铊盐具有极强的毒性 | D.单质钡能与水常温下反应生成氢气 |
您最近一年使用:0次
名校
解题方法
4 . 下列化学反应对应的离子方程式表示正确的是
A.氢氟酸与 反应: 反应: |
B.向氯化铝溶液中滴入过量的氨水: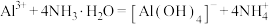 |
C.向 溶液中通入过量 溶液中通入过量 : :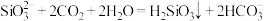 |
D.铁丝插入CuSO4溶液中: |
您最近一年使用:0次
名校
解题方法
5 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温常压下,18g重水( )中所含的中子数为 )中所含的中子数为 |
B.标准状况下,14g氮气含有的核外电子数为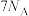 |
C.标准状况下,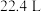 的 的 和 和 组成的混合气体中,含氧原子数为 组成的混合气体中,含氧原子数为 |
D.1mol 与足量 与足量 充分反应,生成的 充分反应,生成的 分子数为 分子数为 |
您最近一年使用:0次
名校
解题方法
6 . 正确掌握化学用语是学好化学的基础,下列有关化学用语表述正确的是
A.质子数为18、中子数为22的氩原子: | B.次氯酸的电子式: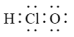 |
C. 的结构示意图: 的结构示意图: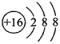 | D.58.5g NaCl晶体含有 个NaCl分子 个NaCl分子 |
您最近一年使用:0次
7 . 2024年3月5日,习近平总书记在全国两会期间强调:“面对新一轮科技革命和产业变革,我们必须抢抓机遇,加大创新力度,培育壮大新兴产业,超前布局建设未来产业,完善现代化产业体系。”下列说法正确的是
A.“华龙一号”核电海外投产,其反应堆所用铀棒中含有的经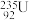 与 与 互为同素异形体 互为同素异形体 |
| B.“天机芯”是全球首款异构融合类脑计算芯片,芯片的主要成分为二氧化硅 |
| C.“天和”核心舱用的碳化硅陶瓷属于传统无机非金属材料 |
D.“北斗卫星”授时系统的“星载铷钟”含铷元素,其单质遇水能剧烈反应放出 |
您最近一年使用:0次
名校
解题方法
8 . 下列图示与对应的叙述相符的是
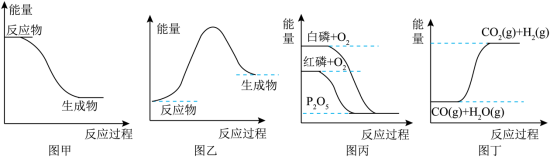
| A.图甲代表浓H2SO4稀释过程中体系的能量变化 |
| B.图乙表示反应物断键吸收的能量小于生成物成键放出的能量 |
| C.图丙表示白磷比红磷稳定 |
| D.图丁表示CO与H2O的反应是吸热反应 |
您最近一年使用:0次
2024-05-22更新
|
456次组卷
|
2卷引用:青海省西宁市第十四中学2023-2024学年高一下学期期中考试化学试卷
9 . 下列关于反应
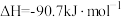 正确的是
正确的是

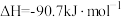 正确的是
正确的是| A.平衡时升高温度,v(正)减小,v(逆)增大 |
| B.使用催化剂能提高平衡时 CH3OH 的产率 |
C.反应的平衡常数可表示为 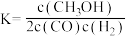 |
| D.平衡时增大 CO 的浓度,v(正)瞬间增大,v(逆)瞬间不变 |
您最近一年使用:0次
10 . 2L 恒容密闭容器内,800℃时反应: 体系中
体系中
(1)写出该反应的平衡常数表达式:K=___________ 。
(2)若在某时刻计算出的浓度商 Q 数值大于平衡常数K,则该反应___________ (向正反应方向移动、向逆反应方向移动、达到平衡状态)。
(3)已知 K300°C > K350°C ,则该反应是___________ 热反应。
(4)能说明该反应已达到平衡状态的是 ___________。
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的措施是___________ 。
(6)保持其他条件不变,仅充入氦气,NO2转化率将___________ (填“变大”、“变小”或“不变”)。
(7)对于可逆反应: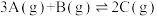
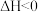 ,下列各图正确的是___________。
,下列各图正确的是___________。
 体系中
体系中(1)写出该反应的平衡常数表达式:K=
(2)若在某时刻计算出的浓度商 Q 数值大于平衡常数K,则该反应
(3)已知 K300°C > K350°C ,则该反应是
(4)能说明该反应已达到平衡状态的是 ___________。
| A.v(NO2)=2v(O2) | B.容器内压强保持不变 |
| C.v逆(NO)=2v正(O2) | D.容器内密度保持不变 |
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的措施是
(6)保持其他条件不变,仅充入氦气,NO2转化率将
(7)对于可逆反应:
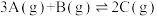
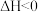 ,下列各图正确的是___________。
,下列各图正确的是___________。A.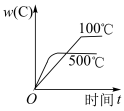 | B.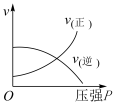 | C.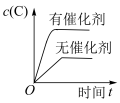 | D.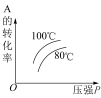 |
您最近一年使用:0次



