名校
1 . 研究硫及其化合物的应用价值对于社会发展意义重大。请回答以下问题:
(1)欲制备 ,从氧化还原角度分析,下列方法合理的是___________(选填字母序号)。
,从氧化还原角度分析,下列方法合理的是___________(选填字母序号)。
(2)用下图所示装置制备纯净的 (同时生成一种正盐),请写出发生装置中反应的化学方程式为
(同时生成一种正盐),请写出发生装置中反应的化学方程式为___________ ,碱石灰的主要作用为___________ 。 的一种途径是:
的一种途径是: 。
。
①写出少量SO2通入氨水发生的离子方程式___________ 。
②某实验小组为测定步骤2溶液中 的氧化率α,设计了以下实验方案。[提示:氧化率
的氧化率α,设计了以下实验方案。[提示:氧化率 ]
]
方案:一定条件下向100 mL 1 mol·L 的
的 溶液中通入空气后,先加入足量的稀盐酸,充分反应后,再加入足量
溶液中通入空气后,先加入足量的稀盐酸,充分反应后,再加入足量 溶液,过滤、洗涤、烘干,得到沉淀18.64g。
溶液,过滤、洗涤、烘干,得到沉淀18.64g。
计算 的氧化率
的氧化率
___________ (用百分数表示)。
(1)欲制备
 ,从氧化还原角度分析,下列方法合理的是___________(选填字母序号)。
,从氧化还原角度分析,下列方法合理的是___________(选填字母序号)。A. | B. | C. | D.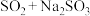 |
(2)用下图所示装置制备纯净的
 (同时生成一种正盐),请写出发生装置中反应的化学方程式为
(同时生成一种正盐),请写出发生装置中反应的化学方程式为
 的一种途径是:
的一种途径是: 。
。①写出少量SO2通入氨水发生的离子方程式
②某实验小组为测定步骤2溶液中
 的氧化率α,设计了以下实验方案。[提示:氧化率
的氧化率α,设计了以下实验方案。[提示:氧化率 ]
]方案:一定条件下向100 mL 1 mol·L
 的
的 溶液中通入空气后,先加入足量的稀盐酸,充分反应后,再加入足量
溶液中通入空气后,先加入足量的稀盐酸,充分反应后,再加入足量 溶液,过滤、洗涤、烘干,得到沉淀18.64g。
溶液,过滤、洗涤、烘干,得到沉淀18.64g。计算
 的氧化率
的氧化率
您最近一年使用:0次
名校
解题方法
2 . 按要求回答下列问题:
(1)下列变化中属于吸热反应的是___________ (填序号)。
①铝片与稀盐酸的反应;②将胆矾加热变为白色粉末;③干冰汽化;④甲烷在氧气中的燃烧反应;⑤ 固体溶于水;⑥C与
固体溶于水;⑥C与 反应生成CO
反应生成CO
(2)镁、海水、溶解氧可构成原电池,为水下小功率设备长时间供电,结构示意图如图所示,其总反应为: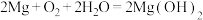 。下列说法正确的是
。下列说法正确的是___________ (填字母序号)。
b. 发生氧化反应
发生氧化反应
c.海水溶液中阴离子移向Mg极
d.电池工作时,电子转移方向:石墨→海水→Mg
(3)下图是一氧化碳和氧在钌催化剂表面形成化学键的过程。下列说法正确的是___________。
(4)合成氨工业中,合成塔中每产生2 mol ,放出92.2 kJ热量,已知断开1 mol
,放出92.2 kJ热量,已知断开1 mol 键、1 mol
键、1 mol 键分别需要吸收的能量为436 kJ、945.8 kJ;则1 mol
键分别需要吸收的能量为436 kJ、945.8 kJ;则1 mol  键断裂吸收的能量约等于
键断裂吸收的能量约等于___________ kJ。
(5)若将两个金属棒用导线相连在一起,总质量为80.00g的镁片和铝片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为74g,则装置工作时负极电极反应式为___________ ,工作时间内装置所产生氢气的体积为___________ L(标准状况)。
(1)下列变化中属于吸热反应的是
①铝片与稀盐酸的反应;②将胆矾加热变为白色粉末;③干冰汽化;④甲烷在氧气中的燃烧反应;⑤
 固体溶于水;⑥C与
固体溶于水;⑥C与 反应生成CO
反应生成CO(2)镁、海水、溶解氧可构成原电池,为水下小功率设备长时间供电,结构示意图如图所示,其总反应为:
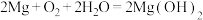 。下列说法正确的是
。下列说法正确的是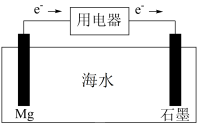
b.
 发生氧化反应
发生氧化反应c.海水溶液中阴离子移向Mg极
d.电池工作时,电子转移方向:石墨→海水→Mg
(3)下图是一氧化碳和氧在钌催化剂表面形成化学键的过程。下列说法正确的是___________。
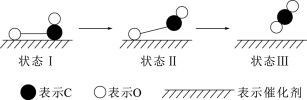
A. 和CO均为酸性氧化物 和CO均为酸性氧化物 | B.该过程中,CO先断键成C和O |
C.状态 到状态 到状态 为放热过程 为放热过程 | D.图示表示CO和 反应生成 反应生成 的过程 的过程 |
(4)合成氨工业中,合成塔中每产生2 mol
 ,放出92.2 kJ热量,已知断开1 mol
,放出92.2 kJ热量,已知断开1 mol 键、1 mol
键、1 mol 键分别需要吸收的能量为436 kJ、945.8 kJ;则1 mol
键分别需要吸收的能量为436 kJ、945.8 kJ;则1 mol  键断裂吸收的能量约等于
键断裂吸收的能量约等于(5)若将两个金属棒用导线相连在一起,总质量为80.00g的镁片和铝片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为74g,则装置工作时负极电极反应式为
您最近一年使用:0次
3 . 下列过程都与热量变化有关,其中表述正确的是
| A.一定条件下,石墨转化为金刚石要吸热,说明金刚石更稳定 |
| B.能量变化必然伴随发生化学变化 |
| C.化学反应中的能量变化与反应物的质量无关 |
D.已知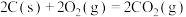 ; ; 等量碳完全燃烧释放的热量更多 等量碳完全燃烧释放的热量更多 |
您最近一年使用:0次
名校
解题方法
4 . 下列说法正确的是
A.制取粗硅时生成的气体产物为 |
B.工业上煅烧黄铁矿( )生产 )生产 |
C. 是具有漂白作用,可使石蕊褪色 是具有漂白作用,可使石蕊褪色 |
D.要除去粗盐中可溶性杂质离子 、 、 、 、 加入试剂的顺序可为NaOH溶液、 加入试剂的顺序可为NaOH溶液、 溶液、 溶液、 溶液、盐酸 溶液、盐酸 |
您最近一年使用:0次
名校
解题方法
5 . 化学与生活息息相关,下列说法错误的是
| A.工业生产玻璃和水泥,均需用石灰石作原料 |
| B.波尔多液是用胆矾和石灰乳混合制成的一种常见的农药 |
| C.华为“麒麟980”芯片的主要成分是二氧化硅 |
| D.酸雨主要是氮、硫的氧化物大量排放引起的 |
您最近一年使用:0次
6 . 用镍铂合金废料(主要成分为Ni、Pt,含少量Al、Co、CaO、 )回收镍和铂,其工艺流程如图:
)回收镍和铂,其工艺流程如图:____________________ 。
(2)用王水浸取“含Pt滤渣”可回收Pt,浸取时有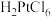 和NO生成,写出该反应的化学方程式
和NO生成,写出该反应的化学方程式______________________ 。
(3)在常温下,若酸浸后溶液中各离子浓度均为0.1mol/L且“滤渣1”为 ,则“除钴”步骤需要控制溶液的pH范围是
,则“除钴”步骤需要控制溶液的pH范围是___________ 。已知: ,
,
 ,
, ,
, ,
, 。
。
(4)加NaOH调pH的目的是除去溶液中的 ,但过程中pH不宜过高原因是
,但过程中pH不宜过高原因是____________________ 。
(5)“控温氧化”时控制其他条件一定, 的产率与温度和时间有关。20℃、40℃时反应后所得滤液主要为NaCl、NaOH和
的产率与温度和时间有关。20℃、40℃时反应后所得滤液主要为NaCl、NaOH和 ,60℃时反应后所得滤液主要为NaCl、
,60℃时反应后所得滤液主要为NaCl、 、NaOH和
、NaOH和 。反应相同时间,60℃时
。反应相同时间,60℃时 的产率低于40℃时,原因可能为
的产率低于40℃时,原因可能为__________________ 。
 )回收镍和铂,其工艺流程如图:
)回收镍和铂,其工艺流程如图:
(2)用王水浸取“含Pt滤渣”可回收Pt,浸取时有
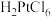 和NO生成,写出该反应的化学方程式
和NO生成,写出该反应的化学方程式(3)在常温下,若酸浸后溶液中各离子浓度均为0.1mol/L且“滤渣1”为
 ,则“除钴”步骤需要控制溶液的pH范围是
,则“除钴”步骤需要控制溶液的pH范围是 ,
,
 ,
, ,
, ,
, 。
。(4)加NaOH调pH的目的是除去溶液中的
 ,但过程中pH不宜过高原因是
,但过程中pH不宜过高原因是(5)“控温氧化”时控制其他条件一定,
 的产率与温度和时间有关。20℃、40℃时反应后所得滤液主要为NaCl、NaOH和
的产率与温度和时间有关。20℃、40℃时反应后所得滤液主要为NaCl、NaOH和 ,60℃时反应后所得滤液主要为NaCl、
,60℃时反应后所得滤液主要为NaCl、 、NaOH和
、NaOH和 。反应相同时间,60℃时
。反应相同时间,60℃时 的产率低于40℃时,原因可能为
的产率低于40℃时,原因可能为
您最近一年使用:0次
7 . 已知A、B、C、D、E、F、G、H可以发生如图所示的转化关系,反应中部分生成物已略去。其中,A、G为同一主族元素形成的单质,G常用来制作半导体材料。B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物。(部分生成物未表示出来)___________ 。
(2)写出E与氢氧化钠溶液反应的离子方程式为___________ 。
(3)反应③的化学方程式是___________ 。

(2)写出E与氢氧化钠溶液反应的离子方程式为
(3)反应③的化学方程式是
您最近一年使用:0次
8 . 草酸是一种用途广泛的二元有机中强酸,某同学通过查阅资料设计了如图所示的装置(夹持仪器省略)制备一定量的草酸晶体( ),回答下列问题:
),回答下列问题: 的溶解度数据如上表
的溶解度数据如上表
(1)仪器A右侧玻璃导管的作用为_________ ,仪器A中使用饱和食盐水代替蒸馏水的目的是________________ 。
(2)装置乙的作用是除杂,写出 被除去的离子方程式
被除去的离子方程式_________________ 。
(3)在装置丙中已加入催化剂,请写出生成 的化学方程式
的化学方程式______________ ,研究表明当硝酸的质量分数超过50%或温度高于50℃,草酸的产率开始下降,其原因是________________________ 。
(4)装置丁的作用是_________________ 。
(5)待反应结束后,从装置丙中分离出 晶体的操作为
晶体的操作为_____________ 、__________ 、过滤、洗涤、低温干燥。
 ),回答下列问题:
),回答下列问题:
 的溶解度数据如上表
的溶解度数据如上表温度/℃ | 20 | 40 | 60 | 80 |
溶解度/g | 9.52 | 21.5 | 44.3 | 84.5 |
(1)仪器A右侧玻璃导管的作用为
(2)装置乙的作用是除杂,写出
 被除去的离子方程式
被除去的离子方程式(3)在装置丙中已加入催化剂,请写出生成
 的化学方程式
的化学方程式(4)装置丁的作用是
(5)待反应结束后,从装置丙中分离出
 晶体的操作为
晶体的操作为
您最近一年使用:0次
名校
9 . 由重晶石矿(主要成分是 ,含
,含 等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
 ,含
,含 等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是
等杂质)可制得氯化钡晶体,在实验室中某兴趣小组按下列流程制取氯化钡晶体,下列说法正确的是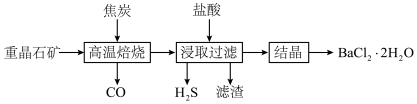
| A.“高温焙烧”前将原料研磨处理,能加快“高温焙烧”的反应速率 |
B.“高温焙烧”时只有 被C还原 被C还原 |
| C.“浸取过滤”发生的主要反应是氧化还原反应 |
| D.“高温焙烧”和“结晶”两处操作均需用到蒸发皿 |
您最近一年使用:0次
名校
解题方法
10 . 常温下,向20mL 0.1 的HA溶液中逐滴加入0.1
的HA溶液中逐滴加入0.1 的烧碱溶液,溶液中水所电离的
的烧碱溶液,溶液中水所电离的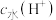 随加入烧碱溶液体积的变化如图所示,下列说法正确的是
随加入烧碱溶液体积的变化如图所示,下列说法正确的是
 的HA溶液中逐滴加入0.1
的HA溶液中逐滴加入0.1 的烧碱溶液,溶液中水所电离的
的烧碱溶液,溶液中水所电离的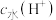 随加入烧碱溶液体积的变化如图所示,下列说法正确的是
随加入烧碱溶液体积的变化如图所示,下列说法正确的是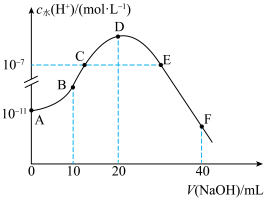
A.由图可知 的水解平衡常数 的水解平衡常数 约为 约为 |
| B.C. E两点因为对水的电离的抑制作用和促进作用相同,所以溶液均呈中性 |
C.B点的溶液中离子浓度之间存在: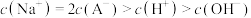 |
D.F点的溶液呈碱性,粒子浓度之间存在: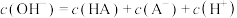 |
您最近一年使用:0次



