名校
1 . 某化学小组模拟工业生产制取HNO3设计如图所示装置,其中a为一个可持续鼓入空气的橡皮球。请回答下列问题。___________ (填“吸热”或“放热”)反应。
(2)控制氨气和氧气的比例是制备硝酸的关键。欲使氨气尽可能的都转化为硝酸,从理论上看
n(NH3):n(O2)的最佳比例为___________ ,按最佳比例时装置E中主要反应的化学方程式 ___________ 。
(3)装置C中浓H2SO4的作用是___________ ,若撤掉C装置,当NH3与O2比例不合适时,D中不仅有红棕色气体产生,还伴有白烟,白烟的化学式是___________ 。
(4)F中处理尾气的方法可以是___________ 。
(5)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置省略未画)进行验证。实验步骤如下:
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是___________ ,由此,该同学得出结论:不能用CaCl2代替碱石灰。
(6)该小组拟利用所得HNO3制取Cu(NO3)2,假设他们直接用铜屑与稀硝酸反应来制取硝酸铜:
①铜屑与稀硝酸反应的化学反应方程式为___________ ;
②此法的两个缺点是___________ 、___________ 。经讨论,小组决定先把铜粉放在空气中灼烧,再与稀硝酸反应制取硝酸铜。

(2)控制氨气和氧气的比例是制备硝酸的关键。欲使氨气尽可能的都转化为硝酸,从理论上看
n(NH3):n(O2)的最佳比例为
(3)装置C中浓H2SO4的作用是
(4)F中处理尾气的方法可以是
(5)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置省略未画)进行验证。实验步骤如下:

②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是
(6)该小组拟利用所得HNO3制取Cu(NO3)2,假设他们直接用铜屑与稀硝酸反应来制取硝酸铜:
①铜屑与稀硝酸反应的化学反应方程式为
②此法的两个缺点是
您最近一年使用:0次
名校
2 . 根据化学能转化电能的相关知识,回答下列问题:
I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是___________ ,发生___________ (填“氧化”或“还原”)反应,电解质溶液是___________ 。
(2)正极上出现的现象是___________ 。
(3)若导线上转移电子1mol,则生成银___________ g。___________ 。
(5)写出乙中负极的电极反应式:___________ 。
Ⅲ.电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。___________ (填“正极”或“负极”);
(7)①正极的电极反应式为___________ 。
②若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为___________ 。
I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是
(2)正极上出现的现象是
(3)若导线上转移电子1mol,则生成银
II.有甲、乙两位同学均想利用原电池反应检测金属 活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol·L-1的H2SO4溶液中,乙同学将电极放入6mol·L-1的NaOH溶液中,如图所示。
活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol·L-1的H2SO4溶液中,乙同学将电极放入6mol·L-1的NaOH溶液中,如图所示。

(5)写出乙中负极的电极反应式:
Ⅲ.电化学法处理SO2是目前研究的热点。利用过氧化氢吸收SO2可消除SO2污染,设计装置如图所示。
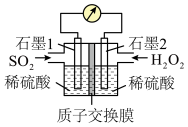
(7)①正极的电极反应式为
②若11.2L(标准状况)SO2参与反应,则迁移H+的物质的量为
您最近一年使用:0次
名校
3 . 已知: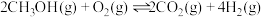 的能量变化如图所示,在绝热恒容的密闭容器中发生该反应,下列说法错误的是
的能量变化如图所示,在绝热恒容的密闭容器中发生该反应,下列说法错误的是
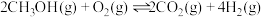 的能量变化如图所示,在绝热恒容的密闭容器中发生该反应,下列说法错误的是
的能量变化如图所示,在绝热恒容的密闭容器中发生该反应,下列说法错误的是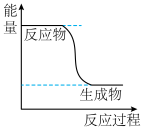
| A.当容器内温度不再变化时,反应处于平衡状态 |
B.反应过程中, 的生成速率与 的生成速率与 的消耗速率之比为2∶1 的消耗速率之比为2∶1 |
| C.当容器内压强不再变化时,反应处于平衡状态 |
| D.1mol甲醇和1mol氧气反应达到平衡状态后,O2(g)的物质的量为0.5mol |
您最近一年使用:0次
4 . 下列四个常用电化学装置的叙述错误的是
|
|
|
|
| 图I水果电池 | 图II干电池 | 图III铅蓄电池 | 图IV氢氧燃料电池 |
A.图  所示电池中,电子从锌片流出 所示电池中,电子从锌片流出 |
B.图  所示干电池中锌作负极 所示干电池中锌作负极 |
C.图 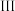 所示电池中正极反应为:PbO2 + 4H+ = Pb2+ + 2H2O 所示电池中正极反应为:PbO2 + 4H+ = Pb2+ + 2H2O |
D.图  所示电池中正极反应为: 所示电池中正极反应为: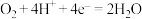 |
您最近一年使用:0次
名校
5 . 回答下列问题
(1)工业合成氨反应: 非常重要,氨在工农业生产中应用广泛。已知:键能是
非常重要,氨在工农业生产中应用广泛。已知:键能是 化学键完全断裂形成气态原子所需要吸收的能量,数值如表格所示。结合合成氨反应过程中的能量变化图,求x=
化学键完全断裂形成气态原子所需要吸收的能量,数值如表格所示。结合合成氨反应过程中的能量变化图,求x=___________ 。
(2)实验室中模拟合成氨过程,将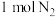 和
和 置于恒温,体积为
置于恒温,体积为 的容器中进行反应。
的容器中进行反应。
①单位时间内生成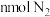 的同时,生成
的同时,生成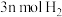
②单位时间内生成
③ 、
、 和
和 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2
④混合气体的密度不再改变
⑤混合气体的压强不再改变
⑥混合气体的平均相对分子质量不再改变
可说明该反应达到化学平衡状态的是___________ (填序号);若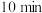 时测得氢气浓度为
时测得氢气浓度为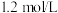 ,则用氨气表示的
,则用氨气表示的 内化学反应速率为
内化学反应速率为___________ ; 时的体系总压强与初始时的总压强之比
时的体系总压强与初始时的总压强之比___________ 。
(3)在四个不同的容器中,在不同的条件下进行合成反应:N2 + 3H2 2NH3根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
2NH3根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
(4)工业合成氨过程中,按一定投料比将原料气置于反应容器中,测得在不同温度和压强下达到化学平衡状态时的氮的平衡含量(%)如表格所示:
实际生产时,常选择 ,
,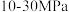 作为反应条件。请结合以上表格数据,从温度或压强的角度,分别分析选择此温度或压强的原因。
作为反应条件。请结合以上表格数据,从温度或压强的角度,分别分析选择此温度或压强的原因。
①温度:___________ ;②压强:___________ 。
(5) ,可视为
,可视为 分子中的
分子中的 被
被 取代的产物。
取代的产物。 —空气燃料电池是一种高效低污染(氧化产物为N2)的新型电池,其结构如图所示。通入
—空气燃料电池是一种高效低污染(氧化产物为N2)的新型电池,其结构如图所示。通入 (肼)的一极的电极反应式为
(肼)的一极的电极反应式为___________ 。
(1)工业合成氨反应:
 非常重要,氨在工农业生产中应用广泛。已知:键能是
非常重要,氨在工农业生产中应用广泛。已知:键能是 化学键完全断裂形成气态原子所需要吸收的能量,数值如表格所示。结合合成氨反应过程中的能量变化图,求x=
化学键完全断裂形成气态原子所需要吸收的能量,数值如表格所示。结合合成氨反应过程中的能量变化图,求x=
| 化学键 | H-H | N-H | N≡N |
| 键能/(kJ∙mol-1) | 436 | 391 | x |
(2)实验室中模拟合成氨过程,将
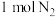 和
和 置于恒温,体积为
置于恒温,体积为 的容器中进行反应。
的容器中进行反应。①单位时间内生成
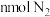 的同时,生成
的同时,生成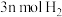
②单位时间内生成

③
 、
、 和
和 的物质的量浓度之比为1:3:2
的物质的量浓度之比为1:3:2④混合气体的密度不再改变
⑤混合气体的压强不再改变
⑥混合气体的平均相对分子质量不再改变
可说明该反应达到化学平衡状态的是
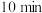 时测得氢气浓度为
时测得氢气浓度为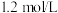 ,则用氨气表示的
,则用氨气表示的 内化学反应速率为
内化学反应速率为 时的体系总压强与初始时的总压强之比
时的体系总压强与初始时的总压强之比(3)在四个不同的容器中,在不同的条件下进行合成反应:N2 + 3H2
 2NH3根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________
2NH3根据在相同时间内测定的结果判断,生成氨气的反应速率由大到小排列___________| A.v(H2) = 0.01 mol/(Lˑs) | B.v(N2) = 0.3mol/(Lˑmin) |
| C.v(NH3)= 0.15mol/(Lˑmin) | D.v(H2) = 0.3 mol/(Lˑmin) |
(4)工业合成氨过程中,按一定投料比将原料气置于反应容器中,测得在不同温度和压强下达到化学平衡状态时的氮的平衡含量(%)如表格所示:
| 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.2 | 79.8 |
| 500 | 0 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23 | 31.4 |
 ,
,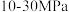 作为反应条件。请结合以上表格数据,从温度或压强的角度,分别分析选择此温度或压强的原因。
作为反应条件。请结合以上表格数据,从温度或压强的角度,分别分析选择此温度或压强的原因。①温度:
(5)
 ,可视为
,可视为 分子中的
分子中的 被
被 取代的产物。
取代的产物。 —空气燃料电池是一种高效低污染(氧化产物为N2)的新型电池,其结构如图所示。通入
—空气燃料电池是一种高效低污染(氧化产物为N2)的新型电池,其结构如图所示。通入 (肼)的一极的电极反应式为
(肼)的一极的电极反应式为
您最近一年使用:0次
6 . 氮化硅( )是一种重要的结构陶瓷材料。用石英砂和原料气(含
)是一种重要的结构陶瓷材料。用石英砂和原料气(含 和少量
和少量 )制备
)制备 的操作流程如下(粗硅中含少量Fe、Cu的单质及化合物):
的操作流程如下(粗硅中含少量Fe、Cu的单质及化合物):
 )是一种重要的结构陶瓷材料。用石英砂和原料气(含
)是一种重要的结构陶瓷材料。用石英砂和原料气(含 和少量
和少量 )制备
)制备 的操作流程如下(粗硅中含少量Fe、Cu的单质及化合物):
的操作流程如下(粗硅中含少量Fe、Cu的单质及化合物):
| A.“还原”是焦炭被还原为CO |
B.“高温氮化”反应的化学方程式为 |
| C.“操作X”可将原料气通过灼热的铜粉 |
| D.“稀酸Y”可选用稀硝酸 |
您最近一年使用:0次
名校
7 . 对于下列所述过程,能正确描述其反应离子方程式的是
A.向 溶液中通入过量 溶液中通入过量 气体:SiO 气体:SiO  +CO2+ H2O = H2SiO3↓ +CO +CO2+ H2O = H2SiO3↓ +CO  |
B.硫代硫酸钠溶液与稀硫酸混合:S2O  +2H+=SO2↑+S↓+H2O +2H+=SO2↑+S↓+H2O |
| C.硫化亚铁落于稀硝酸中: FeS + 2H+=Fe2+ +H2S↑ |
D.稀NaOH溶液和稀NH4Cl溶液混合:NH +OH = NH3↑ + H2O +OH = NH3↑ + H2O |
您最近一年使用:0次
8 . 用NA表示阿伏伽德罗常数的值,下列说法正确的是
| A.1L 1mol/L的氨水中含有 NH3.H2O 分子的数目为NA |
| B.过量的Cu与含0.2molHNO3的浓硝酸反应,转移电子的数目大于0.1NA |
C.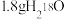 与 与 的混合物中含有的质子数和电子数均为 的混合物中含有的质子数和电子数均为 |
| D.1molO2与2molSO2一定条件下充分反应,生成SO3的分子数为2NA |
您最近一年使用:0次
名校
9 . 下列反应中,硝酸既表现酸性,又表现氧化性的是
| A.碳跟浓硝酸反应 | B.铜跟稀硝酸反应 |
| C.CuO跟稀硝酸反应 | D.常温下Al跟浓硝酸反应 |
您最近一年使用:0次
名校
解题方法
10 . I 亚硝酰氯(NOCl)是有机药物制备的重要试剂,可按以下流程合成和利用。
(1)NOCl的电子式为___________ ,化合物X的结构简式为___________ 。
(2)下列说法正确的是___________。
(3)已知浓盐酸和浓硝酸混合配制王水时会产生亚硝酰氯,写出该反应的化学方程式___________ 。
Ⅱ 请回答下列问题:
(4)由磷原子核形成的三种微粒:a. 、b.
、b. 、c.
、c. ,半径由大到小的顺序为
,半径由大到小的顺序为___________ (填标号,下同);再失去一个电子所需最低能量由大到小的顺序为___________ 。
(5)比较H-O-H键角大小;H3O+___________ H2O(填“>”、“<”或“=”)。
(6)C为有机材料的主角,Si为无机材料的主角,SiC结构类似金刚石,下图为SiC的晶胞图,其中两个正方体中心重合、各面分别平行,其中心为Si原子(用•表示),试在小立方体画出相应C原子(用 表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。
表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。___________

(1)NOCl的电子式为
(2)下列说法正确的是___________。
| A.NOCl中的氮元素呈正价 |
| B.NOCl分子的空间结构为直线形 |
C.化合物X的沸点低于氯乙酰胺(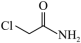 ) ) |
| D.工业上可以用蒸馏水吸收多余的NOCl,防止污染环境 |
(3)已知浓盐酸和浓硝酸混合配制王水时会产生亚硝酰氯,写出该反应的化学方程式
Ⅱ 请回答下列问题:
(4)由磷原子核形成的三种微粒:a.
 、b.
、b. 、c.
、c. ,半径由大到小的顺序为
,半径由大到小的顺序为(5)比较H-O-H键角大小;H3O+
(6)C为有机材料的主角,Si为无机材料的主角,SiC结构类似金刚石,下图为SiC的晶胞图,其中两个正方体中心重合、各面分别平行,其中心为Si原子(用•表示),试在小立方体画出相应C原子(用
 表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。
表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。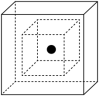
您最近一年使用:0次






 1
1

