1 .  是一种二元弱酸,
是一种二元弱酸, 溶液中各型体浓度在其总浓度中所占比值叫其分布系数,常温下某浓度的
溶液中各型体浓度在其总浓度中所占比值叫其分布系数,常温下某浓度的 溶液中各型体分布系数随pH的变化如图所示,据此分析,下列说法不正确的是
溶液中各型体分布系数随pH的变化如图所示,据此分析,下列说法不正确的是
 是一种二元弱酸,
是一种二元弱酸, 溶液中各型体浓度在其总浓度中所占比值叫其分布系数,常温下某浓度的
溶液中各型体浓度在其总浓度中所占比值叫其分布系数,常温下某浓度的 溶液中各型体分布系数随pH的变化如图所示,据此分析,下列说法不正确的是
溶液中各型体分布系数随pH的变化如图所示,据此分析,下列说法不正确的是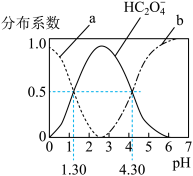
A.曲线a代表 ,曲线b代表 ,曲线b代表 |
B.常温下0.1mol/L的 溶液显酸性 溶液显酸性 |
C.常温下, 的电离平衡常数 的电离平衡常数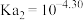 |
D.pH从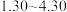 时, 时,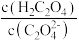 先增大后减小 先增大后减小 |
您最近一年使用:0次
2022-10-05更新
|
703次组卷
|
10卷引用:四川省广安、遂宁、内江、眉山四市2017届高三第二次诊断考试理综化学试题
四川省广安、遂宁、内江、眉山四市2017届高三第二次诊断考试理综化学试题福建省泰宁第一中学2020届高三上学期第一阶段考试化学试题吉林省长春市十一高中2022-2023学年高二上学期第一学程考试化学试题北京市首都师范大学附属中学2022-2023学年高二上学期期中考试化学试题首都师范大学附属中学2022-2023高二上学期期中练习化学试题山东省威海乳山市银滩高级中学2022-2023学年高二12月月考化学试题湖北省武汉市常青联合体2022-2023学年高二上学期期中考试化学试题(已下线)专项特训5 弱电解质电离常数计算与图像分析云南省昆明市第一中学2023-2024学年高二上学期12月月考化学试题吉林省长春市第五中学长春市田家炳实验中学2023-2024学年高二上学期第一学程考试化学试题
名校
2 . 2021 年作为“十四五”开局之年,调整能源结构,应对碳排放已列入政府工作重点。缓解温室效应,合理利用CO2的碳科技也是当前国际社会关注的热点之一、已知:
I. CO2(g)+H2(g) CO(g)+H2O(g) ΔH=+41.7kJ/mol
CO(g)+H2O(g) ΔH=+41.7kJ/mol
II. CO(g)+2H2(g) CH3OH (g) ΔH=-92.3kJ/mol
CH3OH (g) ΔH=-92.3kJ/mol
回答下列问题:
(1)二氧化碳与氢气生成甲醇(CH3OH)蒸气和水蒸气的热化学方程式为___________ 。
(2)一定条件下,向5L恒容密闭容器中充入2mol CO2(g)和4mol H2(g)发生上述I、II反应,实验测得反应平衡时CH3OH(g)、H2O(g)的物质的量与温度的关系如图1所示。
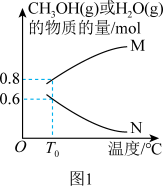
①图中表示CH3OH(g)的物质的量与温度关系的曲线为___________ (填“M”或“N”), T0°C时, 若反应在2min时恰好达到平衡状态,则反应的平均速率v(CO2)=___________ mol/(L·min);
②在T0°C温度下,反应II的化学平衡常数的表达式Kc=___________ ,恒温恒容条件下,能判断该反应(反应II)达到平衡的标志为___________ (填序号)
a. v(CO)=2v(H2)
b.反应体系的总压强保持恒定不变
c.气体密度保持恒定不变
d. CH3OH的质量分数不变
(3)2020年世界十大科技进展,排在第四位的就是借助光将二氧化碳催化转化为甲醇(CH3OH),这是迄今最接近人造光合作用的方法。某光电催化反应装置如图所示,A电极是Pt/CNT,B电极是TiO2。通过光解水,可由CO2制得甲醇。
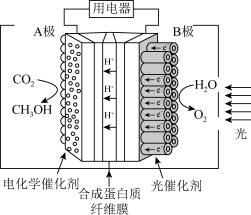
①B极是电池的___________ 极(填“正”或“负”)
②写出A极的电极反应式为___________ 。
I. CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH=+41.7kJ/mol
CO(g)+H2O(g) ΔH=+41.7kJ/molII. CO(g)+2H2(g)
 CH3OH (g) ΔH=-92.3kJ/mol
CH3OH (g) ΔH=-92.3kJ/mol回答下列问题:
(1)二氧化碳与氢气生成甲醇(CH3OH)蒸气和水蒸气的热化学方程式为
(2)一定条件下,向5L恒容密闭容器中充入2mol CO2(g)和4mol H2(g)发生上述I、II反应,实验测得反应平衡时CH3OH(g)、H2O(g)的物质的量与温度的关系如图1所示。

①图中表示CH3OH(g)的物质的量与温度关系的曲线为
②在T0°C温度下,反应II的化学平衡常数的表达式Kc=
a. v(CO)=2v(H2)
b.反应体系的总压强保持恒定不变
c.气体密度保持恒定不变
d. CH3OH的质量分数不变
(3)2020年世界十大科技进展,排在第四位的就是借助光将二氧化碳催化转化为甲醇(CH3OH),这是迄今最接近人造光合作用的方法。某光电催化反应装置如图所示,A电极是Pt/CNT,B电极是TiO2。通过光解水,可由CO2制得甲醇。

①B极是电池的
②写出A极的电极反应式为
您最近一年使用:0次
2022-08-13更新
|
287次组卷
|
3卷引用:四川省广安市2021-2022学年高三上学期零诊理科综合化学试题
解题方法
3 . 已知二氨烯丹( )是一种除草剂,其合成路线如下:
)是一种除草剂,其合成路线如下:
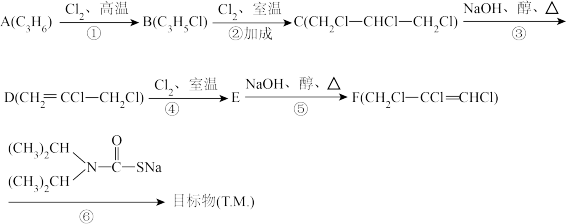
(1)A的结构简式为_______ ,按照系统命名,C的名称为_______
(2)反应③的化学方程式为_______ ,上述流程中,与该反应具有相同反应类型的有_______ (填标号)。
(3)检验E中官能团所用的化学试剂有_______ 。
(4)由上述反应⑥预测 中的较稳定Cl是
中的较稳定Cl是_______ (选填“苯环上氯”或甲基上氧”)。
(5)写出CH2ClCHClCH2Cl的所有同分异构体中,核磁共振氢谱有两种峰的结构构简式_____ 。
(6)设计由丙烯和对甲基苯酚制备 (树脂)的合成线路(无机试利任选)
(树脂)的合成线路(无机试利任选)_______ 。
 )是一种除草剂,其合成路线如下:
)是一种除草剂,其合成路线如下:
(1)A的结构简式为
(2)反应③的化学方程式为
(3)检验E中官能团所用的化学试剂有
(4)由上述反应⑥预测
 中的较稳定Cl是
中的较稳定Cl是(5)写出CH2ClCHClCH2Cl的所有同分异构体中,核磁共振氢谱有两种峰的结构构简式
(6)设计由丙烯和对甲基苯酚制备
 (树脂)的合成线路(无机试利任选)
(树脂)的合成线路(无机试利任选)
您最近一年使用:0次
4 . 下列实验操作或实验设计正确的是
A. 提纯乙酸乙酯 提纯乙酸乙酯 | B.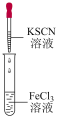 Fe3+的检验 Fe3+的检验 |
C.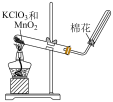 制取少量O2 制取少量O2 | D.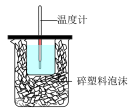 中和反应热的测定 中和反应热的测定 |
您最近一年使用:0次
2022-07-27更新
|
552次组卷
|
2卷引用:四川省广安市2022届高三上学期第一次诊断考试理科综合化学试题
5 . 根皮素R(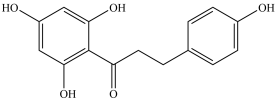 )可 应用于面膜、护肤膏霜和精华素中。其中一种合成R的路线如下:
)可 应用于面膜、护肤膏霜和精华素中。其中一种合成R的路线如下:
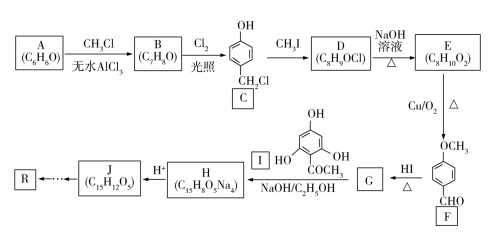
已知:①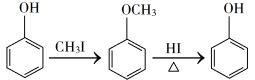
②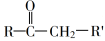 +R”CHO
+R”CHO
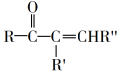 +H2O
+H2O
(1)A的化学名称是
(2)G的结构简式是
(3)I中的官能团的名称是
(4)D→E的化学方程式为
(5)F的同分异构体有多种,请写出同时符合下列条件的F的同分异构体的结构简式:
①苯环上有两个且处于邻位的侧链
②能发生银镜反应
③能与FeCl3溶液发生显色反应
(6)设计以丙酮和1,3-二氯丙烷为起始原料制备
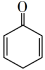 的合 成路线
的合 成路线
您最近一年使用:0次
解题方法
6 . 氧锰八面体纳米棒(OMS-2)是一种新型的环保催化剂。用软锰矿和黄铁矿(主要成分分别为MnO2、FeS2) 合成OMS-2的工艺流程如下:
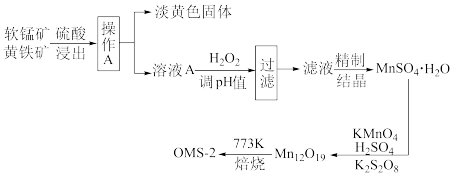
常温条件下,离子沉淀时的pH数据:
(1)为了加快浸出的效率,可以采取的措施是:______ (写一条即可)
(2)实验操作A所需的玻璃仪器有:___ 、烧杯、玻璃棒;MnO2有强氧化性,则淡黄色固体除了有未反应完的矿石外,还有___________ (填化学式)
(3)溶液A中加入H2O2的作用是将Fe2+氧化为Fe3+,写出其反应方程式___________ ;“ 调pH值”步骤中,pH的调节范围是___________ ;当离子浓度≤1.0×10-5mol/L时,可视为该离子完全沉淀,则由题中的数据信息,计算Ksp[Fe(OH)2]=___________ 。
(4)“精制结晶”步骤中的具体操作为:蒸发浓缩,冷却结晶,___________ 、___________ ,干燥;
(5)生产过程中的原料KMnO4、K2S2O8、 MnSO4·H2O 按物质的量比1:1:5反应,产物中硫元素全部以 的形式存在,该反应的离子方程式为
的形式存在,该反应的离子方程式为___________ 。

常温条件下,离子沉淀时的pH数据:
| 金属离子 | Fe3+ | Fe2+ | Mn2+ |
| 开始沉淀的pH | 2.2 | 7.5 | 8.8 |
| 完全沉淀的pH | 3.2 | 9.0 | 10.8 |
(1)为了加快浸出的效率,可以采取的措施是:
(2)实验操作A所需的玻璃仪器有:
(3)溶液A中加入H2O2的作用是将Fe2+氧化为Fe3+,写出其反应方程式
(4)“精制结晶”步骤中的具体操作为:蒸发浓缩,冷却结晶,
(5)生产过程中的原料KMnO4、K2S2O8、 MnSO4·H2O 按物质的量比1:1:5反应,产物中硫元素全部以
 的形式存在,该反应的离子方程式为
的形式存在,该反应的离子方程式为
您最近一年使用:0次
名校
解题方法
7 . 碘酸钙[Ca(IO3)2]是广泛使用的既能补钙又能补碘的新型食品添加剂,不溶于乙醇,在水中的溶解度随温度降低而减小。实验室制取Ca(IO3)2的流程如图所示:
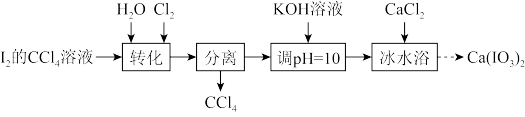
已知:碘酸(HIO3)是易溶于水的强酸,不溶于有机溶剂。
(1)实验流程中“转化”步骤是为了制得碘酸,该过程在下图所示的装置中进行(部分仪器省略)。
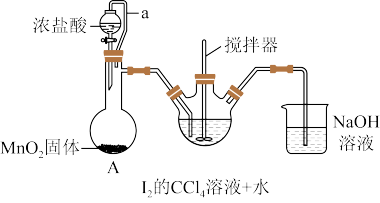
①盛装浓盐酸的仪器的名称为___________ 。
②橡皮管a的作用是___________ 。
③装置A中反应需要加热,其反应的离子方程式___________ 。
(2)三颈烧瓶中发生“转化”的化学方程式___________ 。
(3)流程中采用冰水浴的目的是__ 。
(4)有关该实验说法正确的是__ 。
A.分离出CCl4的操作为分液。
B.“调pH=10”后的溶液中只含有KIO3
C.制得的碘酸钙可选用酒精溶液洗涤
(5)准确称取产品0.25g,加酸溶解后,再加入足量KI发生反应 +5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液,用0.2000 mol·L-1Na2S2O3溶液滴定(I2+2
+5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液,用0.2000 mol·L-1Na2S2O3溶液滴定(I2+2 =2I-+
=2I-+ )至终点,消耗Na2S2O3溶液30.00mL。达滴定终点时的现象是
)至终点,消耗Na2S2O3溶液30.00mL。达滴定终点时的现象是___________ , 产品中Ca(IO3)2的质量分数___________ [已知Ca(IO3)2的摩尔质量: 390g·mol-1]

已知:碘酸(HIO3)是易溶于水的强酸,不溶于有机溶剂。
(1)实验流程中“转化”步骤是为了制得碘酸,该过程在下图所示的装置中进行(部分仪器省略)。

①盛装浓盐酸的仪器的名称为
②橡皮管a的作用是
③装置A中反应需要加热,其反应的离子方程式
(2)三颈烧瓶中发生“转化”的化学方程式
(3)流程中采用冰水浴的目的是
(4)有关该实验说法正确的是
A.分离出CCl4的操作为分液。
B.“调pH=10”后的溶液中只含有KIO3
C.制得的碘酸钙可选用酒精溶液洗涤
(5)准确称取产品0.25g,加酸溶解后,再加入足量KI发生反应
 +5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液,用0.2000 mol·L-1Na2S2O3溶液滴定(I2+2
+5I-+6H+=3I2+3H2O,滴入2~3滴淀粉溶液,用0.2000 mol·L-1Na2S2O3溶液滴定(I2+2 =2I-+
=2I-+ )至终点,消耗Na2S2O3溶液30.00mL。达滴定终点时的现象是
)至终点,消耗Na2S2O3溶液30.00mL。达滴定终点时的现象是
您最近一年使用:0次
2022-07-23更新
|
744次组卷
|
5卷引用:四川省广安市2021-2022学年高三上学期零诊理科综合化学试题
四川省广安市2021-2022学年高三上学期零诊理科综合化学试题黑龙江省双鸭山市第一中学2022-2023学年高三上学期开学考试化学试题(已下线)第29讲 化学综合实验(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)易错点09 氯元素及其化合物-备战2023年高考化学考试易错题四川省成都市新都区2022-2023学年高三上学期期末摸底测试理科综合化学试题
8 . 广安市某中学的化学课外兴趣小组,利用手持技术,进行了酸碱中和滴定实验: 25°C时,向10.00mL 0.10mol/LCH3COOH溶液中,逐滴加入0.10mol/L NaOH溶液,通过pH传感器,在电脑上得到了pH变化曲线如图所示。下列说法正确的是
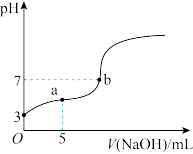

| A.25°C时,CH3COOH的电离平衡常数Ka=1.0 ×10-6 |
| B.b点表示的溶液中c(Na+) < c(CH3COO-) |
| C.a点表示的溶液中2c(Na+)=c(CH3COO-)+c(CH3COOH) |
| D.a、b两点所示的溶液中水的电离程度较大的是a点 |
您最近一年使用:0次
9 . 科学家最近采用碳基电极材料设计了一种新的工艺方案消除甲醇对水质造成的污染,主要包括电化学过程和化学过程,原理如下图所示,下列说法准确的是
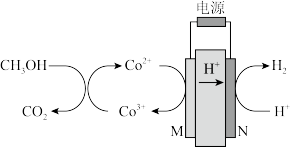

| A.该装置将化学能转化为电能 |
| B.N极发生还原反应,接电源的负极 |
| C.电解过程中,需要不断的向溶液中补充Co2+ |
| D.阳极区消除甲醇的反应为:CH3OH+Co3+=CO2+Co2+ |
您最近一年使用:0次
10 . W、 X、Y、Z是四种常见的短周期主族元素,且原子序数依次增大。已知W的一种核素的质量数为18,中子数为10; X是短周期元素中原子半径最大的元素(不考虑稀有气体的原子半径); Y的单质呈淡黄色,常见于火山口附近。下列说法不正确的是
| A.氧化物的水化物酸性: Y<Z |
| B.简单离子半径:X<W<Z |
| C.简单气态氢化物的稳定性: W>Y |
| D.W与X可形成既有离子键又有共价键的化合物 |
您最近一年使用:0次



