I 亚硝酰氯(NOCl)是有机药物制备的重要试剂,可按以下流程合成和利用。
(1)NOCl的电子式为___________ ,化合物X的结构简式为___________ 。
(2)下列说法正确的是___________。
(3)已知浓盐酸和浓硝酸混合配制王水时会产生亚硝酰氯,写出该反应的化学方程式___________ 。
Ⅱ 请回答下列问题:
(4)由磷原子核形成的三种微粒:a. 、b.
、b. 、c.
、c. ,半径由大到小的顺序为
,半径由大到小的顺序为___________ (填标号,下同);再失去一个电子所需最低能量由大到小的顺序为___________ 。
(5)比较H-O-H键角大小;H3O+___________ H2O(填“>”、“<”或“=”)。
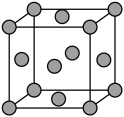
(6)C为有机材料的主角,Si为无机材料的主角,SiC结构类似金刚石,下图为SiC的晶胞图,其中两个正方体中心重合、各面分别平行,其中心为Si原子(用•表示),试在小立方体画出相应C原子(用 表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。
表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。___________

(1)NOCl的电子式为
(2)下列说法正确的是___________。
| A.NOCl中的氮元素呈正价 |
| B.NOCl分子的空间结构为直线形 |
C.化合物X的沸点低于氯乙酰胺(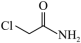 ) ) |
| D.工业上可以用蒸馏水吸收多余的NOCl,防止污染环境 |
(3)已知浓盐酸和浓硝酸混合配制王水时会产生亚硝酰氯,写出该反应的化学方程式
Ⅱ 请回答下列问题:
(4)由磷原子核形成的三种微粒:a.
 、b.
、b. 、c.
、c. ,半径由大到小的顺序为
,半径由大到小的顺序为(5)比较H-O-H键角大小;H3O+
(6)C为有机材料的主角,Si为无机材料的主角,SiC结构类似金刚石,下图为SiC的晶胞图,其中两个正方体中心重合、各面分别平行,其中心为Si原子(用•表示),试在小立方体画出相应C原子(用
 表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。
表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。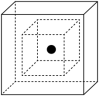
更新时间:2024-05-10 16:52:51
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如下图所示的转化关系:

(1)如果A、B、C、D均是10电子的粒子,请写出:
A的电子式_____________ ;D的电子式____________ ;
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,请写出:
①A与B在溶液中反应的离子方程式:____________________________________
②根据上述离子方程式,可判断C与B结合质子的能力大小是(用化学式或离子符号表示)________ >________ 。

(1)如果A、B、C、D均是10电子的粒子,请写出:
A的电子式
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,请写出:
①A与B在溶液中反应的离子方程式:
②根据上述离子方程式,可判断C与B结合质子的能力大小是(用化学式或离子符号表示)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】随着原子序数的递增,八种短周期元素(用字母x、y、z……表示)的原子半径相对大小、最高正价或最低负价的变化如下图所示。
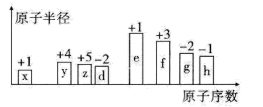
请回答下列问题:
(1)d的简单氢化物的沸点比同主族相邻元素的氢化物沸点___________ (填“高”或“低”),原因是:___________ ;x与e形成的化合物电子式为___________
(2)比较g、h常见离子的半径大小:___________ (填化学式,下同);比较e、f的最高价氧化物对应水化物的碱性强弱:___________ 。
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶1∶1∶3,其化学式为___________ 。
②能形成共价化合物,写出其中一种的结构简式___________ 。

请回答下列问题:
(1)d的简单氢化物的沸点比同主族相邻元素的氢化物沸点
(2)比较g、h常见离子的半径大小:
(3)x、y、z、d四种元素能形成多种化合物。
①能形成离子化合物,其中一种x、y、z、d四种原子的个数比为5∶1∶1∶3,其化学式为
②能形成共价化合物,写出其中一种的结构简式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】元素X、Q、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4;R-、Z+、X+离子半径逐渐减小;化合物XR常温下为气体,Q和Y在周期表中的位置相邻,请回答下列问题:
(1)写出单质R的一种工业用途_______________________ 。
(2)M和R的最高价氧化物的水化物中酸性最强的是___________ (用化学式表示)。
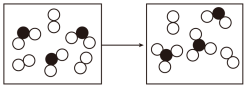
(3)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,写出该转化过程的化学方程式为____________________ 。
(4)由X、Y、Z、M四种元素组成的一种离子化合物A,已知A,既能与盐酸反应,又能与氢氧化钠溶液反应,还能和氯水反应,写出A与氯水反应的离子方程式___________ 。
(5)科学家认为存在QX5这种物质,且预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,已知QX5中含有离子键和极性键,写出化合物的电子式___________ 。
(1)写出单质R的一种工业用途
(2)M和R的最高价氧化物的水化物中酸性最强的是
(3)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,写出该转化过程的化学方程式为

(4)由X、Y、Z、M四种元素组成的一种离子化合物A,已知A,既能与盐酸反应,又能与氢氧化钠溶液反应,还能和氯水反应,写出A与氯水反应的离子方程式
(5)科学家认为存在QX5这种物质,且预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,已知QX5中含有离子键和极性键,写出化合物的电子式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如 显粉红色。
显粉红色。
(1)试判断,
___________ (填“有”或“无”)颜色。
(2)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为 ,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是
,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是___________ (填序号)。并解释不正确的原因___________ 。
A.PFS中铁显+3价
B.铁原子的外围电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
(3)铬的配合物在药物应用、设计合成新磁材料领域和聚乙烯催化剂方面都有重要应用。现有铬(Ⅱ)与甲基丙烯酸根的配合物如图:

①该化合物中一个Cr的配位数为___________ 。
②甲基丙烯酸分子中C原子的杂化方式为___________ 。
③等电子体是具有相同的价电子数和原子数的分子或离子,与H2O分子互为等电子体的微粒是___________ (填两种分子、离子各一种)。
 显粉红色。
显粉红色。(1)试判断,

(2)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为
 ,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是
,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是A.PFS中铁显+3价
B.铁原子的外围电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
| 元素 | Mn | Fe | |
| 电离能/(kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(3)铬的配合物在药物应用、设计合成新磁材料领域和聚乙烯催化剂方面都有重要应用。现有铬(Ⅱ)与甲基丙烯酸根的配合物如图:

①该化合物中一个Cr的配位数为
②甲基丙烯酸分子中C原子的杂化方式为
③等电子体是具有相同的价电子数和原子数的分子或离子,与H2O分子互为等电子体的微粒是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】金属铜、铁、铝等在人类文明史上先后被广泛使用。回答下列问题:
(1)基态铜原子价层电子排布式为_________ ;基态Fe原子中未成对电子数为___ ;
基态铝原子电子占据最高能级的电子云轮廓图为_________ 形。
(2)实验测得气态氯化铝分子的结构式为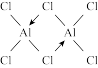 ,氯化铝是
,氯化铝是_________ 晶体,气态氯化铝中存在____ (填字母序号)。
A.离子键 B.配位键 C.氢键 D.范德华力 E.金属键 F.非极性共价键
(3)某些氧化物的熔点数据如表所示:
解释表中氧化物的熔点存在差异的原因:__________ 。
(4)CuCO3可用于制备高温超导体,其3种组成元素中电负性最大的是______ (填元素符号),CO 的空间构型是
的空间构型是_________ ,其中碳原子的杂化方式为_________ 。
(5)氮化铝晶胞结构可看作金刚石晶胞(如图所示)内部的碳原子被N原子代替,顶点和面心的碳原子被铝原子代替。AlN晶体中N和N的原子核间距为apm,AlN摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,则AlN晶体的密度为______ g·cm-3(1pm=10-12m)。

(1)基态铜原子价层电子排布式为
基态铝原子电子占据最高能级的电子云轮廓图为
(2)实验测得气态氯化铝分子的结构式为
 ,氯化铝是
,氯化铝是A.离子键 B.配位键 C.氢键 D.范德华力 E.金属键 F.非极性共价键
(3)某些氧化物的熔点数据如表所示:
| 氧化物 | SO3 | K2O | CuO |
| 熔点/℃ | 62.3 | 350 | 1026 |
(4)CuCO3可用于制备高温超导体,其3种组成元素中电负性最大的是
 的空间构型是
的空间构型是(5)氮化铝晶胞结构可看作金刚石晶胞(如图所示)内部的碳原子被N原子代替,顶点和面心的碳原子被铝原子代替。AlN晶体中N和N的原子核间距为apm,AlN摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,则AlN晶体的密度为

您最近一年使用:0次
【推荐3】安徽省具有丰富的铜矿资源,请回答下列有关铜及其化合物的问题,
(1)请写出基态Cu原子的外围电子排布式____________ 。焰火中的绿色是铜的焰色,基态铜原子在灼烧时外围电子发生了 _________ 而变为激发态。
(2)新型农药松脂酸铜具有低残留的特点,下图是松脂酸铜的结构简式

请分析1个松脂酸铜中π键的个数_____ ;加 “*”碳原子的杂化方式为 ______ 。
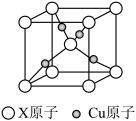
(3)下图是某铜矿的晶胞图,请推算出此晶胞的化学式(以X表示某元素符号)______________ ;与X等距离且最近的X原子个数为____
(4)黄铜矿在冶炼的时候会产生副产品SO2,SO2分子的几何构型______ ,比较第一电离能:S _____ O(填“>”或“<”)
(5)黄铜合金可以表示为Cu3Zn,为面心立方晶胞,晶体密度为8.5g/cm3,求晶胞的边长(只写计算式,不求结果)____________ nm。
(1)请写出基态Cu原子的外围电子排布式
(2)新型农药松脂酸铜具有低残留的特点,下图是松脂酸铜的结构简式

请分析1个松脂酸铜中π键的个数
(3)下图是某铜矿的晶胞图,请推算出此晶胞的化学式(以X表示某元素符号)

(4)黄铜矿在冶炼的时候会产生副产品SO2,SO2分子的几何构型
(5)黄铜合金可以表示为Cu3Zn,为面心立方晶胞,晶体密度为8.5g/cm3,求晶胞的边长(只写计算式,不求结果)

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】研究物质的微观结构,有助于理解物质变化规律和本质。
(1)氨气的水溶液中存在多种氢键,任意表示出其中一种:_______ 。
(2)CO与N2分子结构相似,下表是二者的键能数据( )。
)。
①1个CO分子中含有的π键数目是个_______ 个。
②结合数据比较活泼性:CO_______ N2(填“>”或“<”)。
(3)利用 可以合成化工原料
可以合成化工原料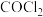 、配合物
、配合物 等。
等。
①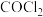 分子结构式为:
分子结构式为: ,该分子空间结构为
,该分子空间结构为_______ 。
② 常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂。据此可以判断
常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂。据此可以判断 晶体属于
晶体属于_______ 晶体。
③ 在一定条件下发生分解反应:
在一定条件下发生分解反应: ,反应过程中,断裂的化学键只有配位键,形成的化学键是
,反应过程中,断裂的化学键只有配位键,形成的化学键是_______ 。
(4)过硫酸(分子式:H2S2O8;结构式: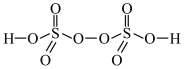 )为无色晶体,易溶于水,在热水中易水解。下列说法正确的是
)为无色晶体,易溶于水,在热水中易水解。下列说法正确的是_______ (填序号)。
a.过硫酸属于共价化合物
b.过硫酸分子中含有与过氧化氢分子中相同的化学键
c.过硫酸分子可看作2个硫酸分子脱去1个水分子
(1)氨气的水溶液中存在多种氢键,任意表示出其中一种:
(2)CO与N2分子结构相似,下表是二者的键能数据(
 )。
)。| 分子 | C-O | C=O | C≡O | 分子 | N-N | N=N | N≡N |
| CO | 351 | 745 | 1071 | N2 | 193 | 418 | 946 |
①1个CO分子中含有的π键数目是个
②结合数据比较活泼性:CO
(3)利用
 可以合成化工原料
可以合成化工原料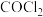 、配合物
、配合物 等。
等。①
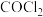 分子结构式为:
分子结构式为: ,该分子空间结构为
,该分子空间结构为②
 常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂。据此可以判断
常温下呈液态,熔点为—20.5℃,沸点为103℃,易溶于非极性溶剂。据此可以判断 晶体属于
晶体属于③
 在一定条件下发生分解反应:
在一定条件下发生分解反应: ,反应过程中,断裂的化学键只有配位键,形成的化学键是
,反应过程中,断裂的化学键只有配位键,形成的化学键是(4)过硫酸(分子式:H2S2O8;结构式:
 )为无色晶体,易溶于水,在热水中易水解。下列说法正确的是
)为无色晶体,易溶于水,在热水中易水解。下列说法正确的是a.过硫酸属于共价化合物
b.过硫酸分子中含有与过氧化氢分子中相同的化学键
c.过硫酸分子可看作2个硫酸分子脱去1个水分子
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】含碳元素的物质是化学世界中最庞大的家族。回答下列问题:
(1)碳在形成化合物时,其键型以共价键为主, 中的化学键从形成的过程来看属于
中的化学键从形成的过程来看属于___________ (填“ ”或“
”或“ ”)键,从其极性来看属于
”)键,从其极性来看属于___________ (填“极性”或“非极性”)键。
(2) 、HCN、CO、
、HCN、CO、 分子中属于非极性分子的是
分子中属于非极性分子的是___________ ;与 互为等电子体的阳离子是
互为等电子体的阳离子是___________ 。(等电子体:原子数目相同,价电子总数相同的微粒。)
(3)有机物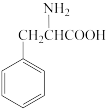 中含氧官能团的名称为
中含氧官能团的名称为___________ ,其中含有___________ 个手性碳原子。
(4)甲醇与乙烷的相对分子质量和范德华力均相近,但是二者的沸点相差很大,造成该差异的原因是___________ 。
(1)碳在形成化合物时,其键型以共价键为主,
 中的化学键从形成的过程来看属于
中的化学键从形成的过程来看属于 ”或“
”或“ ”)键,从其极性来看属于
”)键,从其极性来看属于(2)
 、HCN、CO、
、HCN、CO、 分子中属于非极性分子的是
分子中属于非极性分子的是 互为等电子体的阳离子是
互为等电子体的阳离子是(3)有机物
 中含氧官能团的名称为
中含氧官能团的名称为(4)甲醇与乙烷的相对分子质量和范德华力均相近,但是二者的沸点相差很大,造成该差异的原因是
您最近一年使用:0次
【推荐3】第Ⅷ族元素 、
、 、
、 性质相似,称为铁系元素,主要用于制造合金。回答下列问题:
性质相似,称为铁系元素,主要用于制造合金。回答下列问题:
(1)基态 原子核外能量最高的电子位于
原子核外能量最高的电子位于_______ 能级,同周期元素中,基态原子未成对电子数与 相同的元素名称为
相同的元素名称为______________ 。
(2)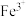 与酚类物质的显色反应常用于其离子检验,已知
与酚类物质的显色反应常用于其离子检验,已知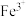 遇邻苯二酚(
遇邻苯二酚( )和对苯二酚(
)和对苯二酚( )均显绿色。邻苯二酚的熔沸点比对苯二酚
)均显绿色。邻苯二酚的熔沸点比对苯二酚_____ (填“高”或“低”),原因是_________ 。
(3)有历史记载的第一个配合物是 (普鲁士蓝),该配合物的内界为
(普鲁士蓝),该配合物的内界为__________ 。表为 、
、 不同配位数时对应的晶体场稳定化能(可衡量形成配合物时,总能量的降低)。由表可知,
不同配位数时对应的晶体场稳定化能(可衡量形成配合物时,总能量的降低)。由表可知, 比较稳定的配离子配位数是
比较稳定的配离子配位数是__________ (填“4”或“6”)。 性质活泼,易被还原,但
性质活泼,易被还原,但 很稳定,可能的原因是
很稳定,可能的原因是________________ 。
(4) 晶体结构中阴阳离子的配位数均为6,则晶胞的俯视图可能是
晶体结构中阴阳离子的配位数均为6,则晶胞的俯视图可能是_______ (填选项字母)。若晶胞参数为apm,阿伏加 德罗常数的值为 ,晶体的密度是
,晶体的密度是________  。
。

 、
、 、
、 性质相似,称为铁系元素,主要用于制造合金。回答下列问题:
性质相似,称为铁系元素,主要用于制造合金。回答下列问题:(1)基态
 原子核外能量最高的电子位于
原子核外能量最高的电子位于 相同的元素名称为
相同的元素名称为(2)
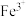 与酚类物质的显色反应常用于其离子检验,已知
与酚类物质的显色反应常用于其离子检验,已知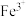 遇邻苯二酚(
遇邻苯二酚( )和对苯二酚(
)和对苯二酚( )均显绿色。邻苯二酚的熔沸点比对苯二酚
)均显绿色。邻苯二酚的熔沸点比对苯二酚(3)有历史记载的第一个配合物是
 (普鲁士蓝),该配合物的内界为
(普鲁士蓝),该配合物的内界为 、
、 不同配位数时对应的晶体场稳定化能(可衡量形成配合物时,总能量的降低)。由表可知,
不同配位数时对应的晶体场稳定化能(可衡量形成配合物时,总能量的降低)。由表可知, 比较稳定的配离子配位数是
比较稳定的配离子配位数是 性质活泼,易被还原,但
性质活泼,易被还原,但 很稳定,可能的原因是
很稳定,可能的原因是| 离子 | 配位数 | 晶体场稳定化能(Dq) |
 | 6 | -8Dq+2p |
| 4 | -5.34Dq+2p | |
 | 6 | -12Dq+3p |
| 4 | -3.56Dq+3p |
(4)
 晶体结构中阴阳离子的配位数均为6,则晶胞的俯视图可能是
晶体结构中阴阳离子的配位数均为6,则晶胞的俯视图可能是 ,晶体的密度是
,晶体的密度是 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】钛由于其稳定的化学性质,良好的耐高温、耐低温、抗强酸、抗强碱以及高强度、低密度,被美誉为“未来钢铁”、“战略金属”。
(1)基态钛原子核外共有_____ 种运动状态不相同的电子,价电子排布式____________________ ;与钛同周期的元素中,基态原子的未成对电子数与钛相同的有__ 种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是___________________ 。
(3)TiCl4是氧化法制取钛的中间产物。TiCl4分子结构与CCl4相同,在常温下都是液体。TiCl4分子的空间构型是_______________ ,Ti原子采取____ 杂化方式;TiCl4稳定性比CCl4差,极易水解,试从结构分析其原因:_______________________________ 。
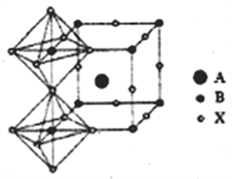
(4)钙钛矿材料是一类有着与钛酸钙(CaTiO3)相同晶体结构的材料,这种奇特的晶体结构让它具备了很多独特的理化性质,比如吸光性、电催化性等。CaTiO3晶体结构如图所示。其中,A代表__________ (写离子符号),它的配位数是___________ 。
(1)基态钛原子核外共有
(2)钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是
(3)TiCl4是氧化法制取钛的中间产物。TiCl4分子结构与CCl4相同,在常温下都是液体。TiCl4分子的空间构型是
(4)钙钛矿材料是一类有着与钛酸钙(CaTiO3)相同晶体结构的材料,这种奇特的晶体结构让它具备了很多独特的理化性质,比如吸光性、电催化性等。CaTiO3晶体结构如图所示。其中,A代表

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】碳族元素( Carbongroup)是位于元素周期表ⅣA族的元素,包括碳(C)、硅(Si)、锗(Ge)、锡(Sn)、铅(Pb)、鈇(Fl)六种。请回答
(1)鈇(Fl),其命名是为了纪念苏联原子物理学家乔治·弗洛伊洛夫,是一种人工合成的放射性化学元素,它的化学符号是Uuq,它的原子序数是____________ ,属于弱金属之一。
(2)基态锡原子价电子的轨道表示式为________________ 与其同周期且未成对电子数相同的元素还有______ 种.
(3)晶体硅的密度为ρg/cm3其晶胞结构与金刚石相似,若硅原子半径为r pm,NA表示阿伏伽德罗常数的值,M(Si)表示硅的相对原子质量,则硅晶胞中原子的体积占晶胞体积的百分率为__________ 用含ρ、r、NA、M(Si)的代数式表示]。
(4)GeO2、SiO2均为共价型化合物,熔点分别为1388K、1983K,则GeO2为______ (填晶体类型),SiO2的熔点高于GeO2的原因为______________ .
(5)三氯甲烷(Trichloromethane)为无色透明液体。有特殊气味,味甜,低毒,有麻醉性。有致癌可能性。三氯甲烷的VSEPR模型为_____ ,与三氯甲烷互为等电子体的阴离子为________ (任写一种)。
(6)石墨烯研究近年有了长足发展。2017年,清华任天令团队曾首次实现石墨烯智能人工喉,贴附在聋哑人喉部便可以辅助聋哑人“开口说话”。石墨烯与金属R可以形成一种插层化合物。其中R层平行于石墨层,晶胞如图甲所示,其垂直于石墨层方向的投影如图乙所示。则该插层化合物的化学式为________ ;若碳碳键的键长为apm,则同层最邻近的两个钾原子之间的距离为_________ pm。(用含a的代数式表示)

(1)鈇(Fl),其命名是为了纪念苏联原子物理学家乔治·弗洛伊洛夫,是一种人工合成的放射性化学元素,它的化学符号是Uuq,它的原子序数是
(2)基态锡原子价电子的轨道表示式为
(3)晶体硅的密度为ρg/cm3其晶胞结构与金刚石相似,若硅原子半径为r pm,NA表示阿伏伽德罗常数的值,M(Si)表示硅的相对原子质量,则硅晶胞中原子的体积占晶胞体积的百分率为
(4)GeO2、SiO2均为共价型化合物,熔点分别为1388K、1983K,则GeO2为
(5)三氯甲烷(Trichloromethane)为无色透明液体。有特殊气味,味甜,低毒,有麻醉性。有致癌可能性。三氯甲烷的VSEPR模型为
(6)石墨烯研究近年有了长足发展。2017年,清华任天令团队曾首次实现石墨烯智能人工喉,贴附在聋哑人喉部便可以辅助聋哑人“开口说话”。石墨烯与金属R可以形成一种插层化合物。其中R层平行于石墨层,晶胞如图甲所示,其垂直于石墨层方向的投影如图乙所示。则该插层化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】如图所示,直线交点处的圆圈为NaCl晶体中Na+离子或Cl-离子所处的位置。这两种离子在空间三个互相垂直的方向上都是等距离排列的。

(1)晶体中,在每个Na+离子的周围与它最接近的且距离相等的Na+离子共有____ 个。
(2)已知食盐晶体的密度为2.2g/cm3,阿伏加德罗常数为6.02×1023mol-1。食盐晶体中两个距离最近的钠离子中心间的距离为________________ cm。计算过程如下:
_________________________________________________________________________________________________________________________________________________________ 。

(1)晶体中,在每个Na+离子的周围与它最接近的且距离相等的Na+离子共有
(2)已知食盐晶体的密度为2.2g/cm3,阿伏加德罗常数为6.02×1023mol-1。食盐晶体中两个距离最近的钠离子中心间的距离为
您最近一年使用:0次



