1 . 下列实验对应的解释或结论正确的是
| 选项 | 实验 | 解释或结论 |
| A | 室温下,向含少量 的 的 溶液中加入铜屑,充分搅拌,过滤,得蓝色溶液 溶液中加入铜屑,充分搅拌,过滤,得蓝色溶液 | 杂质 被除去,得到纯净的 被除去,得到纯净的 溶液 溶液 |
| B |  晶体溶于稀硫酸,滴加 晶体溶于稀硫酸,滴加 溶液,溶液变红 溶液,溶液变红 |  晶体已变质 晶体已变质 |
| C | 向铅丹 中滴加浓盐酸,生成黄绿色气体 中滴加浓盐酸,生成黄绿色气体 | 氧化性: |
| D | 将铁的氧化物溶于过量稀盐酸中,再滴加几滴酸性 溶液,紫红色褪去 溶液,紫红色褪去 | 铁的氧化物含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 下列方案设计、现象和结论都正确的是
| 实验方案 | 现象 | 结论 | |
| A | 取某固体试样加入适量水,取少许于试管中,滴加NaOH溶液,并将湿润的红色石蕊试纸接近管口 | 湿润红色石蕊试纸无明显现象 | 该固体试样中一定不存在NH |
| B | 在橡胶塞侧面挖一个凹槽,嵌入下端卷成螺旋状的铜丝,向具支试管中加入2mL浓硝酸,用橡胶塞塞住试管口,使铜丝与硝酸接触,一段时间后,向上拉铜丝,终止反应 | 剧烈反应,铜丝表面放出红棕色的气泡,铜不断溶解,溶液变成绿色 | 浓硝酸具有强氧化性 |
| C | 取未知溶液于试管中,加入BaCl2溶液,有白色沉淀生成,再加足量稀盐酸 | 沉淀不溶解 | 溶液中一定含有SO |
| D | 向Fe(NO3)2溶液中滴加稀盐酸,再加入几滴KSCN溶液 | 溶液变为红色 | 稀盐酸可以将Fe2+氧化为Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列有关溶液中离子检验的说法正确的是
A.取样,加入硝酸酸化,再加入Ba(NO3)2溶液,若产生白色沉淀,则原溶液中存在 |
| B.取样,先加入少量氯水,再加入KSCN溶液,若溶液变红色,则原溶液中存在 Fe3+ |
| C.取样,加入硝酸酸化的AgNO3溶液:若无黄色沉淀,则原溶液中不存在I- |
| D.用洁净的铂丝蘸取溶液,在酒精灯外焰上灼烧,若火焰不呈紫色,则原溶液中不存在 K+ |
您最近一年使用:0次
2024-04-09更新
|
57次组卷
|
2卷引用:河南省周口市鹿邑县2023-2024学年高一下学期3月月考化学试题
解题方法
4 . 工业上用FeCl3溶液做印刷电路铜板的腐蚀液。化学小组设计如下流程对腐蚀废液(阳离子主要有H+、Fe3+、Fe2+和Cu2+)进行处理,实现FeCl3溶液再生并回收Cu。
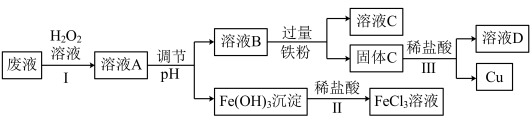
(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:_____________ ;
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为__________ ;
(3)步骤Ⅱ中发生反应的化学方程式为_____________ ;
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?_____________ ;
(5)固体C中的成分为________________ (填化学式);
(6)步骤Ⅲ中发生反应的离子方程式为___________ ,分离的操作名称为_______ 。

(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为
(3)步骤Ⅱ中发生反应的化学方程式为
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?
(5)固体C中的成分为
(6)步骤Ⅲ中发生反应的离子方程式为
您最近一年使用:0次
名校
解题方法
5 . 某变质的废铜屑主要成分为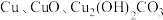 (其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
(其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是

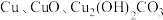 (其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
(其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
A.基态铜原子的价层电子排布式为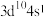 |
B.滤液1的溶质主要成分为 |
C.若分铜过程生成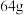 铜,则浸泡过程理论上有 铜,则浸泡过程理论上有 电子转移 电子转移 |
D.可用铁氰化钾溶液检验滤液2中 的存在 的存在 |
您最近一年使用:0次
名校
6 . 铋酸钠(NaBiO3)是常用的氧化剂,MnO2是活性电极。以辉铋矿(主要成分为Bi2S3,含FeS2、SiO2杂质)和软锰矿(主要成分是MnO2)为原料联合焙烧制备NaBiO3和MnO2,流程如下:
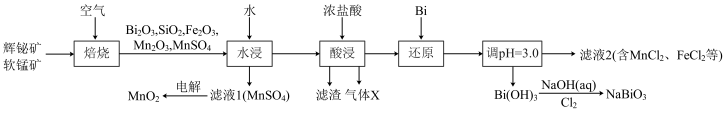
已知:①金属活动性:Fe>(H)>Bi>Cu。
②几种金属离子的氢氧化物沉淀pH如下:
回答下列问题:
(1)NaBiO3中Bi的化合价为_____ 。气体X是_____ (填化学式)。
(2)“焙烧”中Bi2S3和MnO2与空气反应生成Bi2O3和MnSO4,写出其反应的化学方程式:_____ 。被还原的元素是_____ (填元素符号)。
(3)“还原”中Bi的作用是_____ 。
(4)检验滤液2中是否有FeCl3的试剂是_____ (填化学式)。
(5)已知Bi(OH)3难溶于水,NaBiO3难溶于冷水,写出冷水中利用Bi(OH)3制备NaBiO3的离子方程式:_____ 。
(6)为探究Cl2和NaBiO3的氧化性相对强弱,设计如下实验:

实验中观察到试管B中溶液变蓝色。
由上述实验现象可知,氧化性:NaBiO3_____ Cl2(填“>”或“<”)。与根据第(5)小题得出的NaBiO3与Cl2氧化性强弱关系相反,其主要原因是_____ 。

已知:①金属活动性:Fe>(H)>Bi>Cu。
②几种金属离子的氢氧化物沉淀pH如下:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.5 | 2.8 |
| Fe2+ | 6.3 | 8.3 |
| Mn2+ | 8.1 | 10.1 |
(1)NaBiO3中Bi的化合价为
(2)“焙烧”中Bi2S3和MnO2与空气反应生成Bi2O3和MnSO4,写出其反应的化学方程式:
(3)“还原”中Bi的作用是
(4)检验滤液2中是否有FeCl3的试剂是
(5)已知Bi(OH)3难溶于水,NaBiO3难溶于冷水,写出冷水中利用Bi(OH)3制备NaBiO3的离子方程式:
(6)为探究Cl2和NaBiO3的氧化性相对强弱,设计如下实验:

实验中观察到试管B中溶液变蓝色。
由上述实验现象可知,氧化性:NaBiO3
您最近一年使用:0次
名校
7 . 铁及其化合物是重要的化学物质,如天然磁石中含有较多的Fe3O4、三水合草酸合铁(Ⅲ)酸钾{K3[Fe(C2O4)3]·3H2O,呈绿色,可溶于水,难溶于乙醇,见光易分解}常用于化学光量计、绿矾(FeSO4·7H2O)是常用的还原剂。回答下列问题:
(1)电子工业中,常用氯化铁溶液腐蚀铜制造印刷电路板,该原理的离子方程式为_____ 。
(2)根据化合价及元素的性质,Na2S5可以改写为Na2S·4S、Fe3O4可以改写为FeO·Fe2O3,则Fe3Cl8可以改写为_____ 、Fe3I8可以改写为_____ 。
(3)可通过下列两个步骤制备三水合草酸合铁(Ⅲ)酸钾晶体。
步骤i:向盛有3.00g黄色晶体FeC2O4·2H2O的烧杯中,加入10.00mLK2C2O4溶液,加热至40℃左右,缓慢滴入过量的H2O2,一段时间后,出现红褐色沉淀。
步骤ii:加热至沸腾,分两次缓慢加入8.00~9.00mLH2C2O4溶液,至沉淀溶解,得到绿色溶液。加热浓缩、加入无水乙醇、结晶,抽滤干燥得7.860g三水合草酸合铁(III)酸钾晶体。
①步骤ⅰ中,生成三草酸合铁酸钾与另一种铁的化合物,该化合物为_____ (填化学式)。
②步骤ⅱ加入无水乙醇的目的是_____ 。
③实验小组完成实验后发现产率偏低,其主要原因可能是_____ 。
(4)8.34gFeSO4·7H2O(Mr=278)样品隔绝空气受热分解生成多种化合物过程的热重曲线(残留样品质量随温度变化的曲线)如图所示。
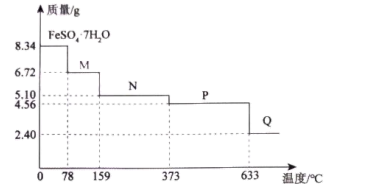
①温度为100℃时,固体物质M的化学式为_____ 。
②在隔绝空气的条件下,由P得到Q的化学方程式为_____ 。
(1)电子工业中,常用氯化铁溶液腐蚀铜制造印刷电路板,该原理的离子方程式为
(2)根据化合价及元素的性质,Na2S5可以改写为Na2S·4S、Fe3O4可以改写为FeO·Fe2O3,则Fe3Cl8可以改写为
(3)可通过下列两个步骤制备三水合草酸合铁(Ⅲ)酸钾晶体。
步骤i:向盛有3.00g黄色晶体FeC2O4·2H2O的烧杯中,加入10.00mLK2C2O4溶液,加热至40℃左右,缓慢滴入过量的H2O2,一段时间后,出现红褐色沉淀。
步骤ii:加热至沸腾,分两次缓慢加入8.00~9.00mLH2C2O4溶液,至沉淀溶解,得到绿色溶液。加热浓缩、加入无水乙醇、结晶,抽滤干燥得7.860g三水合草酸合铁(III)酸钾晶体。
①步骤ⅰ中,生成三草酸合铁酸钾与另一种铁的化合物,该化合物为
②步骤ⅱ加入无水乙醇的目的是
③实验小组完成实验后发现产率偏低,其主要原因可能是
(4)8.34gFeSO4·7H2O(Mr=278)样品隔绝空气受热分解生成多种化合物过程的热重曲线(残留样品质量随温度变化的曲线)如图所示。

①温度为100℃时,固体物质M的化学式为
②在隔绝空气的条件下,由P得到Q的化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 根据实验操作及现象,下列结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向 溶液中滴加KSCN溶液,溶液变红,再加入少量KCl固体,溶液颜色无明显变化 溶液中滴加KSCN溶液,溶液变红,再加入少量KCl固体,溶液颜色无明显变化 |  与 与 的反应不可逆 的反应不可逆 |
| B | 两支试管各盛 酸性高锰酸钾溶液,分别加入 酸性高锰酸钾溶液,分别加入 草酸溶液和 草酸溶液和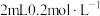 草酸溶液,观察溶液颜色变化 草酸溶液,观察溶液颜色变化 | 其他条件相同,反应物浓度越大,反应速率越快 |
| C | 加热足量的锌与少量浓硫酸的混合物,有大量气体产生 | 气体一定为 |
| D | 向2mL浓度均为 的KCl、KI混合溶液中滴加2滴 的KCl、KI混合溶液中滴加2滴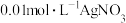 溶液,振荡,产生黄色沉淀 溶液,振荡,产生黄色沉淀 | 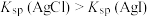 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
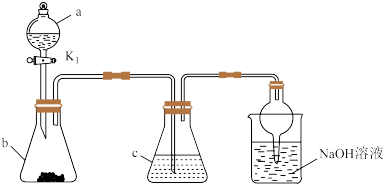
9 . 常温下,实验室利用如图装置进行实验,仪器 中无明显现象的是
中无明显现象的是
 中无明显现象的是
中无明显现象的是
| 选项 | a中的物质 | b中的物质 | c中的物质 |
| A | 浓硝酸 |  | 含有 的 的 溶液 溶液 |
| B | 稀醋酸 |  | 饱和碳酸钠溶液 |
| C | 浓硫酸 |  | 品红溶液 |
| D | 浓盐酸 |  | 淀粉 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-10-09更新
|
469次组卷
|
3卷引用:河南省周口市项城市5校联考2023-2024学年高三上学期10月月考化学试题
10 . 下列操作或事实与对应的化学原理不相符的是
| 选项 | 操作或事实 | 化学原理 |
| A | 用铝粉和氧化铁的混合物焊接钢轨 | 铝热反应放出大量的热使生成的铁熔化 |
| B |  溶液腐蚀覆铜板制作印刷电路板 溶液腐蚀覆铜板制作印刷电路板 | 铁的金属性比铜强 |
| C |  用作面包的膨松剂 用作面包的膨松剂 |  与酸反应或受热分解产生 与酸反应或受热分解产生 |
| D | 用漂白粉对生产车间进行环境杀菌、消毒 |  与空气中的 与空气中的 反应生成 反应生成 , , 具有强氧化性 具有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-06更新
|
60次组卷
|
2卷引用:河南省周口市项城市5校联考2023-2024学年高三上学期9月月考化学试题



