工业上用FeCl3溶液做印刷电路铜板的腐蚀液。化学小组设计如下流程对腐蚀废液(阳离子主要有H+、Fe3+、Fe2+和Cu2+)进行处理,实现FeCl3溶液再生并回收Cu。
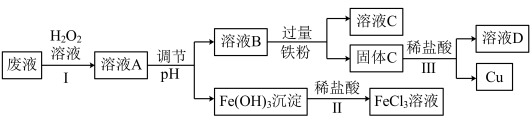
(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:_____________ ;
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为__________ ;
(3)步骤Ⅱ中发生反应的化学方程式为_____________ ;
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?_____________ ;
(5)固体C中的成分为________________ (填化学式);
(6)步骤Ⅲ中发生反应的离子方程式为___________ ,分离的操作名称为_______ 。

(1)FeCl3溶液腐蚀印刷电路铜板的化学方程式为:
(2)步骤Ⅰ的目的是将Fe2+转化为Fe3+,发生反应的离子方程式为
(3)步骤Ⅱ中发生反应的化学方程式为
(4)调节pH的目的是为了使溶液A中的Fe3+全部转化为Fe(OH)3沉淀,如何证明溶液B中没有Fe3+剩余?
(5)固体C中的成分为
(6)步骤Ⅲ中发生反应的离子方程式为
更新时间:2024-04-09 16:48:53
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
【推荐1】工业上采用硫铁矿焙烧去硫后的烧渣(主要成分为Fe2O3、FeO、SiO2、Al2O3,不考虑其他杂质) 制取七水合硫酸亚铁(FeSO4·7H2O),流程如下:
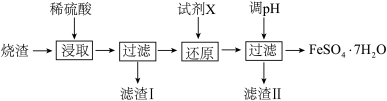
(1)浸取时,溶液中的Fe2+易被空气中的O2氧化,其离子方程式为__________________ 。能提高烧渣浸取速率的措施有__________________ (填字母)。
A.将烧渣粉碎 B.降低硫酸的浓度 C.适当升高温度
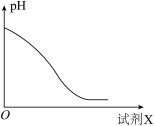
(2)还原时,试剂X的用量与溶液pH的变化如图所示,则试剂X可能是________ (填字母)。还原结束时,溶液中的主要阴离子有_____________ 。
A.Fe粉 B.SO2 C.NaI
(3)滤渣Ⅱ主要成分的化学式为__________________ ;由分离出滤渣Ⅱ后的溶液得到产品,进行的操作是_______________________________ 、过滤、洗涤、干燥。

(1)浸取时,溶液中的Fe2+易被空气中的O2氧化,其离子方程式为
A.将烧渣粉碎 B.降低硫酸的浓度 C.适当升高温度
(2)还原时,试剂X的用量与溶液pH的变化如图所示,则试剂X可能是
A.Fe粉 B.SO2 C.NaI

(3)滤渣Ⅱ主要成分的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】铁红(Fe2O3)是一种常见颜料,用废铁屑(主要含铁,还含有少量 Fe2O3)制取铁红的工艺如下:
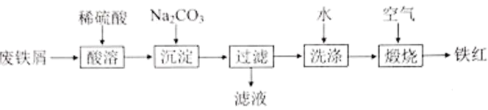
(1)写出废铁屑中的 Fe2O3 和稀硫酸反应的离子方程式:___________ 。
(2)“酸溶”一段时间后,溶液中检测不到 Fe3+的原因是___________ , 写出发生反应的离子方程式:___________ ; 检测 Fe3+常用___________ 试剂,现象是___________ , 反应的离子方程式:___________ 。
(3)“煅烧”时 FeCO3 与 O2 反应的物质的量之比为___________ 。

(1)写出废铁屑中的 Fe2O3 和稀硫酸反应的离子方程式:
(2)“酸溶”一段时间后,溶液中检测不到 Fe3+的原因是
(3)“煅烧”时 FeCO3 与 O2 反应的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】硫酸铁铵[NH4Fe(SO4)2•xH2O]是一种重要的铁盐,为充分利用资源,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如图:

回答下列问题:
(1)NH4Fe(SO4)2•xH2O中铁元素的化合价为____ 价。
(2)步骤②的操作名称为____ ,主要用到的玻璃仪器有烧杯、漏斗和玻璃棒,其中玻璃棒的作用为____ 。
(3)下列有关固体硫酸铵的说法正确的是____ (填标号)。
A.从物质的组成来看,硫酸铵属于氧化物
B.0.1mol硫酸铵中所含的氮元素的总质量为2.8g
C.固体硫酸铵不能导电,但其属于电解质
(4)步骤③中通入O2的目的是将Fe2+全部转化为Fe3+,请写出反应的离子方程式:____ ,该反应中,每转移0.2mol电子,此时消耗O2的体积为____ L(标准状况下)。

回答下列问题:
(1)NH4Fe(SO4)2•xH2O中铁元素的化合价为
(2)步骤②的操作名称为
(3)下列有关固体硫酸铵的说法正确的是
A.从物质的组成来看,硫酸铵属于氧化物
B.0.1mol硫酸铵中所含的氮元素的总质量为2.8g
C.固体硫酸铵不能导电,但其属于电解质
(4)步骤③中通入O2的目的是将Fe2+全部转化为Fe3+,请写出反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】从某含有 、
、 、
、 的工业废液中回收铜并制备氯化铁晶体的流程如下:
的工业废液中回收铜并制备氯化铁晶体的流程如下:
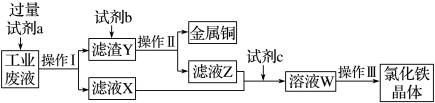
请回答:
(1)试剂 是
是_______ ,滤渣 是
是_______ 。
(2)加入试剂 所发生的离子方程式
所发生的离子方程式_______ 。
(3)下列说法正确的是_______。
 、
、 、
、 的工业废液中回收铜并制备氯化铁晶体的流程如下:
的工业废液中回收铜并制备氯化铁晶体的流程如下:
请回答:
(1)试剂
 是
是 是
是(2)加入试剂
 所发生的离子方程式
所发生的离子方程式(3)下列说法正确的是_______。
| A.操作Ⅰ、操作Ⅱ所用仪器相同 |
| B.操作Ⅲ是蒸发结晶 |
| C.整个流程中,涉及的反应中置换反应只有一个 |
D.滤液 和滤液 和滤液 所含溶质种类完全相同 所含溶质种类完全相同 |
您最近一年使用:0次
【推荐2】将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一,一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺流程提取其他产品。回答下问题:
Ⅰ.(1)为有效除去粗盐中 、
、 、
、 加入试剂的顺序不合理的是
加入试剂的顺序不合理的是___________ 。
A.先加NaOH,后加 ,再加
,再加
B.先加NaOH,后加 ,再加
,再加
C.先加 ,后加NaOH,再加
,后加NaOH,再加
(2)海水中提取金属镁的生产步骤有:①浓缩结晶 ②加熟石灰 ③加盐酸 ④过滤 ⑤熔融电解,正确的生产步骤是___________ 。(填序号)
(3)向海水中通入 ,将海水中的溴化物氧化,其离子方程式为
,将海水中的溴化物氧化,其离子方程式为___________ 。采用“空气吹出法”从浓海水中吹出 ,并用纯碱吸收。碱吸收溴的主要反应是
,并用纯碱吸收。碱吸收溴的主要反应是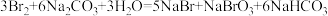 ,吸收1mol
,吸收1mol  时,转移的电子为
时,转移的电子为___________ mol。
Ⅱ.采用下面的工艺流程卤水生产单质碘:
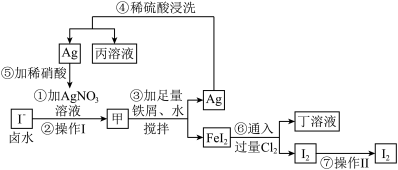
回答下列问题:
(4)操作I为___________ 。
(5)第④步的操作中用稀硫酸浸洗的目的是___________ 。
(6)丁溶液中的溶质为___________ (填化学式)。
(7)写出第⑤步反应的离子方程式___________ 。
Ⅰ.(1)为有效除去粗盐中
 、
、 、
、 加入试剂的顺序不合理的是
加入试剂的顺序不合理的是A.先加NaOH,后加
 ,再加
,再加
B.先加NaOH,后加
 ,再加
,再加
C.先加
 ,后加NaOH,再加
,后加NaOH,再加
(2)海水中提取金属镁的生产步骤有:①浓缩结晶 ②加熟石灰 ③加盐酸 ④过滤 ⑤熔融电解,正确的生产步骤是
(3)向海水中通入
 ,将海水中的溴化物氧化,其离子方程式为
,将海水中的溴化物氧化,其离子方程式为 ,并用纯碱吸收。碱吸收溴的主要反应是
,并用纯碱吸收。碱吸收溴的主要反应是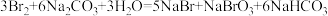 ,吸收1mol
,吸收1mol  时,转移的电子为
时,转移的电子为Ⅱ.采用下面的工艺流程卤水生产单质碘:

回答下列问题:
(4)操作I为
(5)第④步的操作中用稀硫酸浸洗的目的是
(6)丁溶液中的溶质为
(7)写出第⑤步反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】已知A是一种淡黄色固体,可做供氧剂,C为具有磁性的黑色晶体,E的焰色反应为黄色,F为红褐色固体(部分产物已略去)。
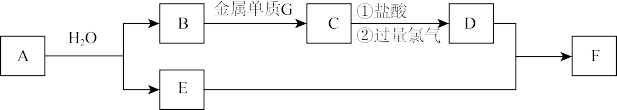
(1)物质A、F的化学式分别是_____________ 、_____________ 。
(2)C→D的过程中第②步反应的离子方程式是____________________________________ 。
(3)如何检验D中的金属阳离子,说明具体的操作和实验现象________________________ 。
(4)E溶液与地壳中含量最多的金属元素的单质发生反应的化学方程式为______________ 。
(5)G与D溶液也能发生反应,其反应的类型为___________________ (填序号)。
a.化合反应 b.置换反应 c.复分解反应 d.氧化还原反应

(1)物质A、F的化学式分别是
(2)C→D的过程中第②步反应的离子方程式是
(3)如何检验D中的金属阳离子,说明具体的操作和实验现象
(4)E溶液与地壳中含量最多的金属元素的单质发生反应的化学方程式为
(5)G与D溶液也能发生反应,其反应的类型为
a.化合反应 b.置换反应 c.复分解反应 d.氧化还原反应
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】某工厂以镍废渣(主要成分为 Ni,含少量 Fe、Fe3O4 、Al2O3 和不溶性杂质等)为原料制备翠矾 ( NiSO4 7H2O ),其生产工艺如下:
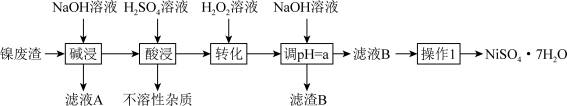
该流程中几种金属离子生成对应氢氧化物沉淀的 pH 如下表。回答下列问题:
(1)“滤液 A”中主要溶质的化学式为___________ 。
(2)“转化”过程中加入H2O2 的目的是将“酸浸”后溶液中的Fe2 氧化为Fe3 ,该过程用离子方程式表示为___________ ;“转化”过程中温度不宜过高,原因是__________ 。
(3)调节pH a ,是为了将溶液中的___________ 元素完全沉淀,则 a 的取值范围是___________ 。证明杂质离子已经被完全除去的实验操作及现象是:取少量滤液 B 于试管中,___________ 。
(4)“操作 1”的目的是将硫酸镍溶液变成NiSO4 7H2O ,具体操作是将溶液进行蒸发浓缩、___________ 、___________ 、洗涤、干燥。

该流程中几种金属离子生成对应氢氧化物沉淀的 pH 如下表。回答下列问题:
| 金属离子 | 开始沉淀的 pH | 完全沉淀的 pH |
| Fe3 | 2.7 | 3.7 |
| Fe2 | 7.6 | 9.7 |
| Ni2 | 7.1 | 9.2 |
(1)“滤液 A”中主要溶质的化学式为
(2)“转化”过程中加入H2O2 的目的是将“酸浸”后溶液中的Fe2 氧化为Fe3 ,该过程用离子方程式表示为
(3)调节pH a ,是为了将溶液中的
(4)“操作 1”的目的是将硫酸镍溶液变成NiSO4 7H2O ,具体操作是将溶液进行蒸发浓缩、
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
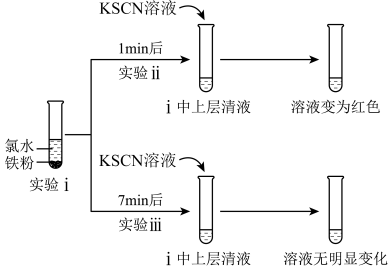
【推荐3】已知三氯化铁的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验。
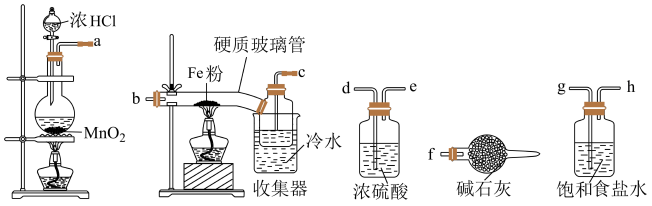
(1)装置的连接顺序为___ 。
(2)饱和食盐水的作用是___ 。
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
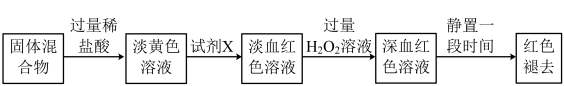
①淡黄色溶液中加入试剂X生成淡血红色溶液的离子方程式为__ 。
②淡血红色溶液中加入过量H2O2后溶液血红色加深的原因是__ 。
(4)已知血红色褪去的同时有气体生成,经检验为O2。该小组同学对血红色褪去的原因进行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现血红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
②另取同物质的量浓度的FeCl3溶液滴加2滴试剂X,溶液变血红,再通入O2,无明显变化。
实验①说明___ ;
实验②的目的是__ ;得出结论:___ 。

(1)装置的连接顺序为
(2)饱和食盐水的作用是
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

①淡黄色溶液中加入试剂X生成淡血红色溶液的离子方程式为
②淡血红色溶液中加入过量H2O2后溶液血红色加深的原因是
(4)已知血红色褪去的同时有气体生成,经检验为O2。该小组同学对血红色褪去的原因进行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现血红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
②另取同物质的量浓度的FeCl3溶液滴加2滴试剂X,溶液变血红,再通入O2,无明显变化。
实验①说明
实验②的目的是
您最近一年使用:0次