硫酸铁铵[NH4Fe(SO4)2•xH2O]是一种重要的铁盐,为充分利用资源,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如图:

回答下列问题:
(1)NH4Fe(SO4)2•xH2O中铁元素的化合价为____ 价。
(2)步骤②的操作名称为____ ,主要用到的玻璃仪器有烧杯、漏斗和玻璃棒,其中玻璃棒的作用为____ 。
(3)下列有关固体硫酸铵的说法正确的是____ (填标号)。
A.从物质的组成来看,硫酸铵属于氧化物
B.0.1mol硫酸铵中所含的氮元素的总质量为2.8g
C.固体硫酸铵不能导电,但其属于电解质
(4)步骤③中通入O2的目的是将Fe2+全部转化为Fe3+,请写出反应的离子方程式:____ ,该反应中,每转移0.2mol电子,此时消耗O2的体积为____ L(标准状况下)。

回答下列问题:
(1)NH4Fe(SO4)2•xH2O中铁元素的化合价为
(2)步骤②的操作名称为
(3)下列有关固体硫酸铵的说法正确的是
A.从物质的组成来看,硫酸铵属于氧化物
B.0.1mol硫酸铵中所含的氮元素的总质量为2.8g
C.固体硫酸铵不能导电,但其属于电解质
(4)步骤③中通入O2的目的是将Fe2+全部转化为Fe3+,请写出反应的离子方程式:
更新时间:2022-12-08 20:52:35
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
【推荐1】氯化钴{ ,常温下,
,常温下,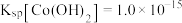 }在仪器制造、陶瓷、分析化学中用途广泛.回答下列问题:
}在仪器制造、陶瓷、分析化学中用途广泛.回答下列问题:
(1)已知钴与铁的化学性质相似.写出单质钴与稀硫酸反应的离子方程式:_________________ ;将 溶液加入坩埚中,然后用酒精喷灯持续加热,最终生成的固体物质是
溶液加入坩埚中,然后用酒精喷灯持续加热,最终生成的固体物质是_________________ (填化学式).
(2)将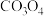 粉末与浓盐酸混合,可生成
粉末与浓盐酸混合,可生成 和一种黄绿色气体,写出该反应的化学方程式:
和一种黄绿色气体,写出该反应的化学方程式:_______________ ;该反应中,每生成 (标准状况下)黄绿色气体,转移电子数为
(标准状况下)黄绿色气体,转移电子数为_____________  .
.
(3)常温下,向 溶液中加入氨水调节
溶液中加入氨水调节 ,可以得到
,可以得到 ,若要使
,若要使 溶液中的
溶液中的 完全沉淀
完全沉淀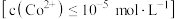 ,控制溶液的
,控制溶液的 最小为
最小为_____________ .
(4)一种从某含钴废料(主要成分为 ,及少量杂质
,及少量杂质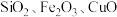 )制备
)制备 的工艺流程如下:
的工艺流程如下:

①滤渣的主要成分_____________ (填化学式).
②“操作a”的名称为_____________ ,所需要的玻璃仪器名称为烧杯、_____________ .
③向有机相加入足量的盐酸分离后,水相中除含有盐酸外,还含有_____________ (填化学式).
 ,常温下,
,常温下,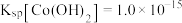 }在仪器制造、陶瓷、分析化学中用途广泛.回答下列问题:
}在仪器制造、陶瓷、分析化学中用途广泛.回答下列问题:(1)已知钴与铁的化学性质相似.写出单质钴与稀硫酸反应的离子方程式:
 溶液加入坩埚中,然后用酒精喷灯持续加热,最终生成的固体物质是
溶液加入坩埚中,然后用酒精喷灯持续加热,最终生成的固体物质是(2)将
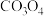 粉末与浓盐酸混合,可生成
粉末与浓盐酸混合,可生成 和一种黄绿色气体,写出该反应的化学方程式:
和一种黄绿色气体,写出该反应的化学方程式: (标准状况下)黄绿色气体,转移电子数为
(标准状况下)黄绿色气体,转移电子数为 .
.(3)常温下,向
 溶液中加入氨水调节
溶液中加入氨水调节 ,可以得到
,可以得到 ,若要使
,若要使 溶液中的
溶液中的 完全沉淀
完全沉淀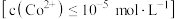 ,控制溶液的
,控制溶液的 最小为
最小为(4)一种从某含钴废料(主要成分为
 ,及少量杂质
,及少量杂质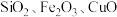 )制备
)制备 的工艺流程如下:
的工艺流程如下:
①滤渣的主要成分
②“操作a”的名称为
③向有机相加入足量的盐酸分离后,水相中除含有盐酸外,还含有
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】一种利用含Co废渣(主要含金属Co,还含有Fe、Zn)制取CoCO3的流程如下图所示:

已知:部分金属离子开始生成氢氧化物沉淀和沉淀完全的pH如下表所示:
(1)酸浸时,不改变H2SO4的浓度和体积,任写出一种可以加快反应速率的方法:_______ 。
(2)酸浸后所得溶液中含Co2+、Fe2+、Zn2+,基态Co2+的电子排布式为_______ 。
(3)加入ZnO调pH的目的是促进Fe3+水解转化为Fe(OH)3沉淀,调pH的范围为_______ ,加入ZnO将Fe3+转化为Fe(OH)3沉淀的离子方程式为_______ 。
(4)写出沉钴反应的离子方程式:_______ 。

已知:部分金属离子开始生成氢氧化物沉淀和沉淀完全的pH如下表所示:
| Fe3+ | Zn2+ | Fe2+ | Co2+ | |
| 开始沉淀的pH | 1.5 | 5.4 | 5.8 | 6.6 |
| 沉淀完全的pH | 3.2 | 8.2 | 8.8 | 9.4 |
(2)酸浸后所得溶液中含Co2+、Fe2+、Zn2+,基态Co2+的电子排布式为
(3)加入ZnO调pH的目的是促进Fe3+水解转化为Fe(OH)3沉淀,调pH的范围为
(4)写出沉钴反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】现有五种物质A、B、C、D、E,其中有一种是碱,四种是盐,溶于水后电离可以产生下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)写出A、C的化学式:_______ 、_______ ,X的名称:_______ 。
(2)B溶于水后的电离方程式为_______ 。
(3)完成以下水溶液中的反应的离子方程式:
A溶液与B溶液反应:_______ 。
B溶液与E反应:_______ 。
C溶液与 溶液反应:
溶液反应:_______ 。
| 阳离子 |    |
| 阴离子 |    |
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)写出A、C的化学式:
(2)B溶于水后的电离方程式为
(3)完成以下水溶液中的反应的离子方程式:
A溶液与B溶液反应:
B溶液与E反应:
C溶液与
 溶液反应:
溶液反应:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】氯酸锶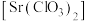 白色结晶粉末,可溶于水,微溶于酒精,主要用于制造红色焰火。
白色结晶粉末,可溶于水,微溶于酒精,主要用于制造红色焰火。 可溶于水,
可溶于水, 是一种常见的可溶性强碱。实验室制取氯酸锶的实验装置如图,反应的化学方程式为
是一种常见的可溶性强碱。实验室制取氯酸锶的实验装置如图,反应的化学方程式为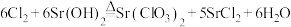 。已知将浓盐酸滴入高锰酸钾固体中,产生黄绿色气体,溶液的紫红色褪去。请回答下列问题:
。已知将浓盐酸滴入高锰酸钾固体中,产生黄绿色气体,溶液的紫红色褪去。请回答下列问题:

(1)仪器M的名称是___________ 。
(2)仪器接口的连接顺序a→___________ 。
(3)A中发生反应的离子方程式为___________ 。
(4)装置D中所装试剂名称为___________ ,其作用是___________ 。
(5)装置B中发生反应的离子方程式为___________ 。
(6)某兴趣小组在40℃条件下,将一定量的 通入一定量的
通入一定量的 溶液中,
溶液中, 恰好反应完全,得到的产物中含有
恰好反应完全,得到的产物中含有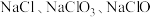 ,其中
,其中 和
和 的物质的量之比为5∶1,则此过程中氧化剂和还原剂的质量比为
的物质的量之比为5∶1,则此过程中氧化剂和还原剂的质量比为___________ 。
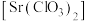 白色结晶粉末,可溶于水,微溶于酒精,主要用于制造红色焰火。
白色结晶粉末,可溶于水,微溶于酒精,主要用于制造红色焰火。 可溶于水,
可溶于水, 是一种常见的可溶性强碱。实验室制取氯酸锶的实验装置如图,反应的化学方程式为
是一种常见的可溶性强碱。实验室制取氯酸锶的实验装置如图,反应的化学方程式为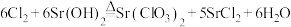 。已知将浓盐酸滴入高锰酸钾固体中,产生黄绿色气体,溶液的紫红色褪去。请回答下列问题:
。已知将浓盐酸滴入高锰酸钾固体中,产生黄绿色气体,溶液的紫红色褪去。请回答下列问题:
(1)仪器M的名称是
(2)仪器接口的连接顺序a→
(3)A中发生反应的离子方程式为
(4)装置D中所装试剂名称为
(5)装置B中发生反应的离子方程式为
(6)某兴趣小组在40℃条件下,将一定量的
 通入一定量的
通入一定量的 溶液中,
溶液中, 恰好反应完全,得到的产物中含有
恰好反应完全,得到的产物中含有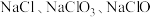 ,其中
,其中 和
和 的物质的量之比为5∶1,则此过程中氧化剂和还原剂的质量比为
的物质的量之比为5∶1,则此过程中氧化剂和还原剂的质量比为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】高铁酸钾( )是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
)是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
(1)高铁酸钾( )中铁元素的化合价为
)中铁元素的化合价为_______ 。
(2)写出 与KOH溶液反应的化学方程式
与KOH溶液反应的化学方程式_______ 。
(3)写出 溶液与碱性KClO溶液反应的离子方程式
溶液与碱性KClO溶液反应的离子方程式_______ 。
(4) 可作为新型多功能水处理剂的原因是
可作为新型多功能水处理剂的原因是_______ 。
(5)从“反应液Ⅱ”中分离出 后,副产品有
后,副产品有_______ (写化学式)。
(6)该工艺每得到1.98kg ,理论上消耗
,理论上消耗 的物质的量为
的物质的量为_______ mol。
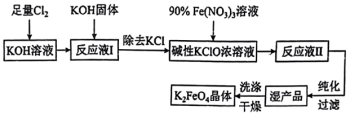
 )是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
)是一种高效多功能的新型非氯绿色消毒剂。其溶于水与水结合放出氧气并有絮状沉淀产生,常用作净水剂。其生产工艺如下:
(1)高铁酸钾(
 )中铁元素的化合价为
)中铁元素的化合价为(2)写出
 与KOH溶液反应的化学方程式
与KOH溶液反应的化学方程式(3)写出
 溶液与碱性KClO溶液反应的离子方程式
溶液与碱性KClO溶液反应的离子方程式(4)
 可作为新型多功能水处理剂的原因是
可作为新型多功能水处理剂的原因是(5)从“反应液Ⅱ”中分离出
 后,副产品有
后,副产品有(6)该工艺每得到1.98kg
 ,理论上消耗
,理论上消耗 的物质的量为
的物质的量为
您最近一年使用:0次
【推荐3】铁是一种重要的金属材料,它的单质及化合物在生产生活中应用广泛。
(1)某补铁口服液中含有 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加_______ ,若_______ ,则说明其已变质。
(2)工业盐的主要成分是 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力。以上事实说明
结合的能力。以上事实说明 具有
具有_______ 。下列不能实现上述转化的物质是_______ (填字母)。
A. B.
B. C.
C. D.
D.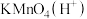
(3) 常用作杀菌消毒剂,生产
常用作杀菌消毒剂,生产 的反应原理是:
的反应原理是: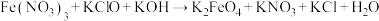 (未配平),则该反应中氧化剂与还原剂的物质的量之比为
(未配平),则该反应中氧化剂与还原剂的物质的量之比为_______ 。
(4)从制造印刷电路板的废液中回收铜,并重新获得 溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得
溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得 溶液,准备采用下列步骤:
溶液,准备采用下列步骤:

请写出上述流程中加入①和④的有关物质的化学式:①_______ ,④_______ 。请写出通入⑥反应的离子方程式_______ 。
(1)某补铁口服液中含有
 ,为检验其是否被氧化变质,可取少量该口服液,向其中滴加
,为检验其是否被氧化变质,可取少量该口服液,向其中滴加(2)工业盐的主要成分是
 ,曾多次发生过因误食
,曾多次发生过因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力。以上事实说明
结合的能力。以上事实说明 具有
具有A.
 B.
B. C.
C. D.
D.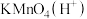
(3)
 常用作杀菌消毒剂,生产
常用作杀菌消毒剂,生产 的反应原理是:
的反应原理是: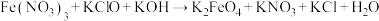 (未配平),则该反应中氧化剂与还原剂的物质的量之比为
(未配平),则该反应中氧化剂与还原剂的物质的量之比为(4)从制造印刷电路板的废液中回收铜,并重新获得
 溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得
溶液的工艺流程如下,某工程师为了从使用过的腐蚀废液中回收铜,并重新获得 溶液,准备采用下列步骤:
溶液,准备采用下列步骤:
请写出上述流程中加入①和④的有关物质的化学式:①
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】工业上用铝土矿(主要成分为Al2O3,含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:

已知:2Al2O3 4Al+3O2↑。
4Al+3O2↑。
(1)操作Ⅱ的名称___________ ,用到的玻璃仪器有_______________ 。
(2)X是___________ ,操作Ⅱ通入过量CO2的离子方程式:______________________________________ 。
(3)沉淀A的主要成分是________ ,在生活中有什么应用:________________________ 。

已知:2Al2O3
 4Al+3O2↑。
4Al+3O2↑。(1)操作Ⅱ的名称
(2)X是
(3)沉淀A的主要成分是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】高铝粉煤灰是火力发电厂燃煤锅炉排放出的固体废物,含有较多的Al2O3,少量MgO、CaO、 铁的氧化物及其他不溶性杂质。从粉煤灰中提取Al2O3的工艺流程如图。
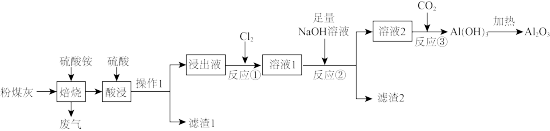
(1)操作1的名称是_______ , 滤渣1中除了原不溶性杂质外,还有_______ 。
(2)检验浸出液中含有Fe2+的操作与现象是_______ 。
(3)反应①的离子方程式为_______ ,反应①中还可以用_______ (填试剂化学式)替代Cl2。
(4)滤渣2的主要成分有_______ 。
(5)溶液2中含铝元素的化合物与过量CO2反应的化学方程式为_______ 。
(6)实验室配制100mL 2.00mol/L H2SO4溶液。
①需要18.00mol/L浓H2SO4的体积为_______ mL。(计算结果保留1位小数)
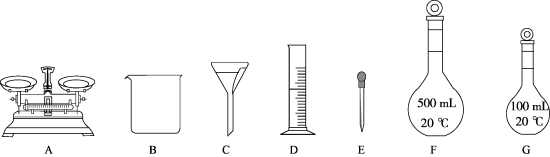
②下列仪器中,需要的有_______ (填标号),还缺少的玻璃仪器为_______ 。(填仪器名称)

(1)操作1的名称是
(2)检验浸出液中含有Fe2+的操作与现象是
(3)反应①的离子方程式为
(4)滤渣2的主要成分有
(5)溶液2中含铝元素的化合物与过量CO2反应的化学方程式为
(6)实验室配制100mL 2.00mol/L H2SO4溶液。
①需要18.00mol/L浓H2SO4的体积为
②下列仪器中,需要的有

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】自然界中的铝元素以化合物的形式存在于各种矿石中、某铝土矿的主要成分是 ,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
已知: 不溶于水且不与盐酸反应;
不溶于水且不与盐酸反应; 能与NaOH溶液反应,生成可溶性盐。
能与NaOH溶液反应,生成可溶性盐。

请回答下列问题。
(1)步骤①加盐酸前先将铝土矿粉碎的目的是_______ ;所得滤液A中的溶质有_______ 种。
(2)步骤②中所加NaOH溶液须过量的目的是___________ 。
(3)步骤③ 加热分解生成两种氧化物,请写出该反应的化学方程式
加热分解生成两种氧化物,请写出该反应的化学方程式___________ 。
(4)步骤④是通过电解熔融状态的 制备铝。
制备铝。 的熔点是
的熔点是 ,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义
,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义___________ 。
氧化亚铜( )可用于电镀工业。干法生产
)可用于电镀工业。干法生产 粉末的主要工艺流程如下:
粉末的主要工艺流程如下:

(5)粉碎机中,发生的变化属于___________ (填“物理变化”或“化学变化”)。
(6) 时,煅烧炉中发生化合反应,该反应的化学方程式为
时,煅烧炉中发生化合反应,该反应的化学方程式为___________ 。
 ,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):已知:
 不溶于水且不与盐酸反应;
不溶于水且不与盐酸反应; 能与NaOH溶液反应,生成可溶性盐。
能与NaOH溶液反应,生成可溶性盐。
请回答下列问题。
(1)步骤①加盐酸前先将铝土矿粉碎的目的是
(2)步骤②中所加NaOH溶液须过量的目的是
(3)步骤③
 加热分解生成两种氧化物,请写出该反应的化学方程式
加热分解生成两种氧化物,请写出该反应的化学方程式(4)步骤④是通过电解熔融状态的
 制备铝。
制备铝。 的熔点是
的熔点是 ,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义
,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义氧化亚铜(
 )可用于电镀工业。干法生产
)可用于电镀工业。干法生产 粉末的主要工艺流程如下:
粉末的主要工艺流程如下:
(5)粉碎机中,发生的变化属于
(6)
 时,煅烧炉中发生化合反应,该反应的化学方程式为
时,煅烧炉中发生化合反应,该反应的化学方程式为
您最近一年使用:0次



