高铝粉煤灰是火力发电厂燃煤锅炉排放出的固体废物,含有较多的Al2O3,少量MgO、CaO、 铁的氧化物及其他不溶性杂质。从粉煤灰中提取Al2O3的工艺流程如图。
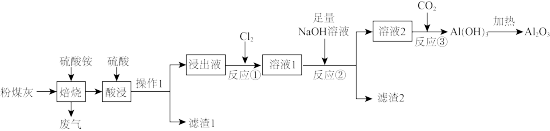
(1)操作1的名称是_______ , 滤渣1中除了原不溶性杂质外,还有_______ 。
(2)检验浸出液中含有Fe2+的操作与现象是_______ 。
(3)反应①的离子方程式为_______ ,反应①中还可以用_______ (填试剂化学式)替代Cl2。
(4)滤渣2的主要成分有_______ 。
(5)溶液2中含铝元素的化合物与过量CO2反应的化学方程式为_______ 。
(6)实验室配制100mL 2.00mol/L H2SO4溶液。
①需要18.00mol/L浓H2SO4的体积为_______ mL。(计算结果保留1位小数)
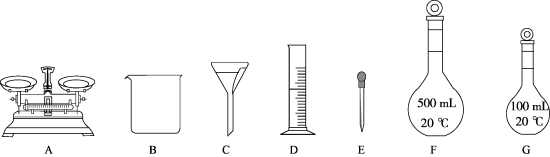
②下列仪器中,需要的有_______ (填标号),还缺少的玻璃仪器为_______ 。(填仪器名称)

(1)操作1的名称是
(2)检验浸出液中含有Fe2+的操作与现象是
(3)反应①的离子方程式为
(4)滤渣2的主要成分有
(5)溶液2中含铝元素的化合物与过量CO2反应的化学方程式为
(6)实验室配制100mL 2.00mol/L H2SO4溶液。
①需要18.00mol/L浓H2SO4的体积为
②下列仪器中,需要的有

更新时间:2022-08-18 19:48:58
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】某兴趣小组用废铝合金(成分为Al、Zn、Fe、Si)制备Al2O3和Fe2O3、ZnSO4·7H2O,流程如图:
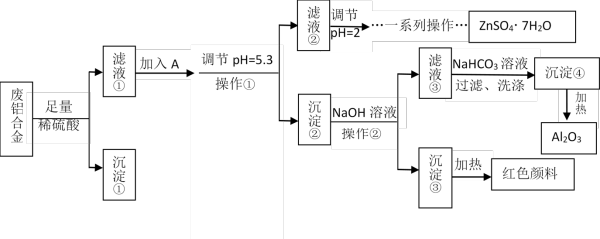
已知:①ZnSO4·7H2O晶体易溶于水,易风化。
②已知25℃常见离子沉淀的pH范围如下:
回答下列问题:
(1)下列操作或描述正确的是___ 。
A.加入试剂A目的是将Fe2+氧化为Fe3+
B.调节pH=5.3,可用试剂ZnO
C.操作②中用玻璃棒在过滤器上搅拌以加快过滤速度
D.为制备ZnSO4·7H2O,可蒸发ZnSO4溶液至有大量晶体析出,再停止加热,用余热蒸干
(2)调节pH=2的目的是___ 。
(3)写出滤液③中加入碳酸氢钠溶液生成沉淀④的反应的离子方程式___ 。
(4)为了得到纯净的沉淀③,需要将沉淀③进行洗涤。洗涤沉淀的具体操作是___ 。
(5)判断滤液②是否有铁元素残留的简要实验方案为___ 。

已知:①ZnSO4·7H2O晶体易溶于水,易风化。
②已知25℃常见离子沉淀的pH范围如下:
| 开始沉淀 | 完全沉淀 | |
| Fe3+ | 1.5 | 3.7 |
| Fe2+ | 6.5 | 9.7 |
| Al3+ | 3.3 | 5.2 |
| Zn2+ | 5.4 | 8.2 |
回答下列问题:
(1)下列操作或描述正确的是
A.加入试剂A目的是将Fe2+氧化为Fe3+
B.调节pH=5.3,可用试剂ZnO
C.操作②中用玻璃棒在过滤器上搅拌以加快过滤速度
D.为制备ZnSO4·7H2O,可蒸发ZnSO4溶液至有大量晶体析出,再停止加热,用余热蒸干
(2)调节pH=2的目的是
(3)写出滤液③中加入碳酸氢钠溶液生成沉淀④的反应的离子方程式
(4)为了得到纯净的沉淀③,需要将沉淀③进行洗涤。洗涤沉淀的具体操作是
(5)判断滤液②是否有铁元素残留的简要实验方案为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】铝土矿【主要成分为Al2O3,还含有SiO2(不溶于水和酸)、Fe2O3】是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:

(1)沉淀A、B的成分分别是__________ 、__________ ;步骤②中的试剂a是__________ ;(以上均填化学式)
(2)试写出步骤③中发生反应的离子方式__________ 、__________ ;

(1)沉淀A、B的成分分别是
(2)试写出步骤③中发生反应的离子方式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】已知铝土矿的主要成分是Al2O3,含有杂质SiO2(不溶于盐酸和水)、Fe2O3、MgO。工业上从铝土矿中提取铝可采用如下工艺流程:
请回答下列问题:
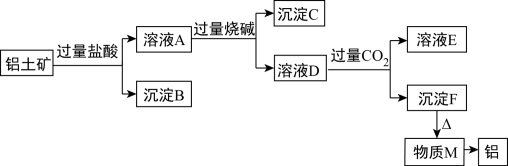
(1)溶液A转化为溶液D发生的离子方程式为________________________________ 。
(2)由物质M制取铝的化学方程式为________________________________________ 。
(3)溶液D中通入过量CO2生成沉淀F的离子方程式为________________________ 。
(4)沉淀C的成分是____________ ,逐滴向少量沉淀C中加入过量盐酸至沉淀全部溶解,此过程的实验现象为_______________________________________________ 。
请回答下列问题:

(1)溶液A转化为溶液D发生的离子方程式为
(2)由物质M制取铝的化学方程式为
(3)溶液D中通入过量CO2生成沉淀F的离子方程式为
(4)沉淀C的成分是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
Ⅰ.某学习小组研究 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
(1)取少量废液滴入KSCN溶液呈红色,则废液中含有的金属阳离子是_______ 。
(2)从 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:

滤渣C中所含物质的化学式为_______ ;通入F发生反应的离子方程式为_______ 。
Ⅱ.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
请回答:
(3)实验Ⅰ中湿棉花的作用是_______ ;实验Ⅰ中反应的化学方程式是_______ 。
(4)甲同学观察到实验Ⅰ中持续产生肥皂泡,若实验Ⅱ中溶液B呈现红色,说明溶液A一定中含有_______ 离子(用离子符号表示)。
(5)乙同学观察到实验Ⅰ中持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色,则溶液B未呈现红色的原因是_______ 。
Ⅰ.某学习小组研究
 腐蚀铜后所得的废液成分并回收铜,进行了如下实验:
腐蚀铜后所得的废液成分并回收铜,进行了如下实验:(1)取少量废液滴入KSCN溶液呈红色,则废液中含有的金属阳离子是
(2)从
 腐蚀铜后的废液中回收铜,并获得
腐蚀铜后的废液中回收铜,并获得 溶液,设计如下方案:
溶液,设计如下方案:
滤渣C中所含物质的化学式为
Ⅱ.学习小组同学继续研究铁与水蒸气的反应,分别进行了如图实验。
| 实验Ⅰ | 实验Ⅱ |
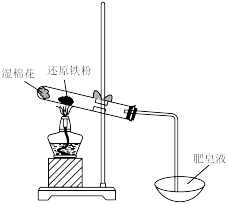 |  |
(3)实验Ⅰ中湿棉花的作用是
(4)甲同学观察到实验Ⅰ中持续产生肥皂泡,若实验Ⅱ中溶液B呈现红色,说明溶液A一定中含有
(5)乙同学观察到实验Ⅰ中持续产生肥皂泡,但实验Ⅱ中溶液B未呈现红色,则溶液B未呈现红色的原因是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】绿矾( )是治疗缺铁性贫血药品的重要成分。实验室模拟如下工艺流程,从主要含Fe、Cu、Al及其氧化物的废旧金属材料回收部分金属,同时制得绿矾。
)是治疗缺铁性贫血药品的重要成分。实验室模拟如下工艺流程,从主要含Fe、Cu、Al及其氧化物的废旧金属材料回收部分金属,同时制得绿矾。
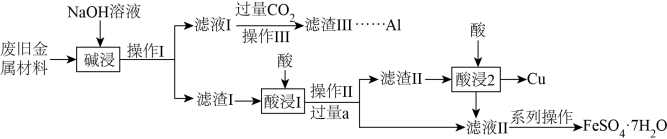
完成下列问题:
(1)碱浸时发生反应的物质有______ (填化学式)。
(2)操作Ⅱ的名称是______ ,用到的玻璃仪器有______ 。
(3)酸浸1和酸浸2用到的酸是______ (填名称,下同),向酸浸1后的溶液中加入过量的试剂a是______ 。
(4)由滤液Ⅱ制得绿矾需要经过一系列操作,主要包括______ 、______ 、过滤、洗涤、干燥。
(5)向滤液Ⅰ中通入过量的 会产生白色沉淀,该反应的化学方程式为
会产生白色沉淀,该反应的化学方程式为____________ 。
(6)已知 易被氧化,则
易被氧化,则 溶液与酸性
溶液与酸性 溶液反应的离子方程式为
溶液反应的离子方程式为____________ 。
 )是治疗缺铁性贫血药品的重要成分。实验室模拟如下工艺流程,从主要含Fe、Cu、Al及其氧化物的废旧金属材料回收部分金属,同时制得绿矾。
)是治疗缺铁性贫血药品的重要成分。实验室模拟如下工艺流程,从主要含Fe、Cu、Al及其氧化物的废旧金属材料回收部分金属,同时制得绿矾。
完成下列问题:
(1)碱浸时发生反应的物质有
(2)操作Ⅱ的名称是
(3)酸浸1和酸浸2用到的酸是
(4)由滤液Ⅱ制得绿矾需要经过一系列操作,主要包括
(5)向滤液Ⅰ中通入过量的
 会产生白色沉淀,该反应的化学方程式为
会产生白色沉淀,该反应的化学方程式为(6)已知
 易被氧化,则
易被氧化,则 溶液与酸性
溶液与酸性 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】三氯化铁在印刷、医药、颜料、污水处理以及有机合成催化剂方面有重要的应用。以硫铁矿(主要成分为FeS2,杂质不与盐酸反应)为原料制备三氯化铁晶体(FeC13•6H2O)的工艺流程如图所示:

回答下列问题:
(1)“焙烧”过程中,理论上1 molFeS2被氧化转移11 mol电子,则该反应的氧化产物为_____ 。
(2)“酸溶”不能用稀硫酸代替30%的盐酸,理由是_________ 。
(3)现有试剂:①稀盐酸②稀硫酸③稀硝酸④氯气⑤硫氰化钾溶液⑥高锰酸钾溶液⑦氢氧化钠溶液。为确认“酸溶”后的溶液中是否会含Fe2+,另取“焙烧”后的烧渣少许,用_______ (从上述试剂中选择,填标号)溶解,将所得溶液滴入_________ (从上述试剂中选择,填标号)中,若________ ,则说明“酸溶”后的溶液中含Fe2+。
(4)从FeCl3溶液中得到FeC13•6H2O的操作包括______ 、冷却结晶、过滤,该过程需保持盐酸过量,结合必要的离子方程式说明原因:____________ 。
(5)若以a吨硫铁矿为原料,最终制得b吨FeC13•6H2O,不计生产过程中的损失,则该硫铁矿中FeS2的含量为__________ (用含a、b的代数式表示)。

回答下列问题:
(1)“焙烧”过程中,理论上1 molFeS2被氧化转移11 mol电子,则该反应的氧化产物为
(2)“酸溶”不能用稀硫酸代替30%的盐酸,理由是
(3)现有试剂:①稀盐酸②稀硫酸③稀硝酸④氯气⑤硫氰化钾溶液⑥高锰酸钾溶液⑦氢氧化钠溶液。为确认“酸溶”后的溶液中是否会含Fe2+,另取“焙烧”后的烧渣少许,用
(4)从FeCl3溶液中得到FeC13•6H2O的操作包括
(5)若以a吨硫铁矿为原料,最终制得b吨FeC13•6H2O,不计生产过程中的损失,则该硫铁矿中FeS2的含量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】今有下列六组仪器:①牛角管 ②锥形瓶 ③温度计 ④冷凝管 ⑤已组装固定好的铁架台、酒精灯和蒸馏烧瓶(垫有石棉网) ⑥带附件的铁架台。现要进行酒精(沸点为78.5℃)和水混合物的分离实验,试回答下列问题:
(1)按仪器的安装先后顺序排列以上提供的各组仪器(填序号):____ →____ →____ →____ →____ →_____ 。
(2)冷凝管的两端有大口和小口之分,靠近大口的小弯管用于___ 冷却水,靠近小口的小弯管用于___ 冷却水(填“引入”或“流出”)。
(3)蒸馏时,温度计水银球应位于____ 。
(4)在蒸馏烧瓶中注入液体混合物后,加几片碎瓷片的目的是___ 。
(1)按仪器的安装先后顺序排列以上提供的各组仪器(填序号):
(2)冷凝管的两端有大口和小口之分,靠近大口的小弯管用于
(3)蒸馏时,温度计水银球应位于
(4)在蒸馏烧瓶中注入液体混合物后,加几片碎瓷片的目的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】现有下列仪器或装置,请回答下列问题
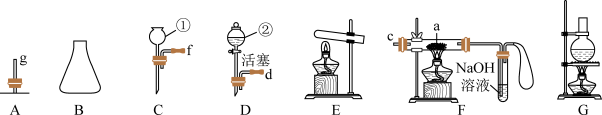
(1)仪器①的名称是_______ ,装置D中的仪器②可改成下图所示仪器,下图所示仪器的名称是_______ ,其优点是_______ 。

(2)用上图仪器组装成气体发生装置:用浓盐酸与MnO2制Cl2,并控制产生Cl2的速率,应选的装置是_______ (填字母),气体发生装置中进行的反应是_______ 。(用化学方程式表示)
(3)图为装置X,仅用装置X即可对气体发生装置中产生的氯气进行除杂、收集和尾气吸收。除杂时,氯气应从_______ (填“b”或“c”)端导入。吸收氯气所用的试剂为_______ ,尾气吸收时发生反应的化学方程式为_______ 。
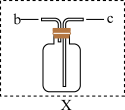
(4)若用F装置进行CO还原Fe2O3的实验,实验室制取CO的方法一般采取甲酸脱水法( ,甲酸沸点为100.6℃),用纯净的CO完成该实验。
,甲酸沸点为100.6℃),用纯净的CO完成该实验。
①除F、X外还需要的装置有_______ ,X中应加入的试剂是_______ ,X与其它导管连接的顺序是_______ (填导管口的序号);
②实验时,a处的可能的现象为_______ ;F装置中气球的作用是_______ 。

(1)仪器①的名称是

(2)用上图仪器组装成气体发生装置:用浓盐酸与MnO2制Cl2,并控制产生Cl2的速率,应选的装置是
(3)图为装置X,仅用装置X即可对气体发生装置中产生的氯气进行除杂、收集和尾气吸收。除杂时,氯气应从

(4)若用F装置进行CO还原Fe2O3的实验,实验室制取CO的方法一般采取甲酸脱水法(
 ,甲酸沸点为100.6℃),用纯净的CO完成该实验。
,甲酸沸点为100.6℃),用纯净的CO完成该实验。①除F、X外还需要的装置有
②实验时,a处的可能的现象为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】如下图所示是中学化学中常用于混合物分离和提纯的装置:
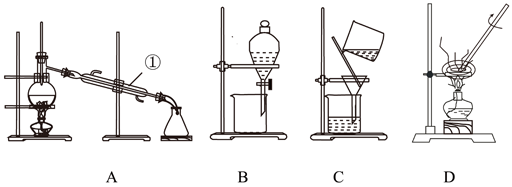
请根据装置图回答下列问题:
(1)从氯化钾溶液中得到氯化钾固体选择装置________ (填代表装置图的字母,下同);除去自来水中的Cl-等杂质得到蒸馏水,选择装置________ 。
(2)从碘水中分离出I2,选择装置________ ,该分离方法的名称为________ 。
(3)装置A中①的名称是________ ,冷凝水流动的方向是_________________________________________________________________ 。
(4)在用装置B进行操作时,为使液体顺利滴下,应进行的具体操作是_________________________________________________________________ 。
分液时要注意及时________ ,防止上层液体流下。分液后漏斗内剩余的液体从分液漏斗的________ (填“上口”或“下口”)倒入烧杯。

请根据装置图回答下列问题:
(1)从氯化钾溶液中得到氯化钾固体选择装置
(2)从碘水中分离出I2,选择装置
(3)装置A中①的名称是
(4)在用装置B进行操作时,为使液体顺利滴下,应进行的具体操作是
分液时要注意及时
您最近一年使用:0次



