自然界中的铝元素以化合物的形式存在于各种矿石中、某铝土矿的主要成分是 ,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
已知: 不溶于水且不与盐酸反应;
不溶于水且不与盐酸反应; 能与NaOH溶液反应,生成可溶性盐。
能与NaOH溶液反应,生成可溶性盐。

请回答下列问题。
(1)步骤①加盐酸前先将铝土矿粉碎的目的是_______ ;所得滤液A中的溶质有_______ 种。
(2)步骤②中所加NaOH溶液须过量的目的是___________ 。
(3)步骤③ 加热分解生成两种氧化物,请写出该反应的化学方程式
加热分解生成两种氧化物,请写出该反应的化学方程式___________ 。
(4)步骤④是通过电解熔融状态的 制备铝。
制备铝。 的熔点是
的熔点是 ,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义
,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义___________ 。
氧化亚铜( )可用于电镀工业。干法生产
)可用于电镀工业。干法生产 粉末的主要工艺流程如下:
粉末的主要工艺流程如下:

(5)粉碎机中,发生的变化属于___________ (填“物理变化”或“化学变化”)。
(6) 时,煅烧炉中发生化合反应,该反应的化学方程式为
时,煅烧炉中发生化合反应,该反应的化学方程式为___________ 。
 ,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):
,含少量SiO2、Fe2O3等杂质。从该铝土矿中提取铝可采用如下工艺流程(不考虑其它杂质参与反应):已知:
 不溶于水且不与盐酸反应;
不溶于水且不与盐酸反应; 能与NaOH溶液反应,生成可溶性盐。
能与NaOH溶液反应,生成可溶性盐。
请回答下列问题。
(1)步骤①加盐酸前先将铝土矿粉碎的目的是
(2)步骤②中所加NaOH溶液须过量的目的是
(3)步骤③
 加热分解生成两种氧化物,请写出该反应的化学方程式
加热分解生成两种氧化物,请写出该反应的化学方程式(4)步骤④是通过电解熔融状态的
 制备铝。
制备铝。 的熔点是
的熔点是 ,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义
,很难达到熔融状态,工业上通过加入冰晶石使其在1000℃左右熔化,请写出这一做法的意义氧化亚铜(
 )可用于电镀工业。干法生产
)可用于电镀工业。干法生产 粉末的主要工艺流程如下:
粉末的主要工艺流程如下:
(5)粉碎机中,发生的变化属于
(6)
 时,煅烧炉中发生化合反应,该反应的化学方程式为
时,煅烧炉中发生化合反应,该反应的化学方程式为
更新时间:2023-09-04 13:24:21
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
【推荐1】以明矾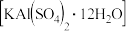 为原料制备Al、
为原料制备Al、 和
和 的工艺流程如下:
的工艺流程如下:
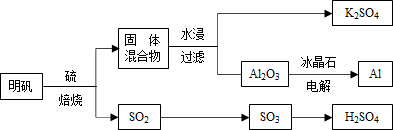
依据上述流程图回答下列问题:
(1)写出明矾和硫单质混合焙烧发生反应的化学方程式______ 。
(2)从水浸后的滤液中得到 晶体的方法是蒸发浓缩、
晶体的方法是蒸发浓缩、______ 、过滤,实验室在过滤过程中用到的玻璃仪器有______ 。
(3)电解 过程中作阳极的石墨易消耗,原因是
过程中作阳极的石墨易消耗,原因是______ 。
(4)以Al和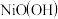 为电极,NaOH溶液为电解液组成一种新型电池,放电时
为电极,NaOH溶液为电解液组成一种新型电池,放电时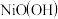 转化为
转化为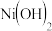 ,该电池反应的化学方程式是
,该电池反应的化学方程式是______ 。
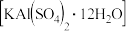 为原料制备Al、
为原料制备Al、 和
和 的工艺流程如下:
的工艺流程如下:
依据上述流程图回答下列问题:
(1)写出明矾和硫单质混合焙烧发生反应的化学方程式
(2)从水浸后的滤液中得到
 晶体的方法是蒸发浓缩、
晶体的方法是蒸发浓缩、(3)电解
 过程中作阳极的石墨易消耗,原因是
过程中作阳极的石墨易消耗,原因是(4)以Al和
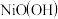 为电极,NaOH溶液为电解液组成一种新型电池,放电时
为电极,NaOH溶液为电解液组成一种新型电池,放电时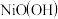 转化为
转化为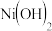 ,该电池反应的化学方程式是
,该电池反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】混合物A主要成分为Al2O3、SiO2、Fe2O3,对A进行如下图所示的实验操作:

(1)沉淀甲、沉淀乙分别是__________ 、__________ (写化学式)
(2)写出反应Ⅱ中所涉及的离子反应方程式__________

(1)沉淀甲、沉淀乙分别是
(2)写出反应Ⅱ中所涉及的离子反应方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】某磁铁矿石 的主要成分是磁性氧化铁
的主要成分是磁性氧化铁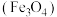 ,还含少量的
,还含少量的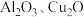 。某工厂利用此矿石进行有关物质的回收利用,其中
。某工厂利用此矿石进行有关物质的回收利用,其中 为常见的补铁剂,工艺流程如图(已知
为常见的补铁剂,工艺流程如图(已知 不溶于水和碱,但溶于强酸:
不溶于水和碱,但溶于强酸: )。根据流程回答下列问题:
)。根据流程回答下列问题: 的溶质主要是
的溶质主要是___________ ,铝离子的结构示意图为___________ 。
(2)溶液D与过量试剂 反应的离子方程式有
反应的离子方程式有___________ 。
(3)在溶液 中滴加
中滴加 溶液的现象是
溶液的现象是___________ 。
(4)㩰作1的名称为___________ 。
(5)写出检验溶液 中
中 原理的离子方程式:
原理的离子方程式:___________ 。
 的主要成分是磁性氧化铁
的主要成分是磁性氧化铁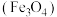 ,还含少量的
,还含少量的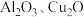 。某工厂利用此矿石进行有关物质的回收利用,其中
。某工厂利用此矿石进行有关物质的回收利用,其中 为常见的补铁剂,工艺流程如图(已知
为常见的补铁剂,工艺流程如图(已知 不溶于水和碱,但溶于强酸:
不溶于水和碱,但溶于强酸: )。根据流程回答下列问题:
)。根据流程回答下列问题:
 的溶质主要是
的溶质主要是(2)溶液D与过量试剂
 反应的离子方程式有
反应的离子方程式有(3)在溶液
 中滴加
中滴加 溶液的现象是
溶液的现象是(4)㩰作1的名称为
(5)写出检验溶液
 中
中 原理的离子方程式:
原理的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】某工厂用废铜铁合金制取生产油漆的颜料铁红(Fe2O3),并回收铜的流程如下:
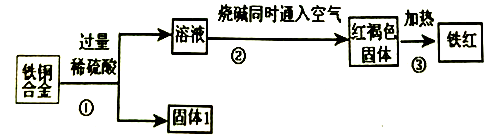
完成下列问题:
(1) 上述三个过程中发生了氧化还原反应的是____________ (填符号①②③)。
(2) 固体1的名称______ ;红褐色固体的化学式______ 。
(3) 写出整个②过程发生反应的离子方程式:______ ;______ ;______ 。

完成下列问题:
(1) 上述三个过程中发生了氧化还原反应的是
(2) 固体1的名称
(3) 写出整个②过程发生反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】某工厂生产废液中含有大量的Cu2+、Fe3+、Fe2+、SO 。某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾(FeSO4·7H2O):
。某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾(FeSO4·7H2O):
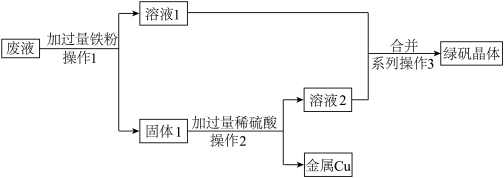
请回答以下问题:
(1)操作1和操作2的名称是________ 。
(2)废液中加过量铁时发生反应的离子方程式为__________ 、__________ 。
(3)若使用得到的绿矾晶体制备净水剂Fe2(SO4)3溶液,除在绿矾中加入适量稀硫酸外,还需要加入________ (填标号)。
①稀H2SO4②Cl2③H2O2④Fe粉
 。某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾(FeSO4·7H2O):
。某兴趣小组设计了以下方案,对废液加以综合利用获得了Cu和绿矾(FeSO4·7H2O):
请回答以下问题:
(1)操作1和操作2的名称是
(2)废液中加过量铁时发生反应的离子方程式为
(3)若使用得到的绿矾晶体制备净水剂Fe2(SO4)3溶液,除在绿矾中加入适量稀硫酸外,还需要加入
①稀H2SO4②Cl2③H2O2④Fe粉
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】CoC2O4是制备氧化钴和金属钴的原料。一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下:
(1)为了加快“碱浸”速率,可采用的方法有______ (写两种)。反应的主要化学方程式为______ 。
(2)“钴浸出”过程中加入Na2SO3的作用是______ 。
(3)“除杂1”过程中,在40~50℃加入H2O2,写出加入H2O2反应的主要离子方程式:______ 。
(4)“除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+ )=1.0×10-5mol/L,则滤液中c(Mg2+ )为______ [已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10]。
(5)萃取剂对金属离子的萃取率与pH的关系如图所示,经过萃取可除去Mn2+,则控制溶液的pH范围是______ (填字母)。

A.1.0~2.0 B.2.0~3.0 C.3.0~3.5

(1)为了加快“碱浸”速率,可采用的方法有
(2)“钴浸出”过程中加入Na2SO3的作用是
(3)“除杂1”过程中,在40~50℃加入H2O2,写出加入H2O2反应的主要离子方程式:
(4)“除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+ )=1.0×10-5mol/L,则滤液中c(Mg2+ )为
(5)萃取剂对金属离子的萃取率与pH的关系如图所示,经过萃取可除去Mn2+,则控制溶液的pH范围是

A.1.0~2.0 B.2.0~3.0 C.3.0~3.5
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】某工业废水中含有大量的Cu2+、Fe3+、Fe2+和 ,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
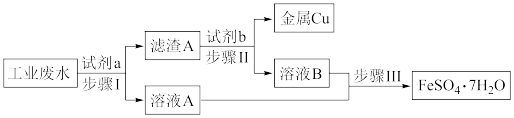
(1)下列叙述正确的是___________。
(2)步骤Ⅰ发生反应的离子方程式为Fe+Cu2+=Fe2++Cu和___________ 。
(3)取2mL溶液A于试管中,滴加少量NaOH溶液,观察到的实验现象是___________ 。
(4)获得的绿矾晶体(FeSO4·7H2O)可能有部分被氧化,请设计检验方案验证(操作、现象、结论)___________ 。
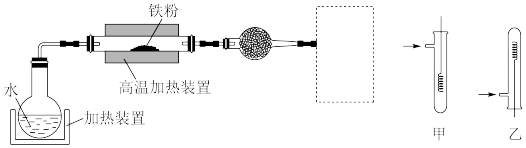
(5)已知:3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是
Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是___________ (填“甲”或“乙”)。
 ,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
,拟从该废水中回收金属铜并制得绿矾(FeSO4·7H2O),工艺流程如下图:
(1)下列叙述正确的是___________。
| A.滤渣A为Fe和Cu的混合物 |
| B.试剂b为盐酸 |
| C.步骤Ⅱ可以分离出Cu,并能得到FeSO4溶液 |
| D.步骤Ⅲ为蒸发溶液 |
(3)取2mL溶液A于试管中,滴加少量NaOH溶液,观察到的实验现象是
(4)获得的绿矾晶体(FeSO4·7H2O)可能有部分被氧化,请设计检验方案验证(操作、现象、结论)
(5)已知:3Fe(s)+4H2O(g)
 Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是
Fe3O4(s)+4H2(g)。虚线框处宜选择的装置是
您最近一年使用:0次





