混合物A主要成分为Al2O3、SiO2、Fe2O3,对A进行如下图所示的实验操作:

(1)沉淀甲、沉淀乙分别是__________ 、__________ (写化学式)
(2)写出反应Ⅱ中所涉及的离子反应方程式__________

(1)沉淀甲、沉淀乙分别是
(2)写出反应Ⅱ中所涉及的离子反应方程式
更新时间:2020-11-06 15:39:04
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
【推荐1】利用炼铝厂的废料—铝灰(含 、
、 及少量
及少量 和
和 、
、 )回收少量铝。有关工艺流程如下:
)回收少量铝。有关工艺流程如下:
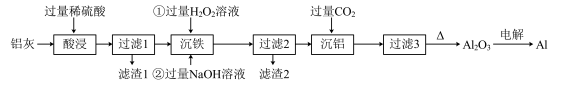
已知: 是酸性氧化物;
是酸性氧化物; 具有粘合性;
具有粘合性;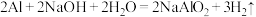
回答下列问题:
(1)“酸浸”操作后溶液中含有的阳离子为___________ (填离子符号)。
(2)滤渣1的主要成分是___________ (填化学式)。
(3)“沉铁”时加入过量 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为___________ 。
(4)“沉铁”时加入过量NaOH溶液的主要目的是沉淀铁,有同学提出在“酸浸”时将稀硫酸替换成为NaOH溶液,这样就无需进行“沉铁”操作,你认为先进行“酸浸”再进行“沉铁”的原因为___________ 。
(5)“沉铝”时发生反应的化学方程式为___________ 。
(6)工业通过电解的方法得到铝,通常在电解时会加入冰晶石,加入冰晶石的目的是___________ ;若回收1tAl,在电解 生产过程中Al的损失率为10%,则消耗的
生产过程中Al的损失率为10%,则消耗的 的质量为
的质量为___________ t(结果保留2位有效数字)。
 、
、 及少量
及少量 和
和 、
、 )回收少量铝。有关工艺流程如下:
)回收少量铝。有关工艺流程如下:
已知:
 是酸性氧化物;
是酸性氧化物; 具有粘合性;
具有粘合性;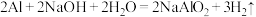
回答下列问题:
(1)“酸浸”操作后溶液中含有的阳离子为
(2)滤渣1的主要成分是
(3)“沉铁”时加入过量
 溶液时发生反应的离子方程式为
溶液时发生反应的离子方程式为(4)“沉铁”时加入过量NaOH溶液的主要目的是沉淀铁,有同学提出在“酸浸”时将稀硫酸替换成为NaOH溶液,这样就无需进行“沉铁”操作,你认为先进行“酸浸”再进行“沉铁”的原因为
(5)“沉铝”时发生反应的化学方程式为
(6)工业通过电解的方法得到铝,通常在电解时会加入冰晶石,加入冰晶石的目的是
 生产过程中Al的损失率为10%,则消耗的
生产过程中Al的损失率为10%,则消耗的 的质量为
的质量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】利用油脂厂废弃的镍( )催化剂(主要含有
)催化剂(主要含有 、
、 、
、 及少量
及少量 、
、 、
、 )制备
)制备 的工艺流程如下:
的工艺流程如下:

回答下列问题:
(1)为加快“碱浸”的速率可采取的措施是___________ (任写一条);“碱浸”中 的作用有:去除油脂、
的作用有:去除油脂、___________ 。
(2)“滤液2”中含金属阳离子,主要有:___________ 。
(3)①“转化”中反应的离子方程式是___________ 。
②“转化”中可替代 的最佳物质是
的最佳物质是___________ (填标号)。
a、 b、
b、 c、
c、
(4)某温度下, 分解得到铁、氧质量比为
分解得到铁、氧质量比为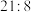 的氧化物,其化学式为
的氧化物,其化学式为___________ 。
 )催化剂(主要含有
)催化剂(主要含有 、
、 、
、 及少量
及少量 、
、 、
、 )制备
)制备 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)为加快“碱浸”的速率可采取的措施是
 的作用有:去除油脂、
的作用有:去除油脂、(2)“滤液2”中含金属阳离子,主要有:
(3)①“转化”中反应的离子方程式是
②“转化”中可替代
 的最佳物质是
的最佳物质是a、
 b、
b、 c、
c、
(4)某温度下,
 分解得到铁、氧质量比为
分解得到铁、氧质量比为 的氧化物,其化学式为
的氧化物,其化学式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】石墨在材料领域有重要应用。某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。设计的提纯与综合利用工艺如下:

(注:SiCl4的沸点为57.6 ℃,金属氯化物的沸点均高于150 ℃)
(1)向反应器中通入Cl2前,需通一段时间N2,主要目的是__________________ 。
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物。气体Ⅰ中的碳氧化物主要为________ 。由气体Ⅱ中某物质得到水玻璃的化学反应方程式为_____________________________________ 。
(3)步骤①为:搅拌、________ 。所得溶液Ⅳ中的阴离子有________________ 。
(4)100 kg初级石墨最多可获得Ⅴ的质量为________ kg。

(注:SiCl4的沸点为57.6 ℃,金属氯化物的沸点均高于150 ℃)
(1)向反应器中通入Cl2前,需通一段时间N2,主要目的是
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物。气体Ⅰ中的碳氧化物主要为
(3)步骤①为:搅拌、
(4)100 kg初级石墨最多可获得Ⅴ的质量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:
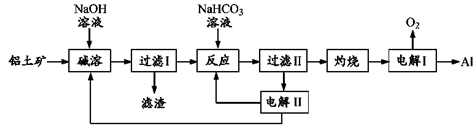
注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时的离子方程式为_____________________ 。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH_________ (填“增大”、“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融 Al2O3,电解过程中作阳极的石墨易消耗,原因是___________ 。
(4)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是_____________________ 。
(5)向“过滤Ⅰ”所得滤液中通入过量的CO2,其离子方程式为:_____________________

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时的离子方程式为
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH
(3)“电解Ⅰ”是电解熔融 Al2O3,电解过程中作阳极的石墨易消耗,原因是
(4)铝粉在1000℃时可与N2反应制备AlN。在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因是
(5)向“过滤Ⅰ”所得滤液中通入过量的CO2,其离子方程式为:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】按要求回答问题:
(一)以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质) 为原料制备铝的工艺流程如下:
为原料制备铝的工艺流程如下:

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时Al2O3发生反应的离子方程式________________ ;
(2)“过滤Ⅰ”所得滤液中加入NaHCO3溶液时发生反应的离子方程式__________ 。
(二)常温下,向Ba(OH)2和NaOH混合溶液中缓慢通入CO2至过量(溶液温度变化忽略不计),生成沉淀的物质的量与通入CO2体积的关系如图所示。

(3)ab段反应的离子方程式______________ ;b点的溶质为________ 。
(4)bc段反应的化学方程式____________ ;原混合物中n[Ba(OH)2] :n(NaOH)之比________ 。
(一)以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)
 为原料制备铝的工艺流程如下:
为原料制备铝的工艺流程如下:
注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时Al2O3发生反应的离子方程式
(2)“过滤Ⅰ”所得滤液中加入NaHCO3溶液时发生反应的离子方程式
(二)常温下,向Ba(OH)2和NaOH混合溶液中缓慢通入CO2至过量(溶液温度变化忽略不计),生成沉淀的物质的量与通入CO2体积的关系如图所示。

(3)ab段反应的离子方程式
(4)bc段反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】铝是应用广泛的金属,以铝土矿(主要成分为A12O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如图:

已知:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为___________ 。
(2)“滤渣Ⅰ”的成分有___________ 。
(3)向“过滤Ⅰ”所得滤液中通入足量的CO2,反应的离子方程式为___________ 。
(4)“滤液Ⅱ”中加入足量的CaO,生成的___________ (填化学式)可循环利用。
(5)“灼烧”的化学方程式为___________ 。

已知:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为
(2)“滤渣Ⅰ”的成分有
(3)向“过滤Ⅰ”所得滤液中通入足量的CO2,反应的离子方程式为
(4)“滤液Ⅱ”中加入足量的CaO,生成的
(5)“灼烧”的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】化学小组同学为研究氯气制备进行了如图实验。如图是实验室制取纯净、干燥氯气装置图。
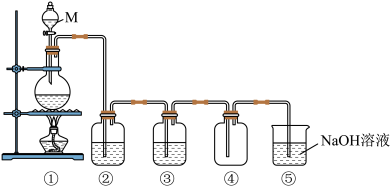
(1)M仪器的名称是_______ ,①中反应的反应的化学方程式是_______
(2)③中存放的试剂是_______
(3)⑤中反应的离子方程式是_______

(1)M仪器的名称是
(2)③中存放的试剂是
(3)⑤中反应的离子方程式是
您最近一年使用:0次
【推荐2】刚玉在工业上有广泛的用途.其主要成分为 氧化铝。利用铝灰(主要成分为
氧化铝。利用铝灰(主要成分为 ,含少量
,含少量 、
、 、
、 杂质),制备刚玉的工艺流程如图所示:
杂质),制备刚玉的工艺流程如图所示:
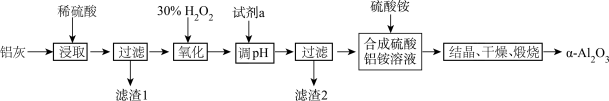
回答下列问题:
(1)“浸取”步骤中 发生反应的离子方程式为
发生反应的离子方程式为______________________________ 。
(2)滤渣1的主要成分为___________________ 。
(3)“氧化”步骤中发生反应的离子方程式为__________________________ ,此步骤需控制温度低于40℃的原因是____________________________________________ 。
(4)试剂a为_________________ 。
(5)已知:生成氢氧化物沉淀的pH如下表所示,则“调pH”的范围是________________ 。
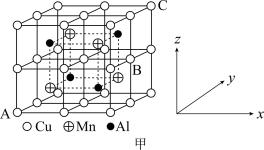
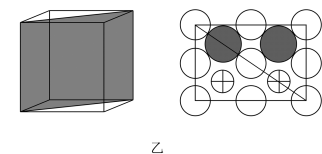
(6)Cu-Mn-Al合金的晶胞如图甲所示,该晶胞可视为Mn、Al位于Cu形成的立方体体心位置,图乙是沿立方格子对角面取得的截图。基态锰原子的价电子排布图为__________________ ,该晶体的化学式为_________ 。
 氧化铝。利用铝灰(主要成分为
氧化铝。利用铝灰(主要成分为 ,含少量
,含少量 、
、 、
、 杂质),制备刚玉的工艺流程如图所示:
杂质),制备刚玉的工艺流程如图所示:
回答下列问题:
(1)“浸取”步骤中
 发生反应的离子方程式为
发生反应的离子方程式为(2)滤渣1的主要成分为
(3)“氧化”步骤中发生反应的离子方程式为
(4)试剂a为
(5)已知:生成氢氧化物沉淀的pH如下表所示,则“调pH”的范围是
氢氧化物 |
|
|
|
开始沉淀时 | 3.4 | 6.3 | 1.5 |
完全沉淀时 | 4.7 | 8.3 | 2.8 |


您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】实验室要配制80 mlL1.00 mol/LNaCl溶液,实验室现有含有少量碳酸钠的氯化钠固体。
Ⅰ.为了除去氯化钠样品中的杂质,某兴趣小组最初设计了如下方案进行实验:

(1)沉淀A的化学式是_______________ 。
(2)在实验过程中,又发现了新的问题:此方案很容易引入新的杂质。则固体物质B的成分为_________________ (用化学式表示)。
(3)继续探究后又提出了新的方案:将混合物溶解,先滴加足量_________________ (填试剂名称),再蒸发结晶,有关反应的离子方程式为_______________________________ 。
Ⅱ.配制溶液:
(1)配制过程中需要使用的玻璃仪器除烧杯和玻璃棒外还有_________________ 。
(2)从所配溶液中取出10mL,与足量AgNO3溶液反应,经过滤、洗涤、干燥后得到白色沉淀1.50 g。则所配溶液的浓度________ 1.00 mol/L (填“>”、“<”或“=”),造成此误差的操作可能是_______________ 。
A.使用容量瓶前未干燥
B.用托盘天平称量氯化钠固体时将砝码错放在左盘
C.定容时俯视容量瓶的刻度线
D.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
Ⅰ.为了除去氯化钠样品中的杂质,某兴趣小组最初设计了如下方案进行实验:

(1)沉淀A的化学式是
(2)在实验过程中,又发现了新的问题:此方案很容易引入新的杂质。则固体物质B的成分为
(3)继续探究后又提出了新的方案:将混合物溶解,先滴加足量
Ⅱ.配制溶液:
(1)配制过程中需要使用的玻璃仪器除烧杯和玻璃棒外还有
(2)从所配溶液中取出10mL,与足量AgNO3溶液反应,经过滤、洗涤、干燥后得到白色沉淀1.50 g。则所配溶液的浓度
A.使用容量瓶前未干燥
B.用托盘天平称量氯化钠固体时将砝码错放在左盘
C.定容时俯视容量瓶的刻度线
D.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】海洋中无机氮的循环示意图(部分)如图表示:

回答下列问题:
(1)上述海洋中无机氮循环示意图所涉及物质中,常温常压下呈气态的物质除 和
和 外,还有
外,还有___________ 。
(2)根据图中信息, 的数值为
的数值为___________ 。
(3)海洋中的 一定条件下与游离态氧发生反应④,生成
一定条件下与游离态氧发生反应④,生成 和
和 的物质的量之比为
的物质的量之比为 ,同时海水酸性增强,写出该反应的离子方程式
,同时海水酸性增强,写出该反应的离子方程式___________
(4)某兴趣小组在实验室用如下图所示装置实现过程③的转化,完成 的制备、除杂、收集等操作。
的制备、除杂、收集等操作。

①装置A处发生反应的化学方程式为___________ ,仪器a的名称为___________ 。
②装置B是氨气的干燥装置,U型管中盛放的干燥剂可以为___________ (选填编号)。
a.五氧化二磷 b.生石灰 c.浓硫酸 d.无水氯化钙
③装置C虚线框中可选用下列___________ 装置进行氨气收集。
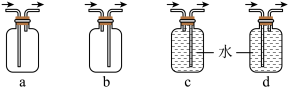

回答下列问题:
(1)上述海洋中无机氮循环示意图所涉及物质中,常温常压下呈气态的物质除
 和
和 外,还有
外,还有(2)根据图中信息,
 的数值为
的数值为(3)海洋中的
 一定条件下与游离态氧发生反应④,生成
一定条件下与游离态氧发生反应④,生成 和
和 的物质的量之比为
的物质的量之比为 ,同时海水酸性增强,写出该反应的离子方程式
,同时海水酸性增强,写出该反应的离子方程式(4)某兴趣小组在实验室用如下图所示装置实现过程③的转化,完成
 的制备、除杂、收集等操作。
的制备、除杂、收集等操作。
①装置A处发生反应的化学方程式为
②装置B是氨气的干燥装置,U型管中盛放的干燥剂可以为
a.五氧化二磷 b.生石灰 c.浓硫酸 d.无水氯化钙
③装置C虚线框中可选用下列

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
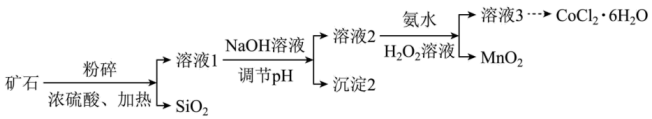
【推荐2】氯化钴(CoCl2)在工业催化、涂料工业、干湿指示剂等领域具有广泛应用。某钴矿石的主要成分包括CoO、MnO、Fe2O3和SiO2。由该矿石制CoCl2∙6H2O固体的方法如图(部分分离操作省略):
资料:Mn2+生成Mn(OH)2,开始沉淀时pH=8.2,完全沉淀时pH=10.2。
(1)上述矿石溶解过程中,能够加快化学反应速率的措施有_____ (写出一条即可)。
(2)CoO溶于浓硫酸是非氧化还原反应,溶液1中阳离子包括H+、Mn2+和_____ 。
(3)调节溶液的pH至2.8时,得到的沉淀2是_____ 。
(4)溶液2中含有Co2+和Mn2+。
ⅰ.已知:25℃时Ksp[Co(OH)2]≈1×10−15,当c(Co2+)≤1×10−5 mol∙L−1时可认为Co2+完全沉淀。若向溶液2中加入碱溶液,常温下,当pH=_____ 时,Co2+完全沉淀。由此可知,通过调节pH无法将Mn2+和Co2+完全分离。
ⅱ.溶液2中加入氨水和H2O2溶液,发生的反应为:_____ 。(完成离子方程式)
______Mn2++______H2O2+______NH3∙H2O=______+______NH +______
+______

资料:Mn2+生成Mn(OH)2,开始沉淀时pH=8.2,完全沉淀时pH=10.2。
(1)上述矿石溶解过程中,能够加快化学反应速率的措施有
(2)CoO溶于浓硫酸是非氧化还原反应,溶液1中阳离子包括H+、Mn2+和
(3)调节溶液的pH至2.8时,得到的沉淀2是
(4)溶液2中含有Co2+和Mn2+。
ⅰ.已知:25℃时Ksp[Co(OH)2]≈1×10−15,当c(Co2+)≤1×10−5 mol∙L−1时可认为Co2+完全沉淀。若向溶液2中加入碱溶液,常温下,当pH=
ⅱ.溶液2中加入氨水和H2O2溶液,发生的反应为:
______Mn2++______H2O2+______NH3∙H2O=______+______NH
 +______
+______
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】利用蛇纹石提镁后的中和渣(主要成分为 及:
及: 等杂质)提取高附加值的铁红
等杂质)提取高附加值的铁红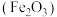 的一种工艺流程如下图所示.
的一种工艺流程如下图所示.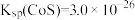 、
、
②溶液中离子浓度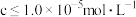 时可认为完全沉淀
时可认为完全沉淀
请回答下列问题:
(1)滤渣1的成分为______________ (填化学式),滤液2中主要的金属阳离子为______________ 。
(2)还原过程中发生反应的离子方程式为______________ ,可用试剂______________ 检验还原是否完全。
(3)欲制备高纯铁红,净化过程溶液中各离子的去除率与pH的关系如下图,则应控制pH为______________ 。 浓度均为
浓度均为 逐渐加入
逐渐加入 ,则先沉淀的离子为
,则先沉淀的离子为______________ ,结合计算说明两种离子能否彻底先后分离______________ 。
(5)煅烧过程中发生的化学方程式为______________ 。
(6)一种测定铁红产品纯度的方法如下:称取 铁红,溶于一定量的硫酸之中,配成
铁红,溶于一定量的硫酸之中,配成 溶液从其中量取
溶液从其中量取 溶液,加入过量的
溶液,加入过量的 ,充分反应后,用
,充分反应后,用 硫代硫酸钠
硫代硫酸钠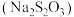 标准液滴定至终点,发生反应:
标准液滴定至终点,发生反应: .平行滴定三次,硫代硫酸钠平均消耗体积为
.平行滴定三次,硫代硫酸钠平均消耗体积为 .则铁红产品的纯度为
.则铁红产品的纯度为______________ (用c、V、m表示)。
 及:
及: 等杂质)提取高附加值的铁红
等杂质)提取高附加值的铁红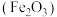 的一种工艺流程如下图所示.
的一种工艺流程如下图所示.
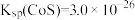 、
、
②溶液中离子浓度
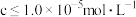 时可认为完全沉淀
时可认为完全沉淀请回答下列问题:
(1)滤渣1的成分为
(2)还原过程中发生反应的离子方程式为
(3)欲制备高纯铁红,净化过程溶液中各离子的去除率与pH的关系如下图,则应控制pH为

 浓度均为
浓度均为 逐渐加入
逐渐加入 ,则先沉淀的离子为
,则先沉淀的离子为(5)煅烧过程中发生的化学方程式为
(6)一种测定铁红产品纯度的方法如下:称取
 铁红,溶于一定量的硫酸之中,配成
铁红,溶于一定量的硫酸之中,配成 溶液从其中量取
溶液从其中量取 溶液,加入过量的
溶液,加入过量的 ,充分反应后,用
,充分反应后,用 硫代硫酸钠
硫代硫酸钠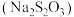 标准液滴定至终点,发生反应:
标准液滴定至终点,发生反应: .平行滴定三次,硫代硫酸钠平均消耗体积为
.平行滴定三次,硫代硫酸钠平均消耗体积为 .则铁红产品的纯度为
.则铁红产品的纯度为
您最近一年使用:0次





