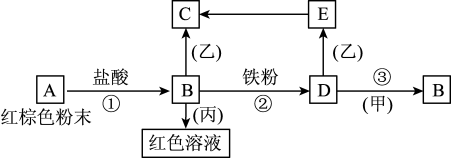
1 . 下列物质之间有如下反应关系:
(1)写出下列物质的化学式:
A___________ B___________ D___________ 甲___________ 乙___________ 丙___________ ;
(2)写出E→C反应的化学方程式:___________ ;
(3)写出B+丙反应的离子方程式:___________ 。
(1)写出下列物质的化学式:
A
(2)写出E→C反应的化学方程式:
(3)写出B+丙反应的离子方程式:
您最近半年使用:0次
解题方法
2 . 有NaCl、FeCl2、FeCl3、MgCl2、AlCl3五种溶液,用一种试剂就可把它们鉴别开来,这种试剂是
| A.盐酸 | B.烧碱溶液 | C.氨水 | D.KSCN溶液 |
您最近半年使用:0次
解题方法
3 . 下列说法中不正确的是
| A.赤铁矿的主要成分与铁锈的主要成分相同 |
| B.Fe3O4可由单质直接化合而得到 |
| C.FeCl2、FeCl3、Fe(OH)3都可通过化合反应生成 |
| D.某溶液中滴加氯水,然后滴加KSCN溶液,溶液显红色,该溶液中一定含有Fe2+ |
您最近半年使用:0次
4 . 下列有关物质检验方法不合理的是
| A.向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含有Fe2+ |
| B.用酸性KMnO4溶液检验Fe2(SO4)3溶液中是否含有FeSO4 |
| C.检验绿矾晶体是否已氧化变质,可将绿矾晶体溶于稀H2SO4后滴加KSCN溶液,再观察溶液是否变红 |
D.向某溶液中加入适量BaCl2溶液,产生白色沉淀,说明溶液中含有 |
您最近半年使用:0次
解题方法
5 . 下列离子方程式正确的是
A.钠与水反应: |
B. 溶液和过量澄清石灰水混合: 溶液和过量澄清石灰水混合: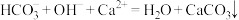 |
C.氯化铁溶液与碘化钾溶液反应: |
D.氯化镁溶液与氨水反应: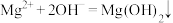 |
您最近半年使用:0次
6 . 下列实验设计不能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 证明氧化性Cl2>Br2>I2 | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 |
| B | 比较水和乙醇中氢的活泼性 | 分别将少量钠投入到盛有水和乙醇的烧杯中 |
| C | 检验溶液中FeSO4是否被氧化 | 取少量待测液,滴加KSCN溶液,观察溶液颜色变化 |
| D | 工业酒精制备无水乙醇 | 工业酒精中加生石灰,蒸馏 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
7 . 为除去括号内的杂质,所选用的试剂或方法正确的是
A. (HCl):通过饱和碳酸氢钠溶液的洗气瓶 (HCl):通过饱和碳酸氢钠溶液的洗气瓶 |
B. 溶液( 溶液( ):加入足量的铁粉,过滤 ):加入足量的铁粉,过滤 |
C. 溶液( 溶液( ): ): 溶液,过滤 溶液,过滤 |
D. 溶液( 溶液( ):加入过量 ):加入过量 溶液 溶液 |
您最近半年使用:0次
解题方法
8 . 某化学实验室产生的废液中含有 、
、 、
、 三种金属离子,实验室设计如图所示方案对废液进行处理,以回收金属并制得氧化铁,保护环境。
三种金属离子,实验室设计如图所示方案对废液进行处理,以回收金属并制得氧化铁,保护环境。
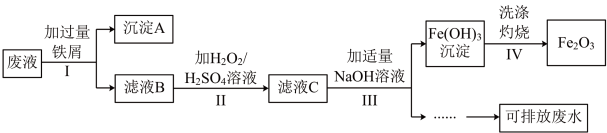
回答下列问题:
(1)步骤Ⅰ中分离沉淀A和滤液B的操作是_____ ,在实验室进行该操作时需要的玻璃仪器有_____ 。
(2)沉淀A中含有的金属单质是铁、_____ (填名称)。
(3)步骤Ⅱ中加入 溶液目的是
溶液目的是_____ (用离子方程式表示)。
(4)请检验步骤Ⅲ中 是否沉淀完全
是否沉淀完全_____
(5)“可排放废水”中含有的主要离子是_____ (填离子符号)。
 、
、 、
、 三种金属离子,实验室设计如图所示方案对废液进行处理,以回收金属并制得氧化铁,保护环境。
三种金属离子,实验室设计如图所示方案对废液进行处理,以回收金属并制得氧化铁,保护环境。
回答下列问题:
(1)步骤Ⅰ中分离沉淀A和滤液B的操作是
(2)沉淀A中含有的金属单质是铁、
(3)步骤Ⅱ中加入
 溶液目的是
溶液目的是(4)请检验步骤Ⅲ中
 是否沉淀完全
是否沉淀完全(5)“可排放废水”中含有的主要离子是
您最近半年使用:0次
9 . 某同学利用如图所示装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
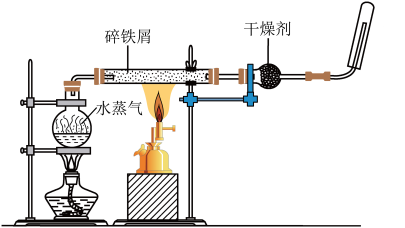
(1)试管中发生反应的化学方程式为___________ 。
(2)该同学欲确定反应一段时间后试管中固体物质的成分,设计了如下方案:
①待试管冷却,取其中固体少许溶于稀盐酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红,则试管中固体是___________ (只有一个选项符合题意),若溶液未变红,则试管中固体是___________ (只有一个选项符合题意)。
A.一定有Fe3O4,可能有Fe
B.只有Fe(OH)3
C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有Fe
E.只有Fe3O4
(3)该同学按上述方案进行了实验,溶液未变红色,该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关反应的化学方程式___________ 。
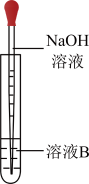
(4)一段时间后,该同学发现(2)中未变红的溶液变成红色。由此可知,实验室FeCl2溶液需现用现配的原因是___________ ,并且配制时应加入少量___________ 。

(1)试管中发生反应的化学方程式为
(2)该同学欲确定反应一段时间后试管中固体物质的成分,设计了如下方案:
①待试管冷却,取其中固体少许溶于稀盐酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红,则试管中固体是
A.一定有Fe3O4,可能有Fe
B.只有Fe(OH)3
C.一定有Fe3O4和Fe
D.一定有Fe(OH)3,可能有Fe
E.只有Fe3O4
(3)该同学按上述方案进行了实验,溶液未变红色,该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述现象相关反应的化学方程式

(4)一段时间后,该同学发现(2)中未变红的溶液变成红色。由此可知,实验室FeCl2溶液需现用现配的原因是
您最近半年使用:0次
解题方法
10 . 下列实验设计不能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 检验溶液中FeSO4是否被氧化 | 取少量待测液,滴加KSCN溶液,观察溶液颜色变化 |
| B | 净化实验室制备的Cl2 | 气体依次通过盛有饱和NaCl溶液、浓H2SO4的洗气瓶 |
| C | 测定NaOH溶液的pH | 将待测液滴在湿润的pH试纸上,与标准比色卡对照 |
| D | 验证Br2的氧化性比12强 | 将少量溴水加入KI溶液中,再加入几滴淀粉溶,振荡,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



