名校
1 . 铁及其化合物是重要的化学物质,如天然磁石中含有较多的Fe3O4、三水合草酸合铁(Ⅲ)酸钾{K3[Fe(C2O4)3]·3H2O,呈绿色,可溶于水,难溶于乙醇,见光易分解}常用于化学光量计、绿矾(FeSO4·7H2O)是常用的还原剂。回答下列问题:
(1)电子工业中,常用氯化铁溶液腐蚀铜制造印刷电路板,该原理的离子方程式为_____ 。
(2)根据化合价及元素的性质,Na2S5可以改写为Na2S·4S、Fe3O4可以改写为FeO·Fe2O3,则Fe3Cl8可以改写为_____ 、Fe3I8可以改写为_____ 。
(3)可通过下列两个步骤制备三水合草酸合铁(Ⅲ)酸钾晶体。
步骤i:向盛有3.00g黄色晶体FeC2O4·2H2O的烧杯中,加入10.00mLK2C2O4溶液,加热至40℃左右,缓慢滴入过量的H2O2,一段时间后,出现红褐色沉淀。
步骤ii:加热至沸腾,分两次缓慢加入8.00~9.00mLH2C2O4溶液,至沉淀溶解,得到绿色溶液。加热浓缩、加入无水乙醇、结晶,抽滤干燥得7.860g三水合草酸合铁(III)酸钾晶体。
①步骤ⅰ中,生成三草酸合铁酸钾与另一种铁的化合物,该化合物为_____ (填化学式)。
②步骤ⅱ加入无水乙醇的目的是_____ 。
③实验小组完成实验后发现产率偏低,其主要原因可能是_____ 。
(4)8.34gFeSO4·7H2O(Mr=278)样品隔绝空气受热分解生成多种化合物过程的热重曲线(残留样品质量随温度变化的曲线)如图所示。
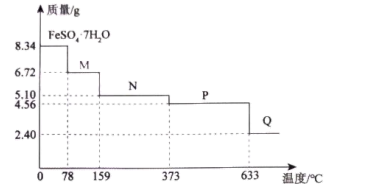
①温度为100℃时,固体物质M的化学式为_____ 。
②在隔绝空气的条件下,由P得到Q的化学方程式为_____ 。
(1)电子工业中,常用氯化铁溶液腐蚀铜制造印刷电路板,该原理的离子方程式为
(2)根据化合价及元素的性质,Na2S5可以改写为Na2S·4S、Fe3O4可以改写为FeO·Fe2O3,则Fe3Cl8可以改写为
(3)可通过下列两个步骤制备三水合草酸合铁(Ⅲ)酸钾晶体。
步骤i:向盛有3.00g黄色晶体FeC2O4·2H2O的烧杯中,加入10.00mLK2C2O4溶液,加热至40℃左右,缓慢滴入过量的H2O2,一段时间后,出现红褐色沉淀。
步骤ii:加热至沸腾,分两次缓慢加入8.00~9.00mLH2C2O4溶液,至沉淀溶解,得到绿色溶液。加热浓缩、加入无水乙醇、结晶,抽滤干燥得7.860g三水合草酸合铁(III)酸钾晶体。
①步骤ⅰ中,生成三草酸合铁酸钾与另一种铁的化合物,该化合物为
②步骤ⅱ加入无水乙醇的目的是
③实验小组完成实验后发现产率偏低,其主要原因可能是
(4)8.34gFeSO4·7H2O(Mr=278)样品隔绝空气受热分解生成多种化合物过程的热重曲线(残留样品质量随温度变化的曲线)如图所示。

①温度为100℃时,固体物质M的化学式为
②在隔绝空气的条件下,由P得到Q的化学方程式为
您最近一年使用:0次
2 . 下列实验操作和现象、结论或目的均正确的是
| 选项 | 操作和现象 | 结论或目的 |
| A | 向 溶液中加入适量铜粉,铜粉溶解,溶液变蓝 溶液中加入适量铜粉,铜粉溶解,溶液变蓝 | Fe比Cu活泼 |
| B | 在过硫化钠(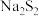 )溶液中加入稀盐酸,产生淡黄色沉淀和臭鸡蛋气味的气体 )溶液中加入稀盐酸,产生淡黄色沉淀和臭鸡蛋气味的气体 | 发生歧化反应: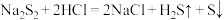 |
| C | 取少量 试样加水溶解,加稀 试样加水溶解,加稀 酸化后,滴加KSCN溶液,溶液变为红色 酸化后,滴加KSCN溶液,溶液变为红色 | 该 试样已经变质 试样已经变质 |
| D | 向某溶液中通入 ,然后再加入KSCN溶液,变红色 ,然后再加入KSCN溶液,变红色 | 原溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-23更新
|
81次组卷
|
4卷引用:T9-实验方案的设计与评价
(已下线)T9-实验方案的设计与评价甘肃省永昌县第一高级中学2023-2024学年高三上学期期中考试化学试题(已下线)选择题6-10贵州省顶效开发区顶兴学校2023-2024学年高三第三次月考化学试题
解题方法
3 . 为将某部分被氧化的废铜屑[主要含Cu、CuO、 ]转化为铜单质,同时制备绿矾(
]转化为铜单质,同时制备绿矾( ),某实验小组设计如图所示流程.
),某实验小组设计如图所示流程.

回答下列问题:
(1)“浸泡”时,Cu发生反应的离子方程式为______ , 的作用为
的作用为______ .
(2)“滤液1”中所含溶质的主要成分为______ .
(3)“分铜”时的操作名称是______ .
(4)“滤液2”容易被空气中的氧气氧化,长时间保存“滤液2”时需向其中加入一定量______ .
(5)向“滤液2”中滴加NaOH溶液,观察到的实验现象为______ ;发生反应的化学方程式为______ 和______ .
 ]转化为铜单质,同时制备绿矾(
]转化为铜单质,同时制备绿矾( ),某实验小组设计如图所示流程.
),某实验小组设计如图所示流程.
回答下列问题:
(1)“浸泡”时,Cu发生反应的离子方程式为
 的作用为
的作用为(2)“滤液1”中所含溶质的主要成分为
(3)“分铜”时的操作名称是
(4)“滤液2”容易被空气中的氧气氧化,长时间保存“滤液2”时需向其中加入一定量
(5)向“滤液2”中滴加NaOH溶液,观察到的实验现象为
您最近一年使用:0次
2023-12-22更新
|
119次组卷
|
2卷引用:河南省(驻马店)青桐鸣联考2023-2024学年高一上学期12月月考化学试题
解题方法
4 . 下列实验操作、现象及结论均正确的是
选项 | 实验操作及现象 | 结论 |
A | 向待测液中滴入 | 原溶液中一定不含 |
B | 向待测液中滴入过量稀盐酸,再滴入 | 原溶液中一定含 |
C | 向盛有酸性高锰酸钾溶液的试管中滴加浓盐酸,有大量黄绿色气体产生 | 酸性条件下,氧化性: |
D | 先向硫酸亚铁溶液中加入少量 | 原硫酸亚铁溶液已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-22更新
|
110次组卷
|
2卷引用:河南省(驻马店)青桐鸣联考2023-2024学年高一上学期12月月考化学试题
解题方法
5 . 在无色酸性溶液中能大量存在的离子组是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
2023-12-22更新
|
85次组卷
|
2卷引用:河南省(驻马店)青桐鸣联考2023-2024学年高一上学期12月月考化学试题
名校
6 . “价类”二维图是学习元素及其化合物的重要工具,如图所示是铁及其化合物的“价类”二维图。
(1)X、Y分别代表___________ 、___________ ;Z在空气中转化为W的化学方程式为___________ 。
(2)某小组研究 性质,预测
性质,预测 能与
能与___________ 发生氧化还原反应(填序号)。
① 溶液 ②氯水 ③稀盐酸 ④酸性
溶液 ②氯水 ③稀盐酸 ④酸性 溶液 ⑤镁 ⑥碳酸钠
溶液 ⑤镁 ⑥碳酸钠
(3)铁盐溶液可用于金属刻蚀。如用 溶液刻蚀铜制电路板,该反应的离子方程式为
溶液刻蚀铜制电路板,该反应的离子方程式为___________ 。
(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、___________ ,然后将少许滤液加入试管中,加入少量 ,再滴加几滴
,再滴加几滴 溶液,振荡,若观察到
溶液,振荡,若观察到___________ 现象,说明试验样品中含有铁元素。
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用 氧化
氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用双线桥法表示该反应的电子转移方向和数目
,用双线桥法表示该反应的电子转移方向和数目___________ 。
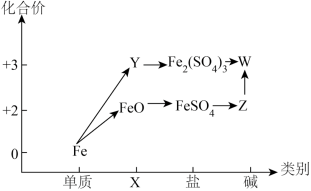
(1)X、Y分别代表
(2)某小组研究
 性质,预测
性质,预测 能与
能与①
 溶液 ②氯水 ③稀盐酸 ④酸性
溶液 ②氯水 ③稀盐酸 ④酸性 溶液 ⑤镁 ⑥碳酸钠
溶液 ⑤镁 ⑥碳酸钠(3)铁盐溶液可用于金属刻蚀。如用
 溶液刻蚀铜制电路板,该反应的离子方程式为
溶液刻蚀铜制电路板,该反应的离子方程式为(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、
 ,再滴加几滴
,再滴加几滴 溶液,振荡,若观察到
溶液,振荡,若观察到(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用
 氧化
氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用双线桥法表示该反应的电子转移方向和数目
,用双线桥法表示该反应的电子转移方向和数目
您最近一年使用:0次
2023-12-15更新
|
276次组卷
|
2卷引用:河南省洛阳偃师中成外国语学校2023-2024学年高一上学期12月月考化学试卷
名校
解题方法
7 . 硫酸亚铁晶体 在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
(1)向操作①的滤液中滴加 溶液后变为红色,则该滤液中含有
溶液后变为红色,则该滤液中含有_______ (填离子符号)。
(2)操作②中反应的离子方程式:_______ 。
(3)操作③中反应的离子方程式:_______ 。
(4)操作④中系列操作的步骤:过滤、_______ 、_______ 、灼烧、冷却至室温、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为_______ g(用含a的代数式表示)。
 在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下: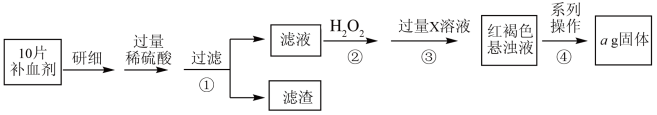
(1)向操作①的滤液中滴加
 溶液后变为红色,则该滤液中含有
溶液后变为红色,则该滤液中含有(2)操作②中反应的离子方程式:
(3)操作③中反应的离子方程式:
(4)操作④中系列操作的步骤:过滤、
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为
您最近一年使用:0次
2023-12-14更新
|
158次组卷
|
2卷引用:河南省洛阳偃师中成外国语学校2023-2024学年高一上学期12月月考化学试卷
名校
解题方法
8 . 根据实验操作及现象,下列结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向 溶液中滴加KSCN溶液,溶液变红,再加入少量KCl固体,溶液颜色无明显变化 溶液中滴加KSCN溶液,溶液变红,再加入少量KCl固体,溶液颜色无明显变化 |  与 与 的反应不可逆 的反应不可逆 |
| B | 两支试管各盛 酸性高锰酸钾溶液,分别加入 酸性高锰酸钾溶液,分别加入 草酸溶液和 草酸溶液和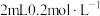 草酸溶液,观察溶液颜色变化 草酸溶液,观察溶液颜色变化 | 其他条件相同,反应物浓度越大,反应速率越快 |
| C | 加热足量的锌与少量浓硫酸的混合物,有大量气体产生 | 气体一定为 |
| D | 向2mL浓度均为 的KCl、KI混合溶液中滴加2滴 的KCl、KI混合溶液中滴加2滴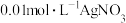 溶液,振荡,产生黄色沉淀 溶液,振荡,产生黄色沉淀 | 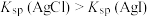 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 下列关于离子检验的说法正确的是
A.取少量样液,加入 溶液,若溶液变红,证明样液中含 溶液,若溶液变红,证明样液中含 |
B.取少量样液,加入硝酸酸化的 溶液,若产生白色沉淀,证明样液中含 溶液,若产生白色沉淀,证明样液中含 |
C.取少量样液,加入稀盐酸,若产生能使澄清石灰水变浑浊的气体,证明样液中含 |
D.用洁净的铂丝蘸取样液,在酒精灯外焰上灼烧,若火焰呈黄色,证明样液中含 ,不含 ,不含 |
您最近一年使用:0次
2023-12-06更新
|
426次组卷
|
5卷引用:河南省郑州市宇华实验学校2023-2024学年高一下学期3月月考化学试题
河南省郑州市宇华实验学校2023-2024学年高一下学期3月月考化学试题辽宁省丹东市2023-2024学年高一上学期期中教学质量调研测试化学试题(已下线)巩固测试卷02-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)甘肃省天水市第一中学2023-2024学年高一下学期开学化学试题江西省上饶市万年县第一中学2023-2024学年高一上学期第二次月考化学试题
10 . 磷酸亚铁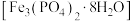 是生产锂电池的原料,能溶于强酸,不溶于水。实验室可以绿矾
是生产锂电池的原料,能溶于强酸,不溶于水。实验室可以绿矾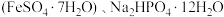 及
及 为原料制备磷酸亚铁,主要反应为
为原料制备磷酸亚铁,主要反应为 。
。
I.配制 溶液
溶液
(1)实验室常用绿矾配制 溶液,配制过程中需要用到的玻璃仪器除烧杯、量筒、容量瓶外,还有
溶液,配制过程中需要用到的玻璃仪器除烧杯、量筒、容量瓶外,还有___________ 。若实验需要配制。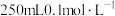 的
的 溶液,则需要称取的绿矾的质量为
溶液,则需要称取的绿矾的质量为___________ g。
Ⅱ.提纯制备晶体
(2)利用工业品十二水合磷酸氢二钠(含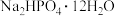 、重金属盐及有色杂质等)提纯得到
、重金属盐及有色杂质等)提纯得到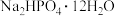 晶体。已知:
晶体。已知: 溶液
溶液 在
在 ,重金属硫化物不溶于水。请将实验步骤补充完整:
,重金属硫化物不溶于水。请将实验步骤补充完整:
将工业品溶于热水;
①___________ ;
②___________ ;
③___________ ;
冷却结晶,过滤、洗涤及干燥。
(实验中可选用的试剂: 溶液、
溶液、 溶液、
溶液、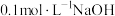 溶液、活性炭)
溶液、活性炭)
Ⅲ.合成磷酸亚铁及杂质的检验
(3)在三颈烧瓶中先加入抗坏血酸(维生素C)稀溶液作底液,然后向烧瓶中滴入 与
与 的混合溶液至
的混合溶液至 时,再滴入
时,再滴入 溶液,最终维持
溶液,最终维持 。
。
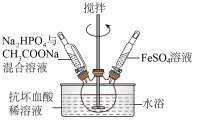
①用抗坏血酸稀溶液作底液的作用是___________ 。
②检验产品中是否混有 或
或 杂质的操作方法是
杂质的操作方法是___________ 。
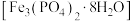 是生产锂电池的原料,能溶于强酸,不溶于水。实验室可以绿矾
是生产锂电池的原料,能溶于强酸,不溶于水。实验室可以绿矾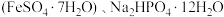 及
及 为原料制备磷酸亚铁,主要反应为
为原料制备磷酸亚铁,主要反应为 。
。I.配制
 溶液
溶液(1)实验室常用绿矾配制
 溶液,配制过程中需要用到的玻璃仪器除烧杯、量筒、容量瓶外,还有
溶液,配制过程中需要用到的玻璃仪器除烧杯、量筒、容量瓶外,还有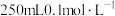 的
的 溶液,则需要称取的绿矾的质量为
溶液,则需要称取的绿矾的质量为Ⅱ.提纯制备晶体
(2)利用工业品十二水合磷酸氢二钠(含
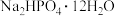 、重金属盐及有色杂质等)提纯得到
、重金属盐及有色杂质等)提纯得到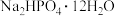 晶体。已知:
晶体。已知: 溶液
溶液 在
在 ,重金属硫化物不溶于水。请将实验步骤补充完整:
,重金属硫化物不溶于水。请将实验步骤补充完整:将工业品溶于热水;
①
②
③
冷却结晶,过滤、洗涤及干燥。
(实验中可选用的试剂:
 溶液、
溶液、 溶液、
溶液、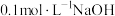 溶液、活性炭)
溶液、活性炭)Ⅲ.合成磷酸亚铁及杂质的检验
(3)在三颈烧瓶中先加入抗坏血酸(维生素C)稀溶液作底液,然后向烧瓶中滴入
 与
与 的混合溶液至
的混合溶液至 时,再滴入
时,再滴入 溶液,最终维持
溶液,最终维持 。
。
①用抗坏血酸稀溶液作底液的作用是
②检验产品中是否混有
 或
或 杂质的操作方法是
杂质的操作方法是
您最近一年使用:0次
2023-12-01更新
|
509次组卷
|
4卷引用:2024届河南省新乡市高三第一次模拟考试理科综合试题
2024届河南省新乡市高三第一次模拟考试理科综合试题河北省邯郸市六校联考2023-2024学年高二上学期11月月考化学试题陕西省西安市2023-2024学年高三上学期12月联考化学试卷(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)

 溶液,产生白色沉淀,再滴加稀盐酸,沉淀完全溶解
溶液,产生白色沉淀,再滴加稀盐酸,沉淀完全溶解


