名校
1 . 实验室由炼钢污泥(简称铁泥,主要成分为铁的氧化物)制备软磁性材料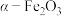 。其主要实验流程如下:
。其主要实验流程如下:
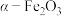 。其主要实验流程如下:
。其主要实验流程如下:
| A.酸浸:用一定浓度的硫酸浸取铁泥,能提高铁元素浸出率的措施有适当升高温度,加快搅拌速度 |
B.还原:向“酸浸”后的滤液中加入过量铁粉,可用KSCN溶液检验 是否完全还原 是否完全还原 |
C.沉铁:将提纯后的 溶液与氨水 溶液与氨水 混合溶液反应,生成 混合溶液反应,生成 沉淀的离子方程式为 沉淀的离子方程式为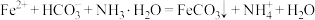 |
D.沉铁步骤中为防止生成 ,应在搅拌下向氨水 ,应在搅拌下向氨水 混合溶液中缓慢加入 混合溶液中缓慢加入 溶液 溶液 |
您最近一年使用:0次
2024-02-29更新
|
565次组卷
|
5卷引用:2024届河南省焦作市博爱县第一中学高三下学期二模化学试题
名校
解题方法
2 . 利用钴铁矿(主要成分 ,还有
,还有 等杂质)为原料,通过硫酸法制备钛白粉(主要成分
等杂质)为原料,通过硫酸法制备钛白粉(主要成分 )的工艺流程如图所示,下列有关说法错误的是
)的工艺流程如图所示,下列有关说法错误的是
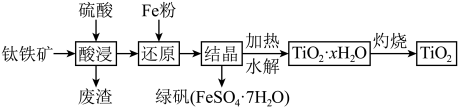
已知:“酸浸”后钛主要以 形式存在。
形式存在。
 ,还有
,还有 等杂质)为原料,通过硫酸法制备钛白粉(主要成分
等杂质)为原料,通过硫酸法制备钛白粉(主要成分 )的工艺流程如图所示,下列有关说法错误的是
)的工艺流程如图所示,下列有关说法错误的是
已知:“酸浸”后钛主要以
 形式存在。
形式存在。A.“酸浸”时主要反应的离子方程式为 |
B.检验还原反应是否完全可以选择 溶液 溶液 |
| C.结晶操作为蒸发结晶 |
D.在实验室灼烧 需要在坩埚中完成 需要在坩埚中完成 |
您最近一年使用:0次
2024-02-29更新
|
295次组卷
|
3卷引用:河南省郑州市宇华实验学校2023-2024学年高三下学期开学化学试题
名校
解题方法
3 . 硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。某实验小组模拟工业制备硫氰化钾的方法,设计实验如图:
I.制备NH4SCN溶液
(1)装置A用于制备NH3,圆底烧瓶内的固体a是_______ (填名称)。
(2)三颈烧瓶内盛放有CS2、水和固体催化剂,发生反应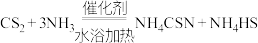 。实验开始时,打开K2和K1,水浴加热装置B,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是
。实验开始时,打开K2和K1,水浴加热装置B,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是_______ 。
(3)一段时间后,当观察到三颈烧瓶内_______ 时,停止通入气体,反应完成。
II.制备KSCN溶液
(4)关闭K1,将三颈烧瓶继续加热至100℃,待NH4HS完全分解后,再打开K3,继续保持水浴温度为100℃,缓缓滴入稍过量的KOH溶液,制得KSCN溶液。发生反应的化学方程式为_______ ;酸性K2Cr2O7溶液除可以吸收NH3外,还能将H2S气体氧化成硫酸,其离子方程式为_______ 。
III.制备KSCN晶体
(5)先除去三颈烧瓶中的固体催化剂,再通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。该提取过程中一定不用的仪器有_______ (填序号)。
①坩埚②蒸发皿③分液漏斗④玻璃棒⑤烧杯
(6)测定晶体中KSCN的含量:称取5.0g样品,配成500mL溶液。量取25.00mL溶液加入锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,达到滴定终点,三次滴定平均消耗AgNO3标准溶液21.00mL。
①滴定时发生的反应: ,则指示剂的化学式为
,则指示剂的化学式为_______ (填序号)。
A. B.
B.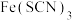 C.
C. D.
D.
②晶体中KSCN的质量分数为_______ (计算结果保留三位有效数字)。

I.制备NH4SCN溶液
(1)装置A用于制备NH3,圆底烧瓶内的固体a是
(2)三颈烧瓶内盛放有CS2、水和固体催化剂,发生反应
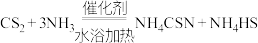 。实验开始时,打开K2和K1,水浴加热装置B,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是
。实验开始时,打开K2和K1,水浴加热装置B,反应发生。三颈烧瓶左侧导管口必须插入CS2中,其目的是(3)一段时间后,当观察到三颈烧瓶内
II.制备KSCN溶液
(4)关闭K1,将三颈烧瓶继续加热至100℃,待NH4HS完全分解后,再打开K3,继续保持水浴温度为100℃,缓缓滴入稍过量的KOH溶液,制得KSCN溶液。发生反应的化学方程式为
III.制备KSCN晶体
(5)先除去三颈烧瓶中的固体催化剂,再通过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。该提取过程中一定不用的仪器有
①坩埚②蒸发皿③分液漏斗④玻璃棒⑤烧杯
(6)测定晶体中KSCN的含量:称取5.0g样品,配成500mL溶液。量取25.00mL溶液加入锥形瓶中,加入适量稀硝酸,再加入几滴铁盐溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,达到滴定终点,三次滴定平均消耗AgNO3标准溶液21.00mL。
①滴定时发生的反应:
 ,则指示剂的化学式为
,则指示剂的化学式为A.
 B.
B.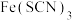 C.
C. D.
D.
②晶体中KSCN的质量分数为
您最近一年使用:0次
2024-02-29更新
|
86次组卷
|
2卷引用:河南省信阳高级中学2023-2024学年高三上学期2月月考理综试题-高中化学
4 . 1.Ⅰ.铁是使用最广泛的金属。我国目前发现最早的人工冶铁制品是河南三门峡出土的西周晚期的玉柄铁剑。
(1)在铁器制造中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理。用化学方程式解释其原因为__________________ 。
1.(2)检验 溶液蚀覆铜板后混合溶液中是否存在
溶液蚀覆铜板后混合溶液中是否存在 ,最好选择下列试剂中的
,最好选择下列试剂中的________ (填编号,下同)进行检验,现象和结论是__________________ 。
A. KSCN溶液 B. 酸性 溶液 C. 新制氯水 D. NaOH溶液
溶液 C. 新制氯水 D. NaOH溶液
(2)高铁酸钠( )是一种新型净水剂,遇酸会发生分解反应。其一种制备原理如下:
)是一种新型净水剂,遇酸会发生分解反应。其一种制备原理如下:
______ ______
______ ______=______
______=______ ______
______ ______
______
补充完整并配平后的离子方程式为__________________ 。
Ⅱ.氯是一种重要的成盐元素,氯的单质氯气是一种重要的化工原料。实验室利用下图所示装置制取并收集氯气。回答有关问题。
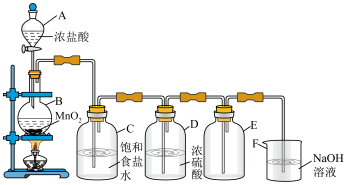
(3)装置A的名称是______ 。装置C的作用是__________________ 。
(4)该实验中收集氯气的方法叫做______ 。氯气还可以用排______ 溶液的方法收集。
(5)制备时装置B中发生反应的化学方程式为____________ ,F装置中发生反应的离子方程式为____________ 。
(1)在铁器制造中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理。用化学方程式解释其原因为
1.(2)检验
 溶液蚀覆铜板后混合溶液中是否存在
溶液蚀覆铜板后混合溶液中是否存在 ,最好选择下列试剂中的
,最好选择下列试剂中的A. KSCN溶液 B. 酸性
 溶液 C. 新制氯水 D. NaOH溶液
溶液 C. 新制氯水 D. NaOH溶液(2)高铁酸钠(
 )是一种新型净水剂,遇酸会发生分解反应。其一种制备原理如下:
)是一种新型净水剂,遇酸会发生分解反应。其一种制备原理如下:______
 ______
______ ______=______
______=______ ______
______ ______
______
补充完整并配平后的离子方程式为
Ⅱ.氯是一种重要的成盐元素,氯的单质氯气是一种重要的化工原料。实验室利用下图所示装置制取并收集氯气。回答有关问题。

(3)装置A的名称是
(4)该实验中收集氯气的方法叫做
(5)制备时装置B中发生反应的化学方程式为
您最近一年使用:0次
解题方法
5 . 下列实验操作、现象和结论都正确且有相关性的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向Na2SiO3溶液中加入醋酸 | 产生白色沉淀 | 非金属性:C>Si |
| B | 在溴水中滴加适量植物油(无色) | 橙色溶液变无色,液体分层 | 植物油含有不饱和碳碳键 |
| C | 测定饱和的碳酸和亚硫酸溶液的pH值 | 亚硫酸溶液的pH较小 | 酸性:H2SO3>H2CO3 |
| D | 检验铁钉表面的铁锈是不是含有Fe3+,先加盐酸溶解,再滴加KSCN溶液 | 溶液未变红色 | 铁锈中不含Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 某变质的废铜屑主要成分为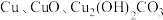 (其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
(其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是

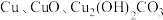 (其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
(其他杂质不参加化学反应),为将其转化为铜单质,同时制备绿矾,某实验小组设计如图所示流程。下列说法错误的是
A.基态铜原子的价层电子排布式为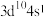 |
B.滤液1的溶质主要成分为 |
C.若分铜过程生成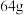 铜,则浸泡过程理论上有 铜,则浸泡过程理论上有 电子转移 电子转移 |
D.可用铁氰化钾溶液检验滤液2中 的存在 的存在 |
您最近一年使用:0次
7 . 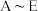 是中学常见的5种化合物,
是中学常见的5种化合物, 是氧化物,它们之间的转化关系如下图所示。则下列说法正确的是
是氧化物,它们之间的转化关系如下图所示。则下列说法正确的是
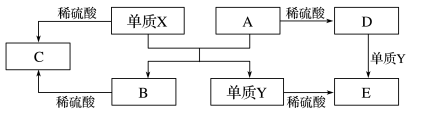
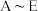 是中学常见的5种化合物,
是中学常见的5种化合物, 是氧化物,它们之间的转化关系如下图所示。则下列说法正确的是
是氧化物,它们之间的转化关系如下图所示。则下列说法正确的是
A. 与 与 反应的化学方程式是: 反应的化学方程式是: |
B.检验 溶液中的金属阳离子的反应: 溶液中的金属阳离子的反应: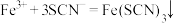 |
C.单质 在一定条件下能与水发生置换反应 在一定条件下能与水发生置换反应 |
| D.化合物C既能与酸反应,又能与碱反应,所以是两性化合物 |
您最近一年使用:0次
8 . 绿矾( )是治疗缺铁性贫血药品的重要成分。实验室模拟如下工艺流程,从主要含Fe、Cu、Al及其氧化物的废旧金属材料回收部分金属,同时制得绿矾。
)是治疗缺铁性贫血药品的重要成分。实验室模拟如下工艺流程,从主要含Fe、Cu、Al及其氧化物的废旧金属材料回收部分金属,同时制得绿矾。
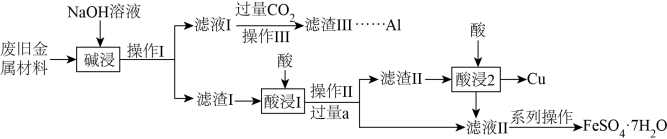
完成下列问题:
(1)碱浸时发生反应的物质有______ (填化学式)。
(2)操作Ⅱ的名称是______ ,用到的玻璃仪器有______ 。
(3)酸浸1和酸浸2用到的酸是______ (填名称,下同),向酸浸1后的溶液中加入过量的试剂a是______ 。
(4)由滤液Ⅱ制得绿矾需要经过一系列操作,主要包括______ 、______ 、过滤、洗涤、干燥。
(5)向滤液Ⅰ中通入过量的 会产生白色沉淀,该反应的化学方程式为
会产生白色沉淀,该反应的化学方程式为____________ 。
(6)已知 易被氧化,则
易被氧化,则 溶液与酸性
溶液与酸性 溶液反应的离子方程式为
溶液反应的离子方程式为____________ 。
 )是治疗缺铁性贫血药品的重要成分。实验室模拟如下工艺流程,从主要含Fe、Cu、Al及其氧化物的废旧金属材料回收部分金属,同时制得绿矾。
)是治疗缺铁性贫血药品的重要成分。实验室模拟如下工艺流程,从主要含Fe、Cu、Al及其氧化物的废旧金属材料回收部分金属,同时制得绿矾。
完成下列问题:
(1)碱浸时发生反应的物质有
(2)操作Ⅱ的名称是
(3)酸浸1和酸浸2用到的酸是
(4)由滤液Ⅱ制得绿矾需要经过一系列操作,主要包括
(5)向滤液Ⅰ中通入过量的
 会产生白色沉淀,该反应的化学方程式为
会产生白色沉淀,该反应的化学方程式为(6)已知
 易被氧化,则
易被氧化,则 溶液与酸性
溶液与酸性 溶液反应的离子方程式为
溶液反应的离子方程式为
您最近一年使用:0次
9 . 实验室中模拟工业上制取少量无水氯化铁的装置及操作如下。
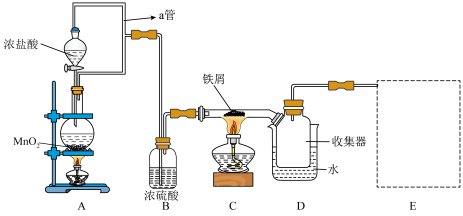
已知:无水 遇水剧烈反应,加热易升华。请回答下列问题:
遇水剧烈反应,加热易升华。请回答下列问题:
(1)反应后产物中常含有 杂质,仔细研究发现原来实验装置设计存在缺陷,需对装置进行改进的措施是
杂质,仔细研究发现原来实验装置设计存在缺陷,需对装置进行改进的措施是__________________ 。
(2)a管的作用是__________________ 。
(3)装置C中硬质玻璃管内的实验现象为____________ 。
(4)下列有关说法正确的是______(填字母)。
(5)某小组实验结束后,取硬质玻璃管中的固体适量,用一定浓度的盐酸溶解,再滴入KSCN溶液,没有出现血红色,说明该固体中没有+3价的铁。他判断结论是否正确,并说明理由:__________________ 。
(6)取含有 的
的 样品一定量溶于水中,选用铁氰化钾溶液(电离方程式:
样品一定量溶于水中,选用铁氰化钾溶液(电离方程式: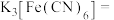
 )检验
)检验 的存在,
的存在, 和
和 在溶液中能发生复分解反应生成特征蓝色沉淀,则对应的离子方程式为
在溶液中能发生复分解反应生成特征蓝色沉淀,则对应的离子方程式为____________ ;又测得样品中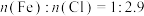 ,则该样品中
,则该样品中 的物质的量分数为
的物质的量分数为______ 。

已知:无水
 遇水剧烈反应,加热易升华。请回答下列问题:
遇水剧烈反应,加热易升华。请回答下列问题:(1)反应后产物中常含有
 杂质,仔细研究发现原来实验装置设计存在缺陷,需对装置进行改进的措施是
杂质,仔细研究发现原来实验装置设计存在缺陷,需对装置进行改进的措施是(2)a管的作用是
(3)装置C中硬质玻璃管内的实验现象为
(4)下列有关说法正确的是______(填字母)。
| A.实验开始前,应先在装置内装好所需药品,再检查装置气密性 |
| B.两处酒精灯加热的顺序为先加热A处,再加热C处 |
C.装置D中的水可用冷水或冰水,目的是更好地冷凝收集 |
D.E处虚线框内的装置可选用或 或 或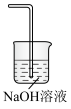 |
(5)某小组实验结束后,取硬质玻璃管中的固体适量,用一定浓度的盐酸溶解,再滴入KSCN溶液,没有出现血红色,说明该固体中没有+3价的铁。他判断结论是否正确,并说明理由:
(6)取含有
 的
的 样品一定量溶于水中,选用铁氰化钾溶液(电离方程式:
样品一定量溶于水中,选用铁氰化钾溶液(电离方程式: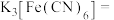
 )检验
)检验 的存在,
的存在, 和
和 在溶液中能发生复分解反应生成特征蓝色沉淀,则对应的离子方程式为
在溶液中能发生复分解反应生成特征蓝色沉淀,则对应的离子方程式为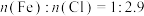 ,则该样品中
,则该样品中 的物质的量分数为
的物质的量分数为
您最近一年使用:0次
解题方法
10 . 下列实验方案中,不能达到实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 将新鲜菠菜剪碎、研磨、溶解、过滤,向滤液中加入少量稀硝酸,再滴加几滴KSCN溶液,观察现象 | 检验菠菜中是否含有铁元素 |
| B | 将干燥的氯气通入红色的鲜花中,观察现象 | 检验 的漂白性 的漂白性 |
| C | 用洁净铂丝蘸取待测液放在酒精灯外焰上灼烧,透过蓝色钴玻璃观察 | 检验是否有钾元素 |
| D | 取氯化镁和氯化铝溶液于两支试管,分别向其中加入过量的氢氧化钠溶液,观察现象 | 检验镁的金属性强于铝 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



