名校
1 . 下列各组离子一定能大量共存的是
A.0.1 mol⋅L  溶液: 溶液: 、 、 、 、 、 、 |
B.能与Al反应产生 的溶液: 的溶液: 、 、 、 、 、 、 |
C.使石蕊变红的溶液中: 、 、 、 、 、 、 |
D.常温下 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
2 . 根据实验操作现象得出的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 用铂丝蘸取少量某溶液进行焰色试验,有黄色火焰,透过蓝色钴玻璃显紫色 | 该溶液中一定含有钠盐和钾盐 |
| B | 向某溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色 | 溶液中一定含有 |
| C | 在包裹有 粉末的脱脂棉上滴几滴水,脱脂棉就能燃烧 粉末的脱脂棉上滴几滴水,脱脂棉就能燃烧 | 证明 与 与 反应是放热反应 反应是放热反应 |
| D | 将有色鲜花放入盛有干燥氯气的集气瓶中,鲜花颜色逐渐褪去 | 氯气具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。
Ⅰ.下图为钠及其化合物的“价-类”二维图,请回答下列问题:
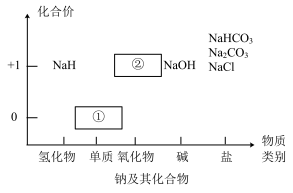
(1)物质①与水反应的离子方程式为___________ ,通常把物质①保存在___________ 中。
(2)写出淡黄色固体②与二氧化碳反应的化学方程式:___________ 。
(3)下列关于 和
和 的说法不正确的是___________。
的说法不正确的是___________。
Ⅱ.下图为铁及其化合物的“价-类”二维图,箭头表示部分物质间的转化关系。
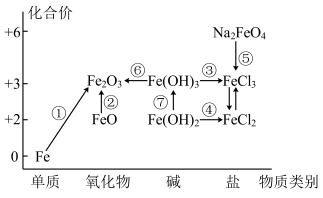
请回答以下问题:
(4)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:___________ 。
(5)已知 在强碱溶液中稳定存在,pH越小稳定性越差,则制备
在强碱溶液中稳定存在,pH越小稳定性越差,则制备 需在
需在___________ (填“酸性”“碱性”或“中性”)环境中进行; 也可以作为净水剂,能与水反应生成具有吸附性的
也可以作为净水剂,能与水反应生成具有吸附性的 胶体,且有氧气放出,写出其中离子方程式:
胶体,且有氧气放出,写出其中离子方程式:___________ 。其中检验溶液中 的试剂是
的试剂是___________ 。
Ⅰ.下图为钠及其化合物的“价-类”二维图,请回答下列问题:

(1)物质①与水反应的离子方程式为
(2)写出淡黄色固体②与二氧化碳反应的化学方程式:
(3)下列关于
 和
和 的说法不正确的是___________。
的说法不正确的是___________。A.相同条件下的溶解度: |
B.可以用澄清石灰水区别 溶液和 溶液和 溶液 溶液 |
C.可以用加热的方法除去 固体中的 固体中的 杂质 杂质 |
D.相同物质的量浓度下, 溶液的碱性比 溶液的碱性比 溶液的强 溶液的强 |
Ⅱ.下图为铁及其化合物的“价-类”二维图,箭头表示部分物质间的转化关系。

请回答以下问题:
(4)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(5)已知
 在强碱溶液中稳定存在,pH越小稳定性越差,则制备
在强碱溶液中稳定存在,pH越小稳定性越差,则制备 需在
需在 也可以作为净水剂,能与水反应生成具有吸附性的
也可以作为净水剂,能与水反应生成具有吸附性的 胶体,且有氧气放出,写出其中离子方程式:
胶体,且有氧气放出,写出其中离子方程式: 的试剂是
的试剂是
您最近一年使用:0次
4 . 等体积的0.3mol/L的FeCl3溶液和0.4mol/L的NaI溶液混合,能证明溶液中存在化学平衡“ ”的试剂,除了淀粉溶液外,还需要用到下列中的
”的试剂,除了淀粉溶液外,还需要用到下列中的
 ”的试剂,除了淀粉溶液外,还需要用到下列中的
”的试剂,除了淀粉溶液外,还需要用到下列中的| A.KSCN溶液 | B.AgNO3溶液 | C.Na2SO4溶液 | D.BaCl2溶液 |
您最近一年使用:0次
解题方法
5 . 元素的“价一类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图象。如图为铁元素的“价一类”二维图,箭头表示部分物质间的转化关系,下列说法正确的是
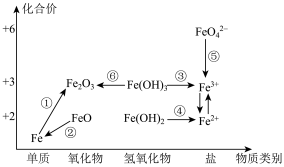

A. 、 、 均可通过化合反应制备 均可通过化合反应制备 |
B.可将 溶液加入浓碱液中制得 溶液加入浓碱液中制得 胶体 胶体 |
C. 溶液中 溶液中 、 、 、 、 、 、 可以大量共存 可以大量共存 |
D.可以用酸性高锰酸钾溶液检验 溶液中是否含有 溶液中是否含有 |
您最近一年使用:0次
6 . 下列除杂试剂或方法不正确的是
| 选项 | 被提纯物质 | 杂质 | 除杂试剂或方法 |
| A |  溶液 溶液 |  | 通入适量 |
| B |  溶液 溶液 |  | 加入过量铁粉并过滤 |
| C |  |  | 加入过量 溶液并过滤 溶液并过滤 |
| D |  |  | 通入饱和 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 在含有Fe3+、Cu2+、Cl-、H+的混合溶液中加入铁粉,充分反应后,溶液中所剩余的固体可被磁铁吸引。此时溶液中存在较多的阳离子是:
| A.Fe3+ | B.Fe2+ | C.Cu2+ | D.H+ |
您最近一年使用:0次
名校
8 . 用含铬不锈钢废渣(含 、
、 、
、 、
、 等)制取
等)制取 (铬绿)工艺流程如图所示:
(铬绿)工艺流程如图所示:
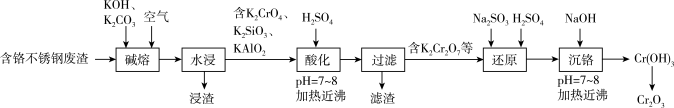
回答下列问题:
(1)“碱熔”时,为使废渣充分氧化可采取的措施是_____ (写一条)。
(2) 、KOH、
、KOH、 反应生成
反应生成 的化学方程式为
的化学方程式为_____ 。
(3)“水浸”时,碱熔渣中的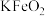 强烈水解生成的难溶物为
强烈水解生成的难溶物为_____ (填化学式);为检验“水浸”后的滤液中是否含有 ,可选用的化学试剂是
,可选用的化学试剂是_____ 。
(4)常温下,“酸化”时pH不宜过低(酸性太强)的原因是_____ 。
(5)“还原”时发生反应的离子方程式为_____ 。
(6)由 制取铬绿的方法是
制取铬绿的方法是_____ 。
 、
、 、
、 、
、 等)制取
等)制取 (铬绿)工艺流程如图所示:
(铬绿)工艺流程如图所示:
回答下列问题:
(1)“碱熔”时,为使废渣充分氧化可采取的措施是
(2)
 、KOH、
、KOH、 反应生成
反应生成 的化学方程式为
的化学方程式为(3)“水浸”时,碱熔渣中的
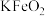 强烈水解生成的难溶物为
强烈水解生成的难溶物为 ,可选用的化学试剂是
,可选用的化学试剂是(4)常温下,“酸化”时pH不宜过低(酸性太强)的原因是
(5)“还原”时发生反应的离子方程式为
(6)由
 制取铬绿的方法是
制取铬绿的方法是
您最近一年使用:0次
2023-06-07更新
|
129次组卷
|
2卷引用:广东省东莞市东华高级中学2022-2023学年高一下学期3月月考化学试题
名校
9 . 下列各组离子一定能大量共存的是
A.在澄清透明强酸性溶液中: 、 、 、Fe2+、 、Fe2+、 、 、 |
B.在含大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.在强酸性溶液中: 、 、 、 、 、 、 |
D.在强碱性溶液中: 、 、 、 、 、 、 、Fe3+ 、Fe3+ |
您最近一年使用:0次
名校
解题方法
10 . 以硫铁矿(主要成分为FeS2,还有少量CuS、SiO2等杂质)为原料制备绿矾晶体FeSO4•7H2O的工艺流程如图:
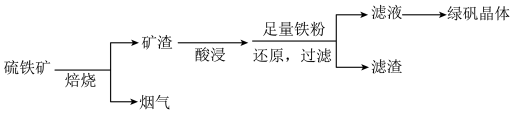
(1)焙烧时黄铁矿要粉碎,其目的是______ 。
(2)由滤液得到绿矾晶体的操作是______ 、______ 、过滤、洗涤、干燥。
(3)烟气中的SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式______ 。
(4)铁粉还原过滤,滤渣中除了铁和铜外还有的成分是______ (写化学式)。
(5)燃料细菌脱硫法是用氧化亚铁硫杆菌对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:

已知总反应为:FeS2+14Fe3++8H2O=2SO +15Fe2++16H+。写出过程Ⅱ反应的离子方程式
+15Fe2++16H+。写出过程Ⅱ反应的离子方程式______ 。
(6)绿矾晶体在空气中易被氧化变质。取xg样品,加水完全溶解,滴加硫酸酸化的amol/LK2Cr2O7溶液至恰好完全反应,消耗K2Cr2O7溶液bmL。反应原理:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为
+14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为______ 。

(1)焙烧时黄铁矿要粉碎,其目的是
(2)由滤液得到绿矾晶体的操作是
(3)烟气中的SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式
(4)铁粉还原过滤,滤渣中除了铁和铜外还有的成分是
(5)燃料细菌脱硫法是用氧化亚铁硫杆菌对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:

已知总反应为:FeS2+14Fe3++8H2O=2SO
 +15Fe2++16H+。写出过程Ⅱ反应的离子方程式
+15Fe2++16H+。写出过程Ⅱ反应的离子方程式(6)绿矾晶体在空气中易被氧化变质。取xg样品,加水完全溶解,滴加硫酸酸化的amol/LK2Cr2O7溶液至恰好完全反应,消耗K2Cr2O7溶液bmL。反应原理:6Fe2++Cr2O
 +14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为
+14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为
您最近一年使用:0次



