1 . 某化学活动小组用如图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。已知:[ ]熔点为306℃,沸点为315℃,易吸水而变质。工业上采用向500~600℃的Fe粉中通入
]熔点为306℃,沸点为315℃,易吸水而变质。工业上采用向500~600℃的Fe粉中通入 来生产无水氯化铁。[
来生产无水氯化铁。[ ]熔点为670℃,易升华。工业上采用向炽热Fe粉中通入HCl来生产无水
]熔点为670℃,易升华。工业上采用向炽热Fe粉中通入HCl来生产无水 。请回答下列问题:
。请回答下列问题:
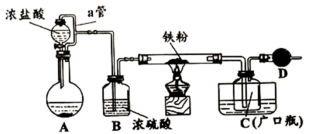
(1)在装置A中装浓盐酸的玻璃仪器名称______ 。
(2)D中装的药品是碱石灰,其作用是______ 。
(3)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。现检验产物中是否含有 ,可用下列试剂中的
,可用下列试剂中的______ (只能选取一种试剂,填序号)进行检验;若含有 ,预期实验现象为
,预期实验现象为______ 。
① 溶液 ②新制氯水 ③KSCN溶液 ④酸性
溶液 ②新制氯水 ③KSCN溶液 ④酸性 溶液
溶液
(4)定量分析。取装置C中的产物,按下列步骤进行实验:①称取4.60g产品溶于过量的稀盐酸;②加入足量 溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀至恒重;⑤称量所得红棕色固体为2.40g。回答下列问题:
溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀至恒重;⑤称量所得红棕色固体为2.40g。回答下列问题:
①用离子方程式表示步骤②的目的______ ;
②步骤④灼烧沉淀的化学方程式是______ 。
③该样品中铁元素的质量分数为______ (结果精确到小数点后两位)。
(5)针对(4)定量分析数据得出的结论,提出改进措施。
①用题目所给的装置制得的产物(不含单质铁)中,铁元素含量______ (填“相等”、“偏高”或“偏低”),说明含有 杂质。
杂质。
②若要得到较纯净的无水氯化铁,上述“装置”的改进措施是______ 。
 ]熔点为306℃,沸点为315℃,易吸水而变质。工业上采用向500~600℃的Fe粉中通入
]熔点为306℃,沸点为315℃,易吸水而变质。工业上采用向500~600℃的Fe粉中通入 来生产无水氯化铁。[
来生产无水氯化铁。[ ]熔点为670℃,易升华。工业上采用向炽热Fe粉中通入HCl来生产无水
]熔点为670℃,易升华。工业上采用向炽热Fe粉中通入HCl来生产无水 。请回答下列问题:
。请回答下列问题:
(1)在装置A中装浓盐酸的玻璃仪器名称
(2)D中装的药品是碱石灰,其作用是
(3)定性分析。取装置C中的少量产物溶于稀硫酸中配成稀溶液待用。现检验产物中是否含有
 ,可用下列试剂中的
,可用下列试剂中的 ,预期实验现象为
,预期实验现象为①
 溶液 ②新制氯水 ③KSCN溶液 ④酸性
溶液 ②新制氯水 ③KSCN溶液 ④酸性 溶液
溶液(4)定量分析。取装置C中的产物,按下列步骤进行实验:①称取4.60g产品溶于过量的稀盐酸;②加入足量
 溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀至恒重;⑤称量所得红棕色固体为2.40g。回答下列问题:
溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀至恒重;⑤称量所得红棕色固体为2.40g。回答下列问题:①用离子方程式表示步骤②的目的
②步骤④灼烧沉淀的化学方程式是
③该样品中铁元素的质量分数为
(5)针对(4)定量分析数据得出的结论,提出改进措施。
①用题目所给的装置制得的产物(不含单质铁)中,铁元素含量
 杂质。
杂质。②若要得到较纯净的无水氯化铁,上述“装置”的改进措施是
您最近一年使用:0次
名校
2 . 某磁铁矿石A的主要成分是磁性氧化铁(Fe3O4),还含少量的Al2O3、CuO。某工厂利用此矿石回收单质铜和绿矾(FeSO4·7H2O)。工艺流程如图,根据流程回答下列问题:
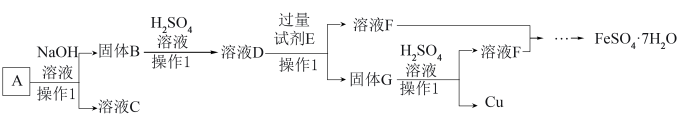
(1)操作1的名称是______ 。
(2)溶液C的溶质主要是______ 。
(3)检验溶液D中含Fe3+的方法是______ ,溶液D与过量试剂E反应的离子方程式Fe+Cu2+=Fe2++Cu、______ 。
(4)FeSO4·7H2O可处理工业废水中有毒的 ,反应的离子方程式为Fe2++
,反应的离子方程式为Fe2++ +H+→Fe3++Cr3++H2O(未配平),该反应中,氧化剂与还原剂的物质的量之比为
+H+→Fe3++Cr3++H2O(未配平),该反应中,氧化剂与还原剂的物质的量之比为______ 。
(5)FeSO4·7H2O由于保存不当容易被空气中氧气氧化而变质,可用酸性KMnO4溶液测定其纯度,测定原理为5Fe2++ +8H+=5Fe3++Mn2++4H2O。现有一瓶绿矾样品,取出ag于试管中,往其中加入Vmlcmol/L酸性KMnO4溶液恰好完全反应,则绿矾样品的纯度为
+8H+=5Fe3++Mn2++4H2O。现有一瓶绿矾样品,取出ag于试管中,往其中加入Vmlcmol/L酸性KMnO4溶液恰好完全反应,则绿矾样品的纯度为______ (用含有a、c、V的式子表示)。

(1)操作1的名称是
(2)溶液C的溶质主要是
(3)检验溶液D中含Fe3+的方法是
(4)FeSO4·7H2O可处理工业废水中有毒的
 ,反应的离子方程式为Fe2++
,反应的离子方程式为Fe2++ +H+→Fe3++Cr3++H2O(未配平),该反应中,氧化剂与还原剂的物质的量之比为
+H+→Fe3++Cr3++H2O(未配平),该反应中,氧化剂与还原剂的物质的量之比为(5)FeSO4·7H2O由于保存不当容易被空气中氧气氧化而变质,可用酸性KMnO4溶液测定其纯度,测定原理为5Fe2++
 +8H+=5Fe3++Mn2++4H2O。现有一瓶绿矾样品,取出ag于试管中,往其中加入Vmlcmol/L酸性KMnO4溶液恰好完全反应,则绿矾样品的纯度为
+8H+=5Fe3++Mn2++4H2O。现有一瓶绿矾样品,取出ag于试管中,往其中加入Vmlcmol/L酸性KMnO4溶液恰好完全反应,则绿矾样品的纯度为
您最近一年使用:0次
解题方法
3 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 铁粉样品中加足量稀硫酸溶解后,滴入两滴 溶液不变红 溶液不变红 | 铁粉未变质 |
| B | 用 试纸测定 试纸测定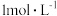 的 的 和 和 溶液的 溶液的 ,前者的试纸颜色比后者深 ,前者的试纸颜色比后者深 | 非金属性: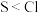 |
| C | 充分加热铁粉和硫粉的混合物,冷却后取少量固体于试管中,加入足量稀硫酸,再滴入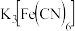 溶液,产生蓝色沉淀 溶液,产生蓝色沉淀 | 铁被硫氧化至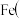 Ⅱ Ⅱ |
| D | 向新制硫酸亚铁溶液中滴加邻二氮菲 | 与邻二氮菲配位能力: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 测定硫酸铜晶体中结晶水的含量 | 加热盛有硫酸铜晶体的蒸发皿,待固体全部呈白色后将蒸发皿放置在铁架台上冷却,再称重 |
| B | 检验Fe(NO3)2中是否混有Fe(NO3)3 | 取样品于试管中,滴加稀硫酸溶解,再滴加几滴KSCN溶液 |
| C | 探究Na2SO3固体样品是否变质 | 取少量待测样品溶于蒸馏水,再加入足量BaCl2溶液 |
| D | 验证Na2CO3溶液中同时存在K+ | 利用焰色试验,透过蓝色钴玻璃后,发现火焰呈紫色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 为探索工业废料的再利用,某化学兴趣小组用含有铝、铁和铜等合金废料制取纯碱、氧化铝和绿矾(FeSO4·7H2O),其工艺流程如下图。
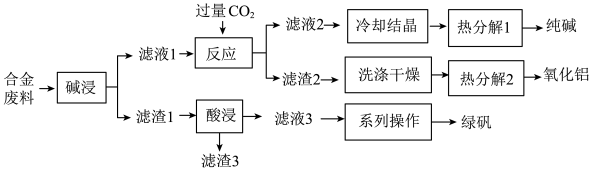
请回答下列问题:
(1)写出“碱浸”中发生反应的化学方程式_______ ,滤渣2的主要成分是_______ (填化学式)。
(2)写出“酸浸”中发生反应的离子方程式_______ ,滤渣3的主要成分是_______ (填化学式)。
(3)写出“热分解1”的化学方程式为_______ ,纯碱在生产生活中的一种用途是_______ 。
(4)该工艺流程中,可循环的物质是_______ (填化学式)。
(5)绿矾可用作补铁剂,长期放置易被氧化而变质。为了探究某绿矾样品是否已变质和变质的程度,该小组同学将样品溶于水,制成待测液,进行如下实验。

请回答下列问题:
(1)写出“碱浸”中发生反应的化学方程式
(2)写出“酸浸”中发生反应的离子方程式
(3)写出“热分解1”的化学方程式为
(4)该工艺流程中,可循环的物质是
(5)绿矾可用作补铁剂,长期放置易被氧化而变质。为了探究某绿矾样品是否已变质和变质的程度,该小组同学将样品溶于水,制成待测液,进行如下实验。
| 实验步骤 | 实验现象 | 结论或方程式 |
| 步骤一:取待测液于试管中,向其中滴加KSCN溶液 | ① | 待测液含有Fe3+。 |
| 步骤二:另取待测液于试管中,向其中滴加② | ③ | 待测液含有Fe2+。 |
| 实验结论:该绿矾样品是部分变质的。 | ||
您最近一年使用:0次
名校
解题方法
6 . 以硫铁矿(主要成分为FeS2,还有少量CuS、SiO2等杂质)为原料制备绿矾晶体FeSO4•7H2O的工艺流程如图:
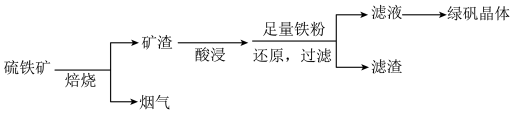
(1)焙烧时黄铁矿要粉碎,其目的是______ 。
(2)由滤液得到绿矾晶体的操作是______ 、______ 、过滤、洗涤、干燥。
(3)烟气中的SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式______ 。
(4)铁粉还原过滤,滤渣中除了铁和铜外还有的成分是______ (写化学式)。
(5)燃料细菌脱硫法是用氧化亚铁硫杆菌对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:

已知总反应为:FeS2+14Fe3++8H2O=2SO +15Fe2++16H+。写出过程Ⅱ反应的离子方程式
+15Fe2++16H+。写出过程Ⅱ反应的离子方程式______ 。
(6)绿矾晶体在空气中易被氧化变质。取xg样品,加水完全溶解,滴加硫酸酸化的amol/LK2Cr2O7溶液至恰好完全反应,消耗K2Cr2O7溶液bmL。反应原理:6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为
+14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为______ 。

(1)焙烧时黄铁矿要粉碎,其目的是
(2)由滤液得到绿矾晶体的操作是
(3)烟气中的SO2会污染环境,可用足量氨水吸收,写出该反应的离子方程式
(4)铁粉还原过滤,滤渣中除了铁和铜外还有的成分是
(5)燃料细菌脱硫法是用氧化亚铁硫杆菌对硫铁矿进行催化脱硫,同时得到FeSO4溶液。其过程如图所示:

已知总反应为:FeS2+14Fe3++8H2O=2SO
 +15Fe2++16H+。写出过程Ⅱ反应的离子方程式
+15Fe2++16H+。写出过程Ⅱ反应的离子方程式(6)绿矾晶体在空气中易被氧化变质。取xg样品,加水完全溶解,滴加硫酸酸化的amol/LK2Cr2O7溶液至恰好完全反应,消耗K2Cr2O7溶液bmL。反应原理:6Fe2++Cr2O
 +14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为
+14H+=6Fe3++2Cr3++7H2O。则绿矾晶体纯度的计算式为
您最近一年使用:0次
解题方法
7 . 由下列实验操作及现象推出的相应结论不正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 将绿矾样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 | 绿矾晶体已经变质 |
| B | 常温下,用pH试纸测定同浓度的NaCl和NaF溶液的pH,pH(NaCl)<pH(NaF) | 结合H+能力:Cl-<F- |
| C | 向CuSO4溶液中通入少量H2S,出现黑色沉淀 | H2S是强酸 |
| D | 向Na2SiO3溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去,2min后,试管中出现凝胶 | 酸性:盐酸>硅酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸,再进行下列实验,其中结论正确的是
| A.若滴加KSCN溶液,溶液变红,说明铁粉变质 |
| B.若滴加KSCN溶液,溶液未变红,说明铁粉未变质 |
| C.若依次滴加氯水,KSCN溶液,溶液变红,说明铁粉全部变质 |
| D.若滴加KSCN溶液,溶液未变红;再滴加氯水,溶液变红,说明铁粉全部变质 |
您最近一年使用:0次
2022-02-27更新
|
1431次组卷
|
24卷引用:广东省化州市第一中学2020-2021学年高一上学期期末考试化学试题
广东省化州市第一中学2020-2021学年高一上学期期末考试化学试题广东省广州中学2022-2023学年高一上学期期末考试化学试题广东省东莞市南城开心实验学校2022-2023学年高一上学期12月半月考化学试题天津市红桥区2020-2021学年高三上学期期中考试化学试题第一节 铁及其化合物 第2课时 铁盐、亚铁盐内蒙古包头市2021-2022学年高一上学期期末考试化学试题辽宁省沈阳市2021-2022学年高一上学期期末质量监测化学试题2北京市北京师范大学第二附属中学2022-2023学年高一上学期12月月考化学试题湖南省株洲世纪星高级中学2022-2023学年高一上学期期末考试化学试题天津市南开中学2022-2023学年高一上学期期末考试化学试题吉林市田家炳高级中学2022-2023学年高一上学期期末考试化学试题内蒙古赤峰市红山区2022-2023学年高一上学期期末质量检测化学试题内蒙古包头市2022-2023学年高一上学期期末考试化学试题内蒙古呼伦贝尔市满洲里市第一中学2022-2023学年高一下学期第一次月考化学试题四川省绵阳南山中学2022-2023学年高一上学期期末模拟化学试题湖南省长沙市珺琟高级中学2023-2024学年高一上学期第二次月考化学试题 四川省宜宾市第四中学校2023-2024学年高一上学期1月期末化学试题云南省昆明市五华区2023-2024学年高一上学期1月期末化学试题天津市静海区第一中学2023-2024学年高一上学期12月月考化学试题浙江省丽水市三校联考2023-2024学年高一上学期12月月考化学试题四川省江油市太白中学2023-2024学年高一上学期第三次月考化学试题湖南省常德石门一中2023-2024年上学期高一年级化学期末考试卷(适用湖南地区))湖南省长沙市长郡中学2023-2024学年高一下学期选科适应性检测化学试卷河南省开封市联考2023-2024学年高一上学期1月期末化学试题
名校
9 . 浅绿色的硫酸亚铁铵晶体[又名莫尔盐,(NH4)2SO4·FeSO4·6H2O]比(FeSO4·7H2O)更稳定,常用于定量分析。
(1)浓度均为0.10mol·L-1的莫尔盐溶液和FeSO4溶液,c(Fe2+)前者____ 后者。(填“>”、“<”或“无法判断”)
(2)0.10mol·L-1莫尔盐溶液中离子浓度由大到小的顺序为____ 。
(3)莫尔盐比硫酸亚铁稳定,但在空气中久置也容易变质,检验其是否变质的试剂是___ 。
(4)用标准浓度的莫尔盐溶液定量分析某样品中KMnO4(式量:158)的含量。
①称量1.5800gKMnO4样品于烧杯中,溶解后加稀H2SO4酸化,配成250mL溶液。
②取0.1000mol·L-1的莫尔盐标准溶液25.00mL于锥形瓶中,然后用KMnO4样品溶液滴定。滴定终点的现象是____ 。平行滴定3次,样品溶液的平均用量为17.50mL,则样品纯度为____ 。(保留三位有效数字)
③滴定时需选用的滴定管应为____ (填“a”或“b”)。

④若测定结果偏高,其原因可能是____ (填字母编号)。
A.滴定管用蒸馏水洗净后未用KMnO4溶液润洗
B.滴定终点读数时,俯视滴定管,其他操作正确
C.配制标准溶液时,俯视定容
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
(1)浓度均为0.10mol·L-1的莫尔盐溶液和FeSO4溶液,c(Fe2+)前者
(2)0.10mol·L-1莫尔盐溶液中离子浓度由大到小的顺序为
(3)莫尔盐比硫酸亚铁稳定,但在空气中久置也容易变质,检验其是否变质的试剂是
(4)用标准浓度的莫尔盐溶液定量分析某样品中KMnO4(式量:158)的含量。
①称量1.5800gKMnO4样品于烧杯中,溶解后加稀H2SO4酸化,配成250mL溶液。
②取0.1000mol·L-1的莫尔盐标准溶液25.00mL于锥形瓶中,然后用KMnO4样品溶液滴定。滴定终点的现象是
③滴定时需选用的滴定管应为

④若测定结果偏高,其原因可能是
A.滴定管用蒸馏水洗净后未用KMnO4溶液润洗
B.滴定终点读数时,俯视滴定管,其他操作正确
C.配制标准溶液时,俯视定容
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
您最近一年使用:0次
10 . 下列根据实验操作和实验现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将某气体通入淀粉KI溶液中 | 溶液变成蓝色 | 该气体一定是氯气 |
| B | 向AgNO3溶液中滴加过量氨水 | 得到澄清溶液 | Ag+和NH3 H2O可以大量共存 H2O可以大量共存 |
| C | 在某盐溶液中加Al,然后加入少量NaOH溶液,加热 | 产生的气体可使湿润的红色石蕊试纸变蓝色 | 该盐中含有NO |
| D | 将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液 | 溶液变血红色 | Fe(NO3)2样品已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次