1 . 下列实验方案设计、现象与结论都正确的是
| 选项 | 目的 | 实验方案设计 | 现象与结论 |
| A | 检验溶液X中是否含有 | 向溶液X中滴加少量稀硝酸,然后滴入几滴 溶液,观察现象 溶液,观察现象 | 有白色沉淀产生,说明溶液中含 |
| B | 检验食品脱氧剂中的还原铁粉是否变质 | 取少量样品溶于盐酸,滴加KSCN溶液 | 溶液变红,说明已变质 |
| C | 验证压强对化学平衡的影响 | 先将密闭注射器内充满 气体,然后将活塞往里推压缩容积 气体,然后将活塞往里推压缩容积 | 观察到注射器内气体颜色加深,证明加压使平衡向生成 气体的方向移动 气体的方向移动 |
| D | 检验1-溴丁烷的消去产物 | 向圆底烧瓶中加2.0gNaOH和15mL无水乙醇,搅拌,再加5mL 1-溴丁烷和几片碎瓷片,微热,将产生的气体通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液紫红色褪去,有1-丁烯生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 下列方案设计、现象和结论都正确的是
选项 | 目的 | 方案设计 | 现象和结论 |
A | 探究温度对化学平衡的影响 | 将2mL0.5mol/L的CuCl2溶液加热后置于冷水中,观察现象 | 若溶液由黄绿色变为蓝色,说明降低温度,平衡向逆方向移动: [Cu(H2O)4]2++4Cl-  [CuCl4]2﹣+4H2O [CuCl4]2﹣+4H2O |
B | 判断某卤代烃中的卤素 | 取2 mL卤代烃样品于试管中,加入5 mL 20% KOH水溶液混合后加热,再滴加AgNO3溶液 | 若产生的沉淀为白色,则该卤代烃中含有氯元素 |
C | 探究FeCl3溶液与KI溶液的反应 | 向10mLFeCl3溶液中滴加5mL等浓度的KI溶液,充分反应后,再滴加KSCN溶液,观察现象 | 若溶液最终变为血红色,FeCl3溶液与KI溶液的反应为可逆反应 |
D | 检验食品脱氧剂中还原铁粉是否已变质 | 取脱氧剂包装内固体粉末于试管中,加足量稀盐酸溶解,充分反应后滴加KSCN溶液,振荡,观察溶液颜色变化 | 若溶液未变红色,说明脱氧剂中还原铁粉没有变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-08更新
|
185次组卷
|
2卷引用:江苏省扬州中学2023-2024学年高二下学期4月期中考试化学试题
解题方法
3 . 下列关于检验样品久置空气中是否变质的实验方法或操作能达到目的的是
| 选项 | 实验目的 | 实验方法或操作 |
| A | 检验 样品是否变质 样品是否变质 | 将样品溶解后加入 酸化的 酸化的 溶液,观察是否产生白色沉淀 溶液,观察是否产生白色沉淀 |
| B | 检验KI溶液是否变质 | 向样品中滴加少量稀硫酸,再滴入2~3滴淀粉溶液,观察溶液颜色变化 |
| C | 检验 样品是否变质 样品是否变质 | 将样品溶解后滴加几滴 溶液,再滴加 溶液,再滴加 溶液,观察溶液颜色变化 溶液,观察溶液颜色变化 |
| D | 检验漂白粉是否变质 | 将漂白粉溶于水后,滴加浓盐酸,观察是否产生气泡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . 硫酸亚铁(FeSO4)是中学化学常用试剂,可用于治疗缺铁性贫血症。
(1)实验室配备FeSO4溶液时为防止硫酸亚铁变质,常采用的措施是___________ (填一种)。
(2)以FeSO4为原料可制备碱式硫酸铁[Fe4(OH)2(SO4)5]、铁红、硫酸亚铁铵[(NH4)2Fe(SO4)2,俗名摩尔盐],转化关系如图所示。___________ 。
②制备FeCO3时,向FeSO4溶液中加入过量的NH4HCO3溶液,有气体生成,该反应的离子方程式为___________ 。
③制备摩尔盐时将反应物混合,经___________ 、冷却结晶、过滤、洗涤、干燥得到产品。
用工业废渣(主要含有Fe2O3、FeO、Al2O3及少量Fe)制备绿矾FeSO4·7H2O晶体的流程如下:___________ 。
(4)“溶解”后所得溶液中含有的阳离子为Fe3+和___________ 。
(5)“还原”时选择FeS2而不用Cu粉的原因是___________ 。
(6)测定绿矾中Fe2+的氧化率实验方案如下:
步骤一:称取一定质量的绿矾样品,将其溶于适量的无氧蒸馏水并配成250mL溶液;
步骤二:取步骤一中配得的溶液25.00mL于锥形瓶,并加入适量稀硫酸酸化,逐滴滴加0.0400mol/LKMnO4溶液至恰好完全反应,反应原理为:MnO +Fe2++H+=Mn2++Fe3++H2O(未配平),消耗KMnO4溶液20.00mL;
+Fe2++H+=Mn2++Fe3++H2O(未配平),消耗KMnO4溶液20.00mL;
步骤三:另取步骤一中配得的溶液25.00mL于烧杯,加入足量氨水,将沉淀过滤、洗涤、干燥,在空气中灼烧至固体质量不再变化,称得残留红棕色固体的质量为0.4g。(已知: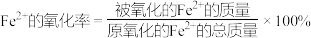 )
)
根据以上数据,计算该绿矾样品中Fe2+的氧化率,写出计算过程:___________ 。
(1)实验室配备FeSO4溶液时为防止硫酸亚铁变质,常采用的措施是
(2)以FeSO4为原料可制备碱式硫酸铁[Fe4(OH)2(SO4)5]、铁红、硫酸亚铁铵[(NH4)2Fe(SO4)2,俗名摩尔盐],转化关系如图所示。
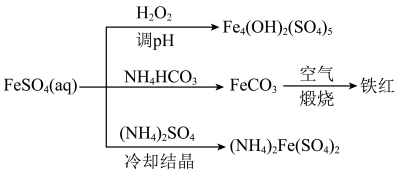
②制备FeCO3时,向FeSO4溶液中加入过量的NH4HCO3溶液,有气体生成,该反应的离子方程式为
③制备摩尔盐时将反应物混合,经
用工业废渣(主要含有Fe2O3、FeO、Al2O3及少量Fe)制备绿矾FeSO4·7H2O晶体的流程如下:

(4)“溶解”后所得溶液中含有的阳离子为Fe3+和
(5)“还原”时选择FeS2而不用Cu粉的原因是
(6)测定绿矾中Fe2+的氧化率实验方案如下:
步骤一:称取一定质量的绿矾样品,将其溶于适量的无氧蒸馏水并配成250mL溶液;
步骤二:取步骤一中配得的溶液25.00mL于锥形瓶,并加入适量稀硫酸酸化,逐滴滴加0.0400mol/LKMnO4溶液至恰好完全反应,反应原理为:MnO
 +Fe2++H+=Mn2++Fe3++H2O(未配平),消耗KMnO4溶液20.00mL;
+Fe2++H+=Mn2++Fe3++H2O(未配平),消耗KMnO4溶液20.00mL;步骤三:另取步骤一中配得的溶液25.00mL于烧杯,加入足量氨水,将沉淀过滤、洗涤、干燥,在空气中灼烧至固体质量不再变化,称得残留红棕色固体的质量为0.4g。(已知:
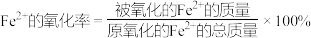 )
)根据以上数据,计算该绿矾样品中Fe2+的氧化率,写出计算过程:
您最近一年使用:0次
名校
解题方法
5 . 根据下列实验操作和现象所得结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 在小烧杯中滴有少量水,加入20gBa(OH)2·8H2O晶体和10gNH4Cl晶体,用玻璃棒快速搅拌并触摸烧杯外壁,发现烧杯外壁很冷 | Ba(OH)2·8H2O与NH4Cl的反应为吸热反应 |
| B | 将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液,溶液变红 | Fe(NO3)2已变质 |
| C | 用3mL稀盐酸与过量Zn反应,当气泡稀少时,加入1mL浓盐酸,又迅速产生较多气泡 | 盐酸浓度增大,反应速率加快 |
| D | 向5mL0.1mol·L-1FeCl3溶液中滴入0.1 mol·L-1KI溶液5~6滴,加2mLCCl4振荡,静置后取上层清液滴加KSCN溶液,溶液变红 | Fe3+与I-的反应有一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-08-03更新
|
1293次组卷
|
4卷引用:江苏省苏州市2019-2020学年高一下学期期末考试化学试题
名校
6 . 铁及其化合物在日常生活中有广泛应用。
(1)写出Fe(OH)2转化为Fe(OH)3的化学方程式_______________ 。
(2)绿矾(FeSO4·7H2O)是补血剂的原料,易变质。检验绿矾是否变质的试剂是_______________
设计实验检验绿矾是否完全变质__________
(3)利用绿矾制备还原铁粉的工业流程如下:
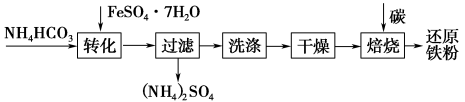
①干燥过程主要是为了脱去游离水和结晶水,过程中会有少量FeCO3·nH2O在空气中被氧化为FeOOH,该反应的化学方程式为_______________
②取干燥后的FeCO3样品12.49g ,焙烧,最终得到还原铁粉6.16g,计算样品中杂质FeOOH的质量____
(4)以羰基化合物为载体运用化学平衡移动原理分离、提纯某纳米级活性铁粉(含有一些不反应的杂质),反应装置如下图。
Fe(s)+5CO(g) Fe(CO)5(g) ΔH<0
Fe(CO)5(g) ΔH<0

T1___ T2(填“>”、“<”或“=”),判断理由是_______________
(1)写出Fe(OH)2转化为Fe(OH)3的化学方程式
(2)绿矾(FeSO4·7H2O)是补血剂的原料,易变质。检验绿矾是否变质的试剂是
设计实验检验绿矾是否完全变质
(3)利用绿矾制备还原铁粉的工业流程如下:

①干燥过程主要是为了脱去游离水和结晶水,过程中会有少量FeCO3·nH2O在空气中被氧化为FeOOH,该反应的化学方程式为
②取干燥后的FeCO3样品12.49g ,焙烧,最终得到还原铁粉6.16g,计算样品中杂质FeOOH的质量
(4)以羰基化合物为载体运用化学平衡移动原理分离、提纯某纳米级活性铁粉(含有一些不反应的杂质),反应装置如下图。
Fe(s)+5CO(g)
 Fe(CO)5(g) ΔH<0
Fe(CO)5(g) ΔH<0
T1
您最近一年使用:0次
2016-12-09更新
|
931次组卷
|
3卷引用:江苏省苏南名校高三上学期9月抽检测试化学试题
2022·浙江金华·二模
名校
解题方法
7 . 下列方案设计、现象和结论有不正确 的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验海带中是否含有碘元素 | 将海带灰溶解过滤后,取适量滤液于试管中,酸化后加入少量新制氯水,充分反应后加入1~2滴淀粉溶液 | 溶液变蓝,则证明海带中含有碘元素 |
| B | 鉴定淀粉是否完全水解 | 取少量淀粉于锥形瓶中,以固液比1∶10加入稀硫酸,牛皮纸封口,在120℃下水解30min,取适量水解液于试管中,加入少量碘-碘化钾溶液 | 溶液未变蓝,则证明淀粉已完全水解 |
| C | 检验CO还原 的生成物中是否含有 的生成物中是否含有 | 将适量反应后的固体溶于稀盐酸中,取少量溶解液于试管中,滴加硫氰化钾溶液 | 溶液变血红色,则证明还原产物中含有 |
| D | 检验食盐中是否混有少量亚硝酸钠 | 取适量食盐样品于试管中,加水溶解后加入硝酸银溶液,过滤后取滤渣,滴加稀硝酸 | 若沉淀部分溶解,则证明食盐中混有亚硝酸钠 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-14更新
|
779次组卷
|
7卷引用:押江苏卷第11题 化学实验综合选择题 -备战2022年高考化学临考题号押题(江苏卷)
(已下线)押江苏卷第11题 化学实验综合选择题 -备战2022年高考化学临考题号押题(江苏卷)江苏省淮安市钦工中学2022-2023学年高三上学期第一次月考化学试题江苏省徐州市第七中学2022-2023学年高三上学期9月摸底学情调研化学试题浙江省金华十校2021-2022学年高三下学期4月模拟考试化学试题(已下线)2022年浙江省6月高考真题变式题21-25湖南省攸县第二中学2022-2023学年高三第六次月考化学试题湖南省攸县第一中学2022-2023学年高三第六次月考化学试题



