24. 某同学利用钠与硫酸铜溶液进行实验,并对其现象进行分析,研究其产物组成。
(1)硫酸铜溶液的配制:准确称取五水硫酸铜(CuSO
4·5H
2O)晶体2.5000g,溶解后转移至100mL容量瓶中。
①上述实验过程中,用不到的实验仪器有
____ (填标号)。

②该CuSO
4溶液的浓度为
__________mo/L。
③通过理论计算,当上述硫酸铜与钠完全反应,溶液质量变化为
___ g。
(2)将配好的CuSO
4溶液,分3组进行实验,实验结果如下图所示:
| 序号 | CuSO4溶液体积/mL | 金属钠质量/g | 实验现象 |
| a | 15 | 0.01g | 迅速产生大量蓝色沉淀 |
| b | 15 | 0.1g | 蓝色沉淀和黑色沉淀共存 |
| c | 15 | 1.0g | 出现大量黑色沉淀 |
查阅资料得知:极细的铜粉,外观呈现黑色
①a组中的蓝色沉淀成分主要是
_________。
②将c组中黑色沉淀进行抽滤,干燥,对其成分进行初步的猜想
猜想ⅰ:金属钠将铜置换出来,以极细的铜粉存在;
猜想ⅱ:金属钠与水反应剧烈放热,
______________。
设计一个简单的实验,证明猜想ⅰ是错误的
______________。
(3)为进一步验证黑色固体的成分,该同学求助实验室检测,得到黑色固体中含铜化合物主要有硫酸氧化铜[Cu
2O(SO
4)]、碱式硫酸铜[Cu
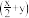
(OH)
x(SO
4)
y]、氧化铜[CuO]三种。写出钠与硫酸铜反应生成碱式硫酸铜的化学方程式
____________。
(4)根据实验结果,可以得到的结论为
____________(写一条)。