2024·广西·模拟预测
解题方法
1 . 实验小组用过量 溶液处理覆铜板得到浸出液,并对其中的物质进行回收,流程如下。下列有关说法正确的是
溶液处理覆铜板得到浸出液,并对其中的物质进行回收,流程如下。下列有关说法正确的是
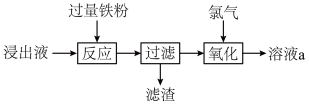
 溶液处理覆铜板得到浸出液,并对其中的物质进行回收,流程如下。下列有关说法正确的是
溶液处理覆铜板得到浸出液,并对其中的物质进行回收,流程如下。下列有关说法正确的是
| A.浸出液呈中性 | B.滤渣只有铜粉 |
| C.用KSCN溶液检验是否“氧化”完全 | D.溶液a回收后可用于处理覆铜板 |
您最近一年使用:0次
23-24高三上·上海宝山·阶段练习
名校
解题方法
2 . 国庆期间,思源同学参观了2023上海新能源车展,他了解到目前新能源电车大部分使用的都是磷酸铁锂电池,草酸亚铁晶体( ,难溶于水)是制备磷酸铁锂正极材料所需的主要原材料。思源同学想在实验室里利用废铁屑制备草酸亚铁晶体(
,难溶于水)是制备磷酸铁锂正极材料所需的主要原材料。思源同学想在实验室里利用废铁屑制备草酸亚铁晶体( )并测定产品的纯度。请帮助他一起完成探究!
)并测定产品的纯度。请帮助他一起完成探究!
Ⅰ.草酸亚铁晶体( )的制备:
)的制备:
(1)实验前的准备——药品的选择与处理
为了防止制备的硫酸亚铁溶液变质,制备过程中应采取的措施是_______ 。
(2)实验过程中——操作与观察
思源同学选取了如图所示装置,在实验过程中,实验过程中往装置中不断通入 ,其目的有:
,其目的有:_______ 、_______ (结合实验装置回答,至少答出两点)。
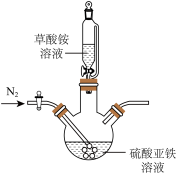
(3)反应结束后——产物的分离与后处理
反应完全后,用蒸馏水和无水乙醇多次洗涤,进行固液分离,在60℃下干燥12h,得到淡黄色的草酸亚铁晶体产品。
①检验草酸亚铁晶体洗涤干净的方法是_______ ;
②写出制备草酸亚铁晶体的离子方程式:_______ 。
Ⅱ.产品纯度的测定:
思源同学对比发现自己制得的草酸亚铁晶体在外观上和商品出售的高纯度草酸亚铁晶体略有不同,他猜测这是由于产物中含有杂质 和
和 所致,于是接着设计实验来测定所得产物中
所致,于是接着设计实验来测定所得产物中 的质量分数。
的质量分数。
实验过程:
①将准确称量的ag草酸亚铁晶体样品置于250 锥形瓶内,加入适量2
锥形瓶内,加入适量2 的
的 溶解,加热至70℃左右,用浓度为0.2000
溶解,加热至70℃左右,用浓度为0.2000 的高锰酸钾标准溶液滴定至终点,重复3次,平均消耗高锰酸钾溶液b
的高锰酸钾标准溶液滴定至终点,重复3次,平均消耗高锰酸钾溶液b ;(已知:
;(已知: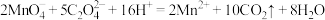 )
)
②向上述滴定混合液中加入适量的 粉和过量的2
粉和过量的2 的
的 溶液,煮沸(不含
溶液,煮沸(不含 ),继续用0.2000
),继续用0.2000 的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液c
的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液c 。
。
(4)步骤②中加入锌粉的目的是_______ 。
(5)步骤②中检验溶液不含 的操作:取一滴煮沸后的溶液滴入装有
的操作:取一滴煮沸后的溶液滴入装有_______ (填化学式)溶液的试管中,若_______ ,则说明溶液不含 。
。
(6)样品中 的质量分数为
的质量分数为_______ %(用含a、b、c的式子表示)。
(7)实验结束整理药品时,思源同学发现在步骤①中配制得到的溶液颜色已发生变化,这是由于部分 被氧化,他又想到自己在配制完溶液后,因为临时接电话耽误了一会儿,则思源同学的测定结果
被氧化,他又想到自己在配制完溶液后,因为临时接电话耽误了一会儿,则思源同学的测定结果_______ (选填字母: A.“偏高”;B.“偏低”;C.“不变”)。
 ,难溶于水)是制备磷酸铁锂正极材料所需的主要原材料。思源同学想在实验室里利用废铁屑制备草酸亚铁晶体(
,难溶于水)是制备磷酸铁锂正极材料所需的主要原材料。思源同学想在实验室里利用废铁屑制备草酸亚铁晶体( )并测定产品的纯度。请帮助他一起完成探究!
)并测定产品的纯度。请帮助他一起完成探究!Ⅰ.草酸亚铁晶体(
 )的制备:
)的制备:(1)实验前的准备——药品的选择与处理
为了防止制备的硫酸亚铁溶液变质,制备过程中应采取的措施是
(2)实验过程中——操作与观察
思源同学选取了如图所示装置,在实验过程中,实验过程中往装置中不断通入
 ,其目的有:
,其目的有:
(3)反应结束后——产物的分离与后处理
反应完全后,用蒸馏水和无水乙醇多次洗涤,进行固液分离,在60℃下干燥12h,得到淡黄色的草酸亚铁晶体产品。
①检验草酸亚铁晶体洗涤干净的方法是
②写出制备草酸亚铁晶体的离子方程式:
Ⅱ.产品纯度的测定:
思源同学对比发现自己制得的草酸亚铁晶体在外观上和商品出售的高纯度草酸亚铁晶体略有不同,他猜测这是由于产物中含有杂质
 和
和 所致,于是接着设计实验来测定所得产物中
所致,于是接着设计实验来测定所得产物中 的质量分数。
的质量分数。实验过程:
①将准确称量的ag草酸亚铁晶体样品置于250
 锥形瓶内,加入适量2
锥形瓶内,加入适量2 的
的 溶解,加热至70℃左右,用浓度为0.2000
溶解,加热至70℃左右,用浓度为0.2000 的高锰酸钾标准溶液滴定至终点,重复3次,平均消耗高锰酸钾溶液b
的高锰酸钾标准溶液滴定至终点,重复3次,平均消耗高锰酸钾溶液b ;(已知:
;(已知: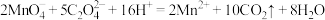 )
)②向上述滴定混合液中加入适量的
 粉和过量的2
粉和过量的2 的
的 溶液,煮沸(不含
溶液,煮沸(不含 ),继续用0.2000
),继续用0.2000 的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液c
的高锰酸钾标准溶液滴定至终点,平均消耗高锰酸钾溶液c 。
。(4)步骤②中加入锌粉的目的是
(5)步骤②中检验溶液不含
 的操作:取一滴煮沸后的溶液滴入装有
的操作:取一滴煮沸后的溶液滴入装有 。
。(6)样品中
 的质量分数为
的质量分数为(7)实验结束整理药品时,思源同学发现在步骤①中配制得到的溶液颜色已发生变化,这是由于部分
 被氧化,他又想到自己在配制完溶液后,因为临时接电话耽误了一会儿,则思源同学的测定结果
被氧化,他又想到自己在配制完溶液后,因为临时接电话耽误了一会儿,则思源同学的测定结果
您最近一年使用:0次
3 . 下列实验设计不能达到实验目的的是
| 实验目的 | 实验设计 | |
| A | 检验溶液中 是否被氧化 是否被氧化 | 取少量待测溶液,滴加KSCN溶液,观察溶液的颜色变化 |
| B | 净化用石灰石和盐酸反应制得的 气体 气体 | 将气体依次通过盛有饱和 溶液、浓硫酸的洗气瓶 溶液、浓硫酸的洗气瓶 |
| C | 测定NaClO溶液的pH值 | 将待测液滴在pH试纸上,待显色后与标准比色卡对照 |
| D | 用工业酒精制备无水乙醇 | 工业酒精中加生石灰、蒸馏 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



