名校
1 . 为了探究浓度和温度对平衡的影响,设计如下方案:
已知:

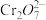 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+ △H1
(黄色)+2H+ △H1
 (蓝色)+4Cl-
(蓝色)+4Cl-
 (黄色)+4H2O △H2
(黄色)+4H2O △H2
下列叙述正确的是
| 实验 | 操作 | 现象 |
| ① | 向1mL 0.05 mol∙L-1 FeCl3溶液中滴加1滴0.15 mol∙L-1 KSCN溶液 | 溶液变红色 |
| ② | 向1mL 0.05 mol∙L-1 FeCl3溶液中滴加1mL 0.5 mol∙L-1 NaF溶液,再滴1滴0.15 mol∙L-1 KSCN溶液 | 溶液不变红色 |
| ③ | 向1mL 0.1 mol∙L-1 K2Cr2O7溶液中滴加几滴浓硫酸 | 溶液橙色加深 |
| ④ | 将盛有1mL 0.5 mol∙L-1 CuCl2溶液的两支试管,分别置于热水浴和冷水浴中 | 前者溶液显黄色,后者溶液显蓝色 |

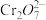 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+ △H1
(黄色)+2H+ △H1 (蓝色)+4Cl-
(蓝色)+4Cl-
 (黄色)+4H2O △H2
(黄色)+4H2O △H2下列叙述正确的是
A.由①和②可知,Fe(SCN)3比 稳定 稳定 |
B.由③可知,c(H+)增大,平衡向生成 的方向移动 的方向移动 |
| C.由④可知,△H2<0 |
| D.由上述实验可知,向CuCl2溶液持续通入HCl,溶液蓝色加深 |
您最近一年使用:0次
2022-11-05更新
|
159次组卷
|
4卷引用:湖南省河南省湘豫名校联考2022- 2023学年高二上学期阶段考试(一)化学试题
22-23高一上·全国·阶段练习
名校
2 . 铁是人体必需的微量元素,严重缺铁时需要服用补铁剂。实验小组为研究某补铁剂中铁元素的价态及其含量,设计并进行了如下实验:
【查阅资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价。
Ⅲ.Fe(OH)3受热分解生成Fe2O3。
实验Ⅰ.检验该补铁剂中铁元素的价态。
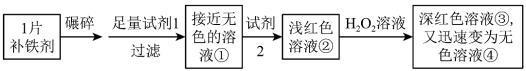
将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是_______ ,试剂2是_______ 。
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有_______ 。
(3)能证明溶液①中含有Fe2+的实验现象是_______ 。
(4)补全在上述条件下Fe2+与H2O2发生反应的离子方程式:_______ 。
_______H++_______Fe2++_______H2O2=_______ _______+_______ _______
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的SCN-与H2O2发生了化学反应。
a.甲同学猜测的依据是_______ 。
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是_______ 。
实验Ⅱ.测定该补铁剂中铁元素的含量。

(6)计算每片该补铁剂含铁元素的质量为_______ g。
(7)人体只能吸收Fe2+,医生建议在服用该补铁剂时,同时服用有较强还原性的维生素C,理由是_______ 。
【查阅资料】Ⅰ.该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
Ⅱ.KSCN中的硫元素为-2价。
Ⅲ.Fe(OH)3受热分解生成Fe2O3。
实验Ⅰ.检验该补铁剂中铁元素的价态。

将补铁剂碾碎的目的是增大接触面积,使其充分溶解。
(1)试剂1是
(2)加入试剂2后溶液变为浅红色,说明溶液①中含有
(3)能证明溶液①中含有Fe2+的实验现象是
(4)补全在上述条件下Fe2+与H2O2发生反应的离子方程式:
_______H++_______Fe2++_______H2O2=_______ _______+_______ _______
(5)甲同学猜测深红色溶液③迅速变为无色溶液④的原因,可能是溶液中的SCN-与H2O2发生了化学反应。
a.甲同学猜测的依据是
b.乙同学通过实验证实了甲同学的猜测,其实验方案及现象是
实验Ⅱ.测定该补铁剂中铁元素的含量。

(6)计算每片该补铁剂含铁元素的质量为
(7)人体只能吸收Fe2+,医生建议在服用该补铁剂时,同时服用有较强还原性的维生素C,理由是
您最近一年使用:0次
2022-11-01更新
|
603次组卷
|
3卷引用:第二次月考测评卷-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
(已下线)第二次月考测评卷-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)北京市海淀区第二十中学2022-2023学年高一上学期11月月考化学试题章末检测卷(三) 铁 金属材料
名校
解题方法
3 . 下列物质的保存或使用方法不正确 的是
| A.保存FeCl3溶液时需要加少量铁粉 | B.Na2O2需要密封保存 |
| C.铝锅不宜长时间存放酸性或碱性食物 | D.金属钠保存在煤油中 |
您最近一年使用:0次
2022-01-14更新
|
209次组卷
|
4卷引用:第二次月考测评卷-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
(已下线)第二次月考测评卷-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)北京市石景山区2021-2022学年高一上学期期末考试化学试题北京市第一○一中学2023-2024学年高一上学期统练四(12月考)化学试题吉林省吉林市第二中学2022-2023学年高一上学期1月期末考试化学试题
名校
4 . 从含有CuCl2、FeCl2、FeCl3的工业废液中回收铜并制备氯化铁晶体的流程如下:
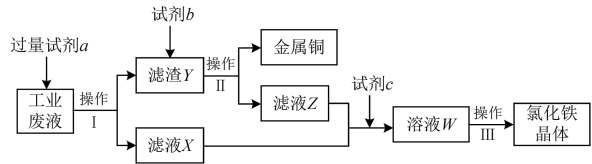
则下列说法正确的是

则下列说法正确的是
| A.试剂a是铁,试剂b是稀硫酸 |
| B.操作Ⅰ、操作Ⅱ、操作Ⅲ所用的仪器完全相同 |
| C.试剂c是氯气,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl- |
| D.用KSCN溶液可检验溶液W中是否有Fe2+ |
您最近一年使用:0次
2019-06-19更新
|
2698次组卷
|
31卷引用:第二次月考测评卷-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
(已下线)第二次月考测评卷-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)2016届河南省八市重点高中高三9月教学质量监测考试化学试卷2016届河南省林州市第一中学高三上学期9月质检化学试卷河南省南阳市第一中学2017-2018学年高一上学期第四次月考化学试题江西省南昌市第二中学2017-2018学年高一上学期第三次月考化学试题四川省成都市第七中学2017-2018学年度上学期高一1月阶段性测试化学试题吉林省长春市市田家炳实验中学2019届高三上学期12月月考化学试题【全国百强校】江西省南昌市第十中学2019届高三上学期第二次月考化学试题天津市杨村第一中学2020届高三上学期第一次月考化学试题四川省绵阳市南山中学2020-2021学年高一上学期12月月考化学试题宁夏银川市景博中学2021-2022学年高一上学期第二次月考化学试题山东省鄄城县第一中学2023-2024学年高三上学期9月月考化学试题2018届高三一轮复习化学:考点21-铜及其化合物性质探究甘肃省酒泉市敦煌中学2019届高三二诊化学试题黑龙江省齐齐哈尔市第八中学2019届高三9月月考化学试题【全国百强校】陕西省西安中学2019届高三上学期期中考试化学试题步步为赢 高二化学暑假作业:作业四 金属及其化合物黑龙江齐齐哈尔市第八中学2018-2019学年高二6月月考化学试题百所名校联考-金属及其化合物(已下线)考点22 工业流程综合——《备战2020年高考精选考点专项突破题集》(已下线)考点05 典型金属元素及其化合物——《备战2020年高考精选考点专项突破题集》辽宁省大连市普兰店区第一中学2019-2020学年高一上学期期末考试化学试题人教版(2019)高一必修第一册第三章 铁 金属材料 高考挑战区鲁科版(2019)高一必修第一册第三章C 高考挑战区 过模拟 2年模拟精编精练(已下线)【浙江新东方】双师107专题9 本专题复习提升-高中化学必修第二册苏教版2019(苏教版2019)必修第二册专题9 金属与人类文明 C 高考挑战区安徽省芜湖市2021-2022学年高一上学期期末教学质量监控化学试题湖南省衡阳市衡阳县2021-2022学年高一上学期期末考试化学试题黑龙江省富锦市第一中学2022-2023学年高一上学期期末考试化学试题新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题



