21-22高一下·浙江宁波·阶段练习
1 . 下列方案设计、现象和结论有不正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验某溶液中是否存在 | 取无锈铁丝用稀硫酸洗净,在外焰上灼烧至与原火焰颜色相同后,蘸取溶液做同样操作,透过蓝色钴玻璃片观察现象 | 若观察到紫色火焰,则溶中存在 |
| B | 探究 固体样品是否变质 固体样品是否变质 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量 溶液 溶液 | 若有白色沉淀产生,则样品已经变质 |
| C | 探究淀粉的水解 | 在试管中加入0.5g淀粉和4mL2mol/L 溶液,加热。冷却后加入少量新制 溶液,加热。冷却后加入少量新制 ,加热,观察现象 ,加热,观察现象 | 若未出现砖红色沉淀,不能说明淀粉未水解 |
| D | 探究 的性质 的性质 | 在稀 中加入少量 中加入少量 (s),观察现象 (s),观察现象 | 若溶液由无色变为蓝色并有红色固体生成,则反应中 既作氧化剂又作还原剂 既作氧化剂又作还原剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 部分被氧化的Fe-Cu合金样品(氧化产物为Fe2O3、CuO)共5.76g,经如下处理:
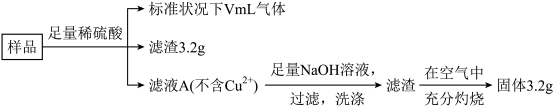
已知:氯化铁溶液用于腐蚀印刷电路铜板的离子反应为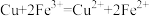 。下列说法正确的是
。下列说法正确的是
①滤液A中的阳离子为Fe2+、Fe3+、H+
②样品中氧原子的物质的量为0.02mol
③溶解样品的过程中消耗H2SO4的总物质的量为0.04mol④V=224⑤V=448

已知:氯化铁溶液用于腐蚀印刷电路铜板的离子反应为
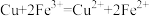 。下列说法正确的是
。下列说法正确的是①滤液A中的阳离子为Fe2+、Fe3+、H+
②样品中氧原子的物质的量为0.02mol
③溶解样品的过程中消耗H2SO4的总物质的量为0.04mol④V=224⑤V=448
| A.①③④ | B.②③④ | C.②③⑤ | D.①②⑤ |
您最近一年使用:0次
名校
解题方法
3 . 取一定量胆矾晶体(CuSO4·5H2O)加热分解,固体残留率( ) 随温度的变化如图所示:
) 随温度的变化如图所示:
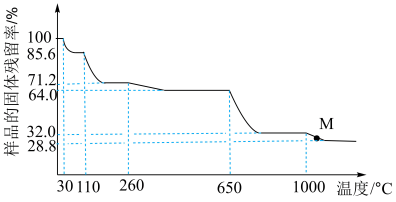
下列说法中不正确的是
 ) 随温度的变化如图所示:
) 随温度的变化如图所示:
下列说法中不正确的是
| A.110°C 时的晶体化学式 CuSO4·3H2O |
B.260°C~ 650°C 过程中的反应方程式为CuSO4·H2O CuSO4+H2O CuSO4+H2O |
| C.已知 650°C 加热至 1000°C ,产物为一种固体与一种气体, 则气体为SO2 |
| D.M 点所得固体是 CuO 与 Cu2O 的混合物 |
您最近一年使用:0次



