名校
1 . 一定量的Cu与足量浓硫酸混合加热,充分反应后生成2.24LSO2气体(标准状况下),反应后溶液体积为500mL。试计算:
(1)参加反应的Cu的质量___ 。
(2)反应后溶液中CuSO4的物质的量浓度___ 。
(1)参加反应的Cu的质量
(2)反应后溶液中CuSO4的物质的量浓度
您最近一年使用:0次
2021-05-27更新
|
614次组卷
|
4卷引用:2020年山西省普通高中学业水平考试化学试题
2 . 在加热条件下,6.4g铜与20mL 18mol/L硫酸(足量)反应,反应后稀释溶液至200mL。计算:
(1)生成气体的体积为_____ (标准状况下)
(2)被还原的硫酸的物质的量为_____
(3)反应后溶液中硫酸根离子的物质的量浓度为_____
(1)生成气体的体积为
(2)被还原的硫酸的物质的量为
(3)反应后溶液中硫酸根离子的物质的量浓度为
您最近一年使用:0次
2021-04-23更新
|
387次组卷
|
2卷引用:福建省莆田第十五中学2018-2019学年高一下学期期中测试化学试题
名校
3 . 将32.0g铜与100mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2的混合气体在标准状况下的体积为11.2L。请回答:
(1)NO气体的体积为_______ L,NO2气体的体积为_______ L。
(2)待产生的气体全部逸出后,向溶液中加入VmLamol•L‒1NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为_______ mol•L‒1。
(1)NO气体的体积为
(2)待产生的气体全部逸出后,向溶液中加入VmLamol•L‒1NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
您最近一年使用:0次
名校
解题方法
4 . 将32.64g铜粉与140 mL 一定量浓硝酸恰好完全反应,铜完全溶解,反应后收集到的气体在标准状况下的体积为11.2 L。(反应中只产生NO或NO2 )请回答:
(1)NO的物质的量为___________ mol
(2)待产生的气体全部释放后,向溶液中加入v mL a mol/L的 NaOH 溶液,恰好使溶液中的 Cu2+ 全部沉淀,则原硝酸的浓度为_____________ 。
(3)欲使铜与硝酸反应生成的气体在溶液中完全转化为NaNO3,至少需要加入30%的双氧水的质量是___ g
(1)NO的物质的量为
(2)待产生的气体全部释放后,向溶液中加入v mL a mol/L的 NaOH 溶液,恰好使溶液中的 Cu2+ 全部沉淀,则原硝酸的浓度为
(3)欲使铜与硝酸反应生成的气体在溶液中完全转化为NaNO3,至少需要加入30%的双氧水的质量是
您最近一年使用:0次
名校
解题方法
5 . 取一定量的Fe、Cu的混合物粉末,平均分成A、B、C、D、E五等份,分别向每一份中加入一定量的稀硝酸,实验中收集到的NO气体(惟一还原产物)的体积及所得剩余物的质量记录如下(所有体积均在标准状况下测定):
(1)A组实验后17.2 g剩余固体为___________ (均填写化学式)
(2)实验中每次所取混合物中铁的物质的量为________ mol。
(3)若C组金属恰好反应完,则反应后溶液中的金属阳离子为:____ ,物质的量之比是:___ 。
| 实验序号 | A | B | C | D | E |
| 硝酸溶液体积 | 100ml | 200 mL | 300 mL | 400 mL | 500 mL |
| 剩余固体的质量 | 17.2 g | 8g | 0 g | 0 g | 0 g |
| 气体体积 | 2.24 L | 4.48 L | 6.72L | 7.84 L | 7.84 L |
(1)A组实验后17.2 g剩余固体为
(2)实验中每次所取混合物中铁的物质的量为
(3)若C组金属恰好反应完,则反应后溶液中的金属阳离子为:
您最近一年使用:0次
名校
解题方法
6 . 1.52g铜镁合金溶于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中恰好完全溶解,得到NO2和N2O4的混合气体1120mL(标准状况)。向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
(1)写出铜与稀硝酸反应的离子方程式_______ ;
(2)该浓硝酸的物质的量浓度________ mol/L;
(3)该合金中铜与镁的物质的量之和是_________ ;
(4)NO2和N2O4的混合气体中含有NO2的物质的量_________ 。
(1)写出铜与稀硝酸反应的离子方程式
(2)该浓硝酸的物质的量浓度
(3)该合金中铜与镁的物质的量之和是
(4)NO2和N2O4的混合气体中含有NO2的物质的量
您最近一年使用:0次
7 . 铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,生成的气体为NO、 。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗
。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗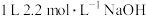 溶液和
溶液和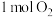 ,则生成的NO、
,则生成的NO、 的物质的量分别为
的物质的量分别为_______ 、_______ ,生成硫酸铜的物质的量为_________________ 。
 。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗
。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗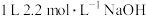 溶液和
溶液和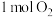 ,则生成的NO、
,则生成的NO、 的物质的量分别为
的物质的量分别为
您最近一年使用:0次
2020-09-23更新
|
452次组卷
|
2卷引用:高一必修第一册(鲁科2019)第3章 第3节 氮的循环 高考帮
8 . 为了测定某铜银合金成分,将30.0g合金溶于80mL13.5mol•L-1的浓硝酸中,待反应完全后,收集到6.72L气体(已换算成标准状况),并测得溶液中c(H+)=1mol•L-1。假设反应后溶液的体积仍为80mL,试计算(已知Ag可与HNO3反应):
(1)被还原的HNO3的物质的量为___ ;
(2)合金中银的质量分数为__ 。
(1)被还原的HNO3的物质的量为
(2)合金中银的质量分数为
您最近一年使用:0次
2020-09-23更新
|
1451次组卷
|
4卷引用:鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第3节 氮的循环 课时3 硝酸
10-11高一上·浙江绍兴·期中
9 . 取一定量的CuO粉末与0.5 L稀硫酸充分反应后,将一根50 g铁棒插入上述溶液中,至铁棒质量不再变化时,铁棒增重0.24 g, 并收集到224 mL气体(标准状况)。求此CuO粉末的质量____ 。
您最近一年使用:0次
解题方法
10 . 在浓硝酸中放入铜片:
(1)反应开始时的化学方程式为______ ,实验现象为_________ 。
(2)若铜片有剩余,则反应将要结束时的化学方程式为__________ 。
(3)待反应停止后,再加入少量的稀硫酸,这时,铜片上又有气泡产生,原因是_______ 。
(4)若将 铜与一定量的浓硝酸反应,铜消耗完后,共产生气体
铜与一定量的浓硝酸反应,铜消耗完后,共产生气体 (标准状况),则所消耗的硝酸的物质的量是
(标准状况),则所消耗的硝酸的物质的量是______ (气体中不含 )。
)。
(1)反应开始时的化学方程式为
(2)若铜片有剩余,则反应将要结束时的化学方程式为
(3)待反应停止后,再加入少量的稀硫酸,这时,铜片上又有气泡产生,原因是
(4)若将
 铜与一定量的浓硝酸反应,铜消耗完后,共产生气体
铜与一定量的浓硝酸反应,铜消耗完后,共产生气体 (标准状况),则所消耗的硝酸的物质的量是
(标准状况),则所消耗的硝酸的物质的量是 )。
)。
您最近一年使用:0次
2020-09-11更新
|
442次组卷
|
4卷引用:2015-2016学年山东省淄博市高青一中高一4月月考化学试卷
2015-2016学年山东省淄博市高青一中高一4月月考化学试卷鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第3节 氮的循环 课时3 硝酸高一必修第二册(人教2019版)第五章 第二节 氮及其化合物 课时3 硝酸(已下线)5.2.3 硝酸(练好题)(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)



