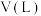名校
1 . 完成下列问题
(1)现有 、
、 和
和 组成的混合物,某研究性学习小组为了探究其组成情况,加入
组成的混合物,某研究性学习小组为了探究其组成情况,加入 溶液恰好使混合物完全溶解,同时收集到
溶液恰好使混合物完全溶解,同时收集到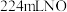 气体(标况)。则产物中硝酸铜的物质的量为
气体(标况)。则产物中硝酸铜的物质的量为___________ 。如原混合物中有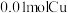 ,则其中
,则其中 与
与 的质量之比为
的质量之比为___________ 。
(2)将一定质量的铜粉加入到 某浓度的稀硝酸中,充分反应后,容器中剩有
某浓度的稀硝酸中,充分反应后,容器中剩有 铜粉,此时共收集到
铜粉,此时共收集到 气体
气体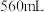 (标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止,容器仍剩有铜粉
(标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止,容器仍剩有铜粉 ,则
,则 为
为___________ 。
(3)将铁粉和铜粉的均匀混合物平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成 的体积和剩余金属的质量如下表(设硝酸的还原产物只有
的体积和剩余金属的质量如下表(设硝酸的还原产物只有 )。
)。
①稀硝酸的物质的量的浓度为___________  。
。
②V=___________ 。
(1)现有
 、
、 和
和 组成的混合物,某研究性学习小组为了探究其组成情况,加入
组成的混合物,某研究性学习小组为了探究其组成情况,加入 溶液恰好使混合物完全溶解,同时收集到
溶液恰好使混合物完全溶解,同时收集到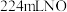 气体(标况)。则产物中硝酸铜的物质的量为
气体(标况)。则产物中硝酸铜的物质的量为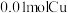 ,则其中
,则其中 与
与 的质量之比为
的质量之比为(2)将一定质量的铜粉加入到
 某浓度的稀硝酸中,充分反应后,容器中剩有
某浓度的稀硝酸中,充分反应后,容器中剩有 铜粉,此时共收集到
铜粉,此时共收集到 气体
气体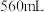 (标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止,容器仍剩有铜粉
(标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止,容器仍剩有铜粉 ,则
,则 为
为(3)将铁粉和铜粉的均匀混合物平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成
 的体积和剩余金属的质量如下表(设硝酸的还原产物只有
的体积和剩余金属的质量如下表(设硝酸的还原产物只有 )。
)。| 编号 | ① | ② | ③ | ④ |
硝酸体积 | 100 | 200 | 300 | 400 |
剩余金属 | 18.0 |  | 0 | 0 |
 体积 体积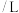 | 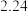 |  | 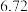 | V |
 。
。②V=
您最近半年使用:0次
名校
解题方法
2 . 为确定某一铁铜样品中各成份的含量,某同学进行了如下实验:准确称取一份质量为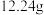 铁铜样品,逐渐加入一定体积某浓度的稀硝酸,每次实验充分反应后,测得生成
铁铜样品,逐渐加入一定体积某浓度的稀硝酸,每次实验充分反应后,测得生成 气体的体积为
气体的体积为 (已换成标准状况,假设生成的
(已换成标准状况,假设生成的 全部逸出),并测得剩余固体质量为
全部逸出),并测得剩余固体质量为 。各次实验的数据如下表:
。各次实验的数据如下表:
根据以上实验数据,请回答:
(1)上述实验当加入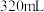 稀硝酸后,所发生反应的离子方程式为
稀硝酸后,所发生反应的离子方程式为______ 。
(2)稀硝酸的物质的量浓度为______  。
。
(3)样品中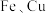 的物质的量之比为
的物质的量之比为______ 。
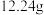 铁铜样品,逐渐加入一定体积某浓度的稀硝酸,每次实验充分反应后,测得生成
铁铜样品,逐渐加入一定体积某浓度的稀硝酸,每次实验充分反应后,测得生成 气体的体积为
气体的体积为 (已换成标准状况,假设生成的
(已换成标准状况,假设生成的 全部逸出),并测得剩余固体质量为
全部逸出),并测得剩余固体质量为 。各次实验的数据如下表:
。各次实验的数据如下表:稀硝酸体积 | 0 | 80 | 160 | 240 | 320 | 400 |
| 0 | 0.896 | 1.792 | 2.688 | 3.584 | 4.48 |
剩余固体质量 | 12.24 | 8.88 | 5.52 | 1.92 | 0 | 0 |
(1)上述实验当加入
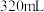 稀硝酸后,所发生反应的离子方程式为
稀硝酸后,所发生反应的离子方程式为(2)稀硝酸的物质的量浓度为
 。
。(3)样品中
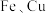 的物质的量之比为
的物质的量之比为
您最近半年使用:0次
名校
解题方法
3 . 将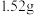 铜镁合金完全溶解于50mL8mol/L的浓硝酸中,得到NO和NO2的混合气体896mL(标准状况),向反应后的溶液中加入
铜镁合金完全溶解于50mL8mol/L的浓硝酸中,得到NO和NO2的混合气体896mL(标准状况),向反应后的溶液中加入 溶液,当金属离子全部沉淀时,得到2.54g沉淀。求:
溶液,当金属离子全部沉淀时,得到2.54g沉淀。求:
(1)50mL8mol/L的浓硝酸中含有HNO3的物质的量为_______  。
。
(2)该合金含铜_______ g。
(3)混合气体中,NO和NO2的物质的量之比为_______ 。
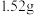 铜镁合金完全溶解于50mL8mol/L的浓硝酸中,得到NO和NO2的混合气体896mL(标准状况),向反应后的溶液中加入
铜镁合金完全溶解于50mL8mol/L的浓硝酸中,得到NO和NO2的混合气体896mL(标准状况),向反应后的溶液中加入 溶液,当金属离子全部沉淀时,得到2.54g沉淀。求:
溶液,当金属离子全部沉淀时,得到2.54g沉淀。求:(1)50mL8mol/L的浓硝酸中含有HNO3的物质的量为
 。
。(2)该合金含铜
(3)混合气体中,NO和NO2的物质的量之比为
您最近半年使用:0次
2023-09-15更新
|
883次组卷
|
2卷引用:浙江省绍兴市稽山中学2022-2023学年高一下学期期中检测化学试题
解题方法
4 . 现有一份部分被氧化的铜片(氧化产物为CuO),称取8.64 g该铜片,溶于280 mL 1.00 mol⋅L 稀硝酸中,反应恰好完全进行,收集到无色气体896 mL(已折算为标准状况)。
稀硝酸中,反应恰好完全进行,收集到无色气体896 mL(已折算为标准状况)。
(1)该稀硝酸中所含硝酸的物质的量为___________ 。
(2)8.64 g铜片中CuO的质量为___________ 。
(3)该铜片中,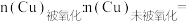
___________ 。
 稀硝酸中,反应恰好完全进行,收集到无色气体896 mL(已折算为标准状况)。
稀硝酸中,反应恰好完全进行,收集到无色气体896 mL(已折算为标准状况)。(1)该稀硝酸中所含硝酸的物质的量为
(2)8.64 g铜片中CuO的质量为
(3)该铜片中,
您最近半年使用:0次
解题方法
5 . 将9.6g铜与150mL一定浓度的硝酸反应,铜完全溶解产生的 和
和 混合气体在标准状况下的体积为4.48L。请回答:
混合气体在标准状况下的体积为4.48L。请回答:
(1)上述反应电子转移的物质的量为___________ mol;
(2)铜完全溶解后,消耗的硝酸的物质的量为___________ mol;
 和
和 混合气体在标准状况下的体积为4.48L。请回答:
混合气体在标准状况下的体积为4.48L。请回答:(1)上述反应电子转移的物质的量为
(2)铜完全溶解后,消耗的硝酸的物质的量为
您最近半年使用:0次
6 . 将64g Cu投入100mL  的浓硝酸中,当硝酸全部反应时,收集到标准状况下
的浓硝酸中,当硝酸全部反应时,收集到标准状况下 和NO的混合气体8.96L。
和NO的混合气体8.96L。
(1)被还原的硝酸的物质的量是___________ 。
(2)生成的NO气体在标准状况下的体积为___________ 。
(3)如果向反应后的溶液中再加入100mL 2mol/L的稀硫酸,发现铜片又逐渐溶解,产生无色气体,则发生反应的离子方程式为___________ ,又继续溶解的Cu的质量为___________ 。
 的浓硝酸中,当硝酸全部反应时,收集到标准状况下
的浓硝酸中,当硝酸全部反应时,收集到标准状况下 和NO的混合气体8.96L。
和NO的混合气体8.96L。(1)被还原的硝酸的物质的量是
(2)生成的NO气体在标准状况下的体积为
(3)如果向反应后的溶液中再加入100mL 2mol/L的稀硫酸,发现铜片又逐渐溶解,产生无色气体,则发生反应的离子方程式为
您最近半年使用:0次
名校
解题方法
7 . 甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答。
(1)甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4g铜。
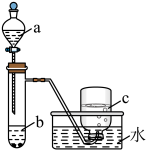
①写出铜与浓硝酸反应的化学方程式_______ 。硝酸所表现出的化学性质主要有_______
②待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是_______ g。
(2)乙组同学对铁与稀硝酸的反应进行探究。他们用0.1mol Fe和含有0.3mol 的稀硝酸进行实验,若两种物质恰好反应都无剩余,且
的稀硝酸进行实验,若两种物质恰好反应都无剩余,且 只被还原成NO。则
只被还原成NO。则
①反应结束后的溶液中 、
、 的物质的量之比
的物质的量之比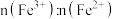 为
为_______ 。
②标准状况下,计算生成NO气体的体积_______ 。
(1)甲组同学采用如图所示装置验证铜与硝酸的反应。已知仪器a中盛有足量一定浓度的硝酸溶液,试管b中盛有6.4g铜。

①写出铜与浓硝酸反应的化学方程式
②待试管b中反应进行完全,如果向b中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是
(2)乙组同学对铁与稀硝酸的反应进行探究。他们用0.1mol Fe和含有0.3mol
 的稀硝酸进行实验,若两种物质恰好反应都无剩余,且
的稀硝酸进行实验,若两种物质恰好反应都无剩余,且 只被还原成NO。则
只被还原成NO。则①反应结束后的溶液中
 、
、 的物质的量之比
的物质的量之比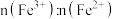 为
为②标准状况下,计算生成NO气体的体积
您最近半年使用:0次
8 . 向27.2gCu和Cu2O的固体混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成4.48LNO(标准状况)和Cu(NO3)2,在所得溶液中加入1.0mol•L-1的NaOH溶液1.0L,此时溶液中的溶质为NaNO3,铜离子已完全沉淀,沉淀质量为39.2g。(提示:Cu2O稀硝酸反应的方程式为:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O)
(1)在上述Cu2O与硝酸的反应中,硝酸表现出的性质有______ 。
(2)计算原固体混合物Cu2O中Cu与的物质的量之比_____ 。
(3)计算原硝酸溶液的物质的量浓度_____ 。
(1)在上述Cu2O与硝酸的反应中,硝酸表现出的性质有
(2)计算原固体混合物Cu2O中Cu与的物质的量之比
(3)计算原硝酸溶液的物质的量浓度
您最近半年使用:0次
2023-05-05更新
|
768次组卷
|
3卷引用:浙江省长河中学2022-2023学年高一下学期期中考试化学试题
浙江省长河中学2022-2023学年高一下学期期中考试化学试题 (已下线)【2023】【高一下】【期中考】【长河】【高中化学】【刘尼尼收集】山东新高考2022-2023学年高一上学期质量测评模拟演练化学试题
9 . 将3.84g铜粉与600mL浓硝酸反应(忽略体积变化),当铜完全溶解时,收集到NO、NO2混合气体2.24L(标准状况下),试计算:
(1)反应后溶液中铜离子浓度为_______ mol/L;
(2)反应所消耗硝酸的物质的量是_______ mol;
(3)生成的NO与NO2体积比为_______ 。
(1)反应后溶液中铜离子浓度为
(2)反应所消耗硝酸的物质的量是
(3)生成的NO与NO2体积比为
您最近半年使用:0次
2023高一下·浙江·期中
解题方法
10 . 向27.2 gCu和Cu2O的混合物中加入某浓度稀硝酸0.5 L,固体完全反应,生成NO和Cu(NO3)2,在所得溶液中加入1.0 mol/L的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。请回答:
(1)原固体温合物中Cu与Cu2O物质的量之比为___________ 。
(2)硝酸的物质的量浓度为___________ mol/L。
(1)原固体温合物中Cu与Cu2O物质的量之比为
(2)硝酸的物质的量浓度为
您最近半年使用:0次