名校
解题方法
1 . 丁二烯是生产合成橡胶的主要原料。一定条件下,2,3-二甲基-1,3-丁二烯(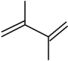 )与溴单质发生液相加成反应(1,2加成和1,4加成),已知溶剂极性越大越容易发生1,4加成。现体系中同时存在如下反应:
)与溴单质发生液相加成反应(1,2加成和1,4加成),已知溶剂极性越大越容易发生1,4加成。现体系中同时存在如下反应:
①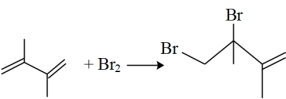
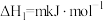
②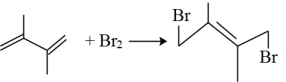
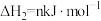
③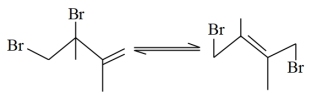

由阿伦尼乌斯公式推知,同一反应在不同温度(T)下,反应速率常数(k)与活化能(Ea)的关系如下: (其中R为常数)。已知体系中两种产物可通过
(其中R为常数)。已知体系中两种产物可通过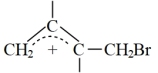 互相转化,反应历程及能量变化如下图所示:
互相转化,反应历程及能量变化如下图所示:
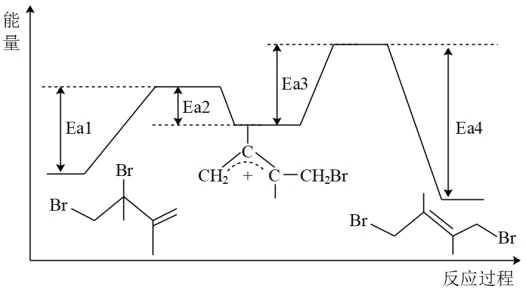
(1)由反应历程及能量变化图示判断,m_______ n(填“>”、“=”或“<”),
_______ 。(用含不同活化能 的式子表示)
的式子表示)
(2)其他条件不变的情况下,升高反应温度,对反应_______ (填①或②)的速率提高更有利,分析原因_______ 。
(3)由反应历程及能量变化图示判断,产物中_______ (用系统命名法命名)含量更大,若要提高该产物在平衡体系中的物质的量分数,还可采取的措施是_______ 。
(4)在一定温度下,向某反应容器中加入1.0mol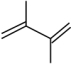 和一定量的
和一定量的 发生上述反应。测得
发生上述反应。测得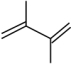 的平衡转化率为
的平衡转化率为 ,平衡时
,平衡时 为b mol,若以物质的量分数表示的平衡常数
为b mol,若以物质的量分数表示的平衡常数 ,反应③的平衡常数
,反应③的平衡常数 ,则产物
,则产物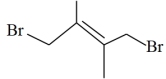 的选择性百分比为
的选择性百分比为_______ ,开始加入的 为
为_______ mol,反应①的平衡常数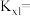
_______ 。
 )与溴单质发生液相加成反应(1,2加成和1,4加成),已知溶剂极性越大越容易发生1,4加成。现体系中同时存在如下反应:
)与溴单质发生液相加成反应(1,2加成和1,4加成),已知溶剂极性越大越容易发生1,4加成。现体系中同时存在如下反应:①

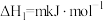
②
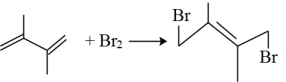
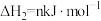
③


由阿伦尼乌斯公式推知,同一反应在不同温度(T)下,反应速率常数(k)与活化能(Ea)的关系如下:
 (其中R为常数)。已知体系中两种产物可通过
(其中R为常数)。已知体系中两种产物可通过 互相转化,反应历程及能量变化如下图所示:
互相转化,反应历程及能量变化如下图所示:
(1)由反应历程及能量变化图示判断,m

 的式子表示)
的式子表示)(2)其他条件不变的情况下,升高反应温度,对反应
(3)由反应历程及能量变化图示判断,产物中
(4)在一定温度下,向某反应容器中加入1.0mol
 和一定量的
和一定量的 发生上述反应。测得
发生上述反应。测得 的平衡转化率为
的平衡转化率为 ,平衡时
,平衡时 为b mol,若以物质的量分数表示的平衡常数
为b mol,若以物质的量分数表示的平衡常数 ,反应③的平衡常数
,反应③的平衡常数 ,则产物
,则产物 的选择性百分比为
的选择性百分比为 为
为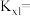
您最近一年使用:0次
2022-04-19更新
|
678次组卷
|
3卷引用:山东省青岛市2022高考一模化学试题
名校
2 . 中国科学家在以乙醇为原料的化工前沿科技中取得了一个又一个突破。
I.近年来,科学家研究了乙醇催化合成乙酸乙酯的新方法:
2C2H5OH(g) CH3COOC2H5(g)+2H2(g) △H=-4.7kJ·mol-1。
CH3COOC2H5(g)+2H2(g) △H=-4.7kJ·mol-1。
(1)300℃时,在某刚性密闭容器内充入一定量的C2H5OH(g),若平衡时容器内总压为pPa,乙醇的转化率为a,则该反应的平衡常数Kp=___________ Pa(用含p、a的代数式表示,Kp为用分压表示的平衡常数)。
(2)其他条件相同,测得不同温度下液态收集物中各种产物的质量分数如下图所示。

①从上图可以看出随着温度升高乙酸乙酯的质量分数先增大又减小,造成质量分数减小的可能原因是___________ (答出两条即可)。
②对该合成方法的理解,下列表述错误的是___________ (填序号)。
A.加压有利于提高乙酸乙酯的产率
B.可采用先对产物冷凝收集再分离的办法获得乙酸乙酯
C.在合成中,可使用热交换器,实现热量的综合利用
Ⅱ.乙醇与水蒸气催化制氢气近年来也广为推广,总的反应方程式为CH3CH2OH(g)+3H2O(g) 2CO2(g)+6H2(g) △H
2CO2(g)+6H2(g) △H
下图是Akande对其动力学机理的研究(M*代表催化剂,*是催化剂上的吸附点)。回答下列问题:

(1)该反应的活化能(最大能垒)为___________ ev(填序号,下同)。
A.bB.dC.eD.d-c
(2)该反应的焓变△H=___________ ev。
A.bB.dC.eD.d-c
(3)下列说法中,与反应历程不符的是___________ 。
A.反应过程中H2O未被吸附到催化剂上B.乙醇在催化剂上的吸附影响反应的速率
C.温度越低越有利于提高乙醇的转化率D.步骤②→③有碳碳单键的断裂
(4)步骤④→⑤发生反应的方程式为M*CH3OH+H2O→M*+CO2+3H2和___________ 。
I.近年来,科学家研究了乙醇催化合成乙酸乙酯的新方法:
2C2H5OH(g)
 CH3COOC2H5(g)+2H2(g) △H=-4.7kJ·mol-1。
CH3COOC2H5(g)+2H2(g) △H=-4.7kJ·mol-1。(1)300℃时,在某刚性密闭容器内充入一定量的C2H5OH(g),若平衡时容器内总压为pPa,乙醇的转化率为a,则该反应的平衡常数Kp=
(2)其他条件相同,测得不同温度下液态收集物中各种产物的质量分数如下图所示。

①从上图可以看出随着温度升高乙酸乙酯的质量分数先增大又减小,造成质量分数减小的可能原因是
②对该合成方法的理解,下列表述错误的是
A.加压有利于提高乙酸乙酯的产率
B.可采用先对产物冷凝收集再分离的办法获得乙酸乙酯
C.在合成中,可使用热交换器,实现热量的综合利用
Ⅱ.乙醇与水蒸气催化制氢气近年来也广为推广,总的反应方程式为CH3CH2OH(g)+3H2O(g)
 2CO2(g)+6H2(g) △H
2CO2(g)+6H2(g) △H下图是Akande对其动力学机理的研究(M*代表催化剂,*是催化剂上的吸附点)。回答下列问题:

(1)该反应的活化能(最大能垒)为
A.bB.dC.eD.d-c
(2)该反应的焓变△H=
A.bB.dC.eD.d-c
(3)下列说法中,与反应历程不符的是
A.反应过程中H2O未被吸附到催化剂上B.乙醇在催化剂上的吸附影响反应的速率
C.温度越低越有利于提高乙醇的转化率D.步骤②→③有碳碳单键的断裂
(4)步骤④→⑤发生反应的方程式为M*CH3OH+H2O→M*+CO2+3H2和
您最近一年使用:0次
解题方法
3 . 氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。
(1)下图是一定温度和压强下,N2和H2反应生成1molNH3过程中能量变化示意图,则N2(g)+3H2(g) 2NH3(g)的△H=
2NH3(g)的△H=_______ (用含字母Q1、Q2的代数式表示)。若在反应体系中加入催化剂使化学反应速率增大,则E1的变化是________ (填 “增大”“减小”或“不变”,下同),该反应的反应热 ΔH_________ 。

(2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应: N2(g)+3H2O(l) 2NH3(g)+
2NH3(g)+ O2(g) △H=a kJ·mol-1为进一步研究NH3生成量与温度的关系,测得常压下达到平衡时部分实验数据如下表:
O2(g) △H=a kJ·mol-1为进一步研究NH3生成量与温度的关系,测得常压下达到平衡时部分实验数据如下表:
此合成反应中,a__________ 0;△S__________ 0(填“>”、“<”或 “=”)
(3)某温度下,体积均为0.25L的两个恒容密闭容器中发生下列反应:N2(g)+3H2(g)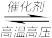 2NH3(g) △H= -92.4kJ·mol-1,实验测得反应起始时、达到平衡时的有关数据如下表所示
2NH3(g) △H= -92.4kJ·mol-1,实验测得反应起始时、达到平衡时的有关数据如下表所示
容器B中反应达到平衡状态时的反应热△H2=________ 。
(1)下图是一定温度和压强下,N2和H2反应生成1molNH3过程中能量变化示意图,则N2(g)+3H2(g)
 2NH3(g)的△H=
2NH3(g)的△H=
(2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应: N2(g)+3H2O(l)
 2NH3(g)+
2NH3(g)+ O2(g) △H=a kJ·mol-1为进一步研究NH3生成量与温度的关系,测得常压下达到平衡时部分实验数据如下表:
O2(g) △H=a kJ·mol-1为进一步研究NH3生成量与温度的关系,测得常压下达到平衡时部分实验数据如下表:| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
此合成反应中,a
(3)某温度下,体积均为0.25L的两个恒容密闭容器中发生下列反应:N2(g)+3H2(g)
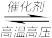 2NH3(g) △H= -92.4kJ·mol-1,实验测得反应起始时、达到平衡时的有关数据如下表所示
2NH3(g) △H= -92.4kJ·mol-1,实验测得反应起始时、达到平衡时的有关数据如下表所示| 容器 编号 | 起始时各物质的物质的量/mol | 反应达平衡时的焓变 | ||
| N2 | H2 | NH3 | ||
| A | 1 | 3 | 0 | △H1=-23.1 kJ·mol-1 |
| B | 0.9 | 2.7 | 0.2 | △H2 |
容器B中反应达到平衡状态时的反应热△H2=
您最近一年使用:0次



