13-14高三上·北京朝阳·期末
1 . 天然气(以甲烷计)在工业生产中用途广泛。
(1)Ⅰ.在制备合成氨原料气H2中的应用
(1)甲烷蒸气转化法制H2的主要转化反应如下:
CH4(g)+H2O(g)⇌CO(g)+3H2(g)ΔH=+206.2kJ/mol
CH4(g)+2H2O(g)⇌CO2(g)+4H2(g)ΔH=+165.0kJ/mol
上述反应所得原料气中的CO能使合成氨催化剂中毒,必须除去。工业上常采用催化剂存在下CO与水蒸气反应生成易除去的CO2,同时又可制得等体积的氢气的方法。此反应称为一氧化碳变换反应,该反应的热化学方程式是_______ 。
(2)CO变换反应的汽气比(水蒸气与原料气中CO物质的量之比)与CO平衡变换率(已转化的一氧化碳量与变换前一氧化碳量之比)的关系如图所示:
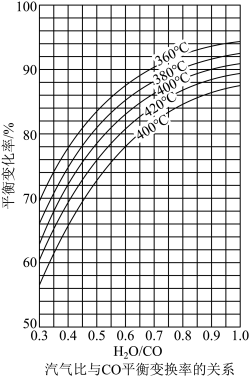
析图可知:
①相同温度时,CO平衡变换率与汽气比的关系是_______ 。
②汽气比相同时,CO平衡变换率与温度的关系是_______ 。
(3)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度也可以表示平衡常数(记作Kp),则CO变换反应的平衡常数表示式为Kp=_______ 。随温度的降低,该平衡常数_______ (填“增大”“减小”或“不变”)。
(4)Ⅱ.在熔融碳酸盐燃料电池中的应用以熔融Li2CO3和K2CO3为电解质,天然气经内重整催化作用提供反应气的燃料电池示意图如图:

①外电路电子流动方向:由_______ 流向_______ (填字母)。
②空气极发生反应的离子方程式是_______ 。
③以此燃料电池为电源电解精炼铜,当电路有0.6 mol e-转移,有_______ g 精铜析出。
(1)Ⅰ.在制备合成氨原料气H2中的应用
(1)甲烷蒸气转化法制H2的主要转化反应如下:
CH4(g)+H2O(g)⇌CO(g)+3H2(g)ΔH=+206.2kJ/mol
CH4(g)+2H2O(g)⇌CO2(g)+4H2(g)ΔH=+165.0kJ/mol
上述反应所得原料气中的CO能使合成氨催化剂中毒,必须除去。工业上常采用催化剂存在下CO与水蒸气反应生成易除去的CO2,同时又可制得等体积的氢气的方法。此反应称为一氧化碳变换反应,该反应的热化学方程式是
(2)CO变换反应的汽气比(水蒸气与原料气中CO物质的量之比)与CO平衡变换率(已转化的一氧化碳量与变换前一氧化碳量之比)的关系如图所示:

析图可知:
①相同温度时,CO平衡变换率与汽气比的关系是
②汽气比相同时,CO平衡变换率与温度的关系是
(3)对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度也可以表示平衡常数(记作Kp),则CO变换反应的平衡常数表示式为Kp=
(4)Ⅱ.在熔融碳酸盐燃料电池中的应用以熔融Li2CO3和K2CO3为电解质,天然气经内重整催化作用提供反应气的燃料电池示意图如图:

①外电路电子流动方向:由
②空气极发生反应的离子方程式是
③以此燃料电池为电源电解精炼铜,当电路有0.6 mol e-转移,有
您最近一年使用:0次



