名校
1 . CO2甲烷化加快了能源结构由化石燃料向可再生碳资源的转变。
(1) CO2甲烷化反应最早由化学家Paul Sabatier提出。在一定的温度和压力条件下,将按一定比例混合的CO2和H2通过装有催化剂的反应器可得到甲烷。已知
CH4(g)+H2O(g)=3H2(g)+CO(g) ΔH=206 kJ·mol-1;
CO(g)+H2O(g)=H2(g)+CO2(g) ΔH=-41kJ·mol-1。
则反应CO2(g)+4H2(g)=CH4(g)+2H2O(g)的ΔH=______ kJ·mol-1,ΔS______ 0(填“>”、“<”或“=”)。
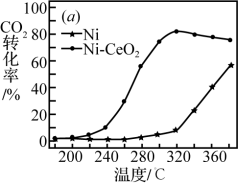
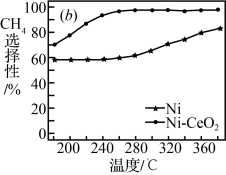
(2) 催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如下图所示。
①过渡元素是寻找催化剂的主要方向。催化剂Ni原子的基态核外电子排布式为______ 。
②高于320℃后,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是______ 。
③对比上述两种催化剂的催化性能,工业上应选择的催化剂是______ ,使用的合适温度为______ 。
(3) 近年来新兴的生物电催化技术运用微生物电解池也可实现CO2甲烷化,其工作原理如图所示。

①微生物电解池实现CO2甲烷化的阴极电极反应式为______ 。
②如果处理有机物[(CH2O)n]产生标准状况下56 m3的甲烷,则理论上导线中通过的电子的物质的量为______ 。
(1) CO2甲烷化反应最早由化学家Paul Sabatier提出。在一定的温度和压力条件下,将按一定比例混合的CO2和H2通过装有催化剂的反应器可得到甲烷。已知
CH4(g)+H2O(g)=3H2(g)+CO(g) ΔH=206 kJ·mol-1;
CO(g)+H2O(g)=H2(g)+CO2(g) ΔH=-41kJ·mol-1。
则反应CO2(g)+4H2(g)=CH4(g)+2H2O(g)的ΔH=
(2) 催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如下图所示。


①过渡元素是寻找催化剂的主要方向。催化剂Ni原子的基态核外电子排布式为
②高于320℃后,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是
③对比上述两种催化剂的催化性能,工业上应选择的催化剂是
(3) 近年来新兴的生物电催化技术运用微生物电解池也可实现CO2甲烷化,其工作原理如图所示。

①微生物电解池实现CO2甲烷化的阴极电极反应式为
②如果处理有机物[(CH2O)n]产生标准状况下56 m3的甲烷,则理论上导线中通过的电子的物质的量为
您最近一年使用:0次
2021-03-06更新
|
369次组卷
|
3卷引用:河北省张家口市宣化第一中学2021届高三下学期阶段模拟(五)化学试题
解题方法
2 . (1)根据下列热化学方程式:
①C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
②H2(g)+ O2(g)═H2O(l)△H=-285.8kJ•mol-1
O2(g)═H2O(l)△H=-285.8kJ•mol-1
③CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H=-870.3kJ•mol-1
可以计算出2C(s)+2H2(g)+O2(g)═CH3COOH(l)的反应热为___ 。
(2)已知在101kPa时,CO的燃烧热为283kJ•mol-1。相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1molCO完全燃烧放出热量的6.30倍,表示CH4燃烧热的热化学方程式是___ 。
(3)催化剂可以加快化学反应速率的原因___ 。
(4)把一小块镁、铝合金放入6mol•L-1的NaOH溶液中,可以形成微型原电池,则该原电池负极发生的电极反应式为___ 。
①C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
②H2(g)+
 O2(g)═H2O(l)△H=-285.8kJ•mol-1
O2(g)═H2O(l)△H=-285.8kJ•mol-1③CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H=-870.3kJ•mol-1
可以计算出2C(s)+2H2(g)+O2(g)═CH3COOH(l)的反应热为
(2)已知在101kPa时,CO的燃烧热为283kJ•mol-1。相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1molCO完全燃烧放出热量的6.30倍,表示CH4燃烧热的热化学方程式是
(3)催化剂可以加快化学反应速率的原因
(4)把一小块镁、铝合金放入6mol•L-1的NaOH溶液中,可以形成微型原电池,则该原电池负极发生的电极反应式为
您最近一年使用:0次
名校
解题方法
3 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4+5H2C2O4+3H2SO4==2MnSO4+10CO2↑+8H2O+K2SO4
【实验内容及记录】
请回答:
(1)请完成上述实验设计表:V1=_________ ,V2=__________ 。
(2)根据上表中的实验数据,可以得到的结论是_________________________________ 。
(3)利用实验1中数据计算,反应速率为v(KMnO4)=_________________________ 。
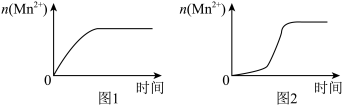
(4)该小组同学依据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。____________________________________________________ 。
②请你帮助该小组同学完成实验方案,并填写表中空白。
③若该小组同学提出的假设成立,应观察到的现象是_______________________________ 。
【实验原理】2KMnO4+5H2C2O4+3H2SO4==2MnSO4+10CO2↑+8H2O+K2SO4
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液褪色至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.1 mol/L KMnO4溶液 | 3 mol/L H2SO4溶液 | ||
| 1 | 3.0 | 13.0 | 2.0 | 2.0 | 8.0 |
| 2 | 2.0 | 14.0 | 2.0 | 2.0 | 10.4 |
| 3 | 1.0 | V1 | V2 | 2.0 | 12.8 |
(1)请完成上述实验设计表:V1=
(2)根据上表中的实验数据,可以得到的结论是
(3)利用实验1中数据计算,反应速率为v(KMnO4)=
(4)该小组同学依据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
②请你帮助该小组同学完成实验方案,并填写表中空白。
| 实验编号 | 室温下,试管中所加试剂及其用量 | 室温下溶液褪色至无色所需时间/min | ||||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.1 mol/L KMnO4溶液 | 3 mol/L H2SO4溶液 | 少量 | ||
| 4 | 3.0mL | 13.0mL | 2.0mL | 2.0mL | t | |
③若该小组同学提出的假设成立,应观察到的现象是
您最近一年使用:0次
2020-09-05更新
|
517次组卷
|
6卷引用:河北正定中学2019-2020学年高一下学期摸底考试化学试题



