17. 实验室用氨法浸出氧化锌烟尘制备活性ZnO,其主要实验流程如下:
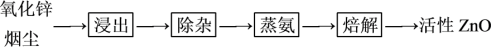
(1)浸出。用一定浓度的氨水和NH
4HCO
3配成的混合液浸取氧化锌烟尘,得到锌氨[Zn(NH
3)
4CO
3]浸出液。
①烟尘中的主要成分ZnO发生反应的化学方程式为
______。
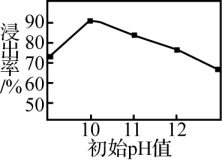
②锌元素的浸出率随浸出液初始pH的变化关系如图所示。当浸出液初始pH大于10时,浸出率随pH增大而减小的原因是
______。
(2) 除杂。Cu
2+、Pb
2+等杂质也与氨水形成配合物存在于浸出后的滤液中,加入Zn粉可将它们置换除去。写出Zn粉和铜氨配合物反应的离子方程式
______。
(3) 蒸氨。加热时溶液中过量的氨和铵被蒸出,锌氨配合物最终以2ZnCO
3·3Zn(OH)
2沉淀形式从溶液中析出。该过程需保持恒温80℃,可采取的加热方式为
______。
(4) 焙解。已知Zn(OH)
2和ZnCO
3的分解温度分别为125℃、300℃。实验室加热碱式碳酸锌[2ZnCO
3·3Zn(OH)
2]时测得的固体残留率随温度的变化关系如图所示。
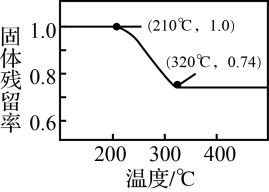
①275℃时,碱式碳酸锌分解产生的气态物质为
______(填化学式)。
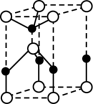
②经焙解得到的活性ZnO晶胞结构如图所示。该晶胞中Zn原子的配位数为
______。
(5) 已知pH>11时,Zn(OH)
2能溶于NaOH溶液生成[Zn(OH)
4]
2-。下表是几种离子生成氢氧化物沉淀的pH:
| 开始沉淀的pH | 沉淀完全的pH |
| Zn2+ | 5.9 | 8.9 |
| Fe2+ | 5.8 | 8.8 |
| Fe3+ | 1.1 | 3.2 |
设计以锌灰(主要成分为Zn和ZnO,杂质为Fe及其氧化物)为原料制备活性ZnO的实验方案:
______。(实验中可供选择的试剂:1.0 mol/L HNO
3、1.0 mol/L H
2SO
4、1.0 mol/L NaOH、20%H
2O
2)