解题方法
1 . 下列各项分别与哪个影响化学反应速率因素的关系最为密切?
(1)夏天的食品易变霉,在冬天不易发生该现象_______ 。
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢_______ 。
(3)MnO2加入双氧水中放出气泡更快_______ 。
(1)夏天的食品易变霉,在冬天不易发生该现象
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢
(3)MnO2加入双氧水中放出气泡更快
您最近一年使用:0次
2 . 在通常情况下,面粉并不会发生爆炸。但是,当面粉在相对密闭的空间内悬浮在空气中,达到一定浓度时,遇火却会发生剧烈的反应,导致爆炸。试用本节所学的知识对此作出解释____________ 。
您最近一年使用:0次
3 . (1)为防止碳素钢菜刀生锈,使用后特别是切过咸菜后,应采取的简易措施是___________
(2)铁与硫可以在一定条件下发生化合反应:Fe+S=FeS。该反应属于放热反应,不需要催化剂。现有块状的铁和硫磺,欲进行反应实验,,反应前宜采取的措施是___________ ,目的是___________ 。
(2)铁与硫可以在一定条件下发生化合反应:Fe+S=FeS。该反应属于放热反应,不需要催化剂。现有块状的铁和硫磺,欲进行反应实验,,反应前宜采取的措施是
您最近一年使用:0次
4 . 对于Fe+2HCl=FeCl2+H2↑,改变下列条件对生成氢气的速率有何影响?(填“增大”“减小”或“不变”)
①降低温度:________ ; ②增大盐酸浓度:________ ;
③加入NaCl固体:________ 。 ④滴入几滴CuSO4溶液:________ 。
①降低温度:
③加入NaCl固体:
您最近一年使用:0次
2020-05-09更新
|
421次组卷
|
2卷引用:安徽省合肥市2019-2020学年高二下学期开学考试化学试题
2020高三·全国·专题练习
解题方法
5 . 某混合物浆液含有Al(OH)3、MnO2和少量Na2CrO4,。考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置,使浆液分离成固体混合物和含铬元素溶液,并回收利用。回答Ⅰ和Ⅱ中的问题。
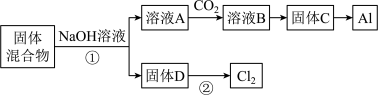
固体混合物分离利用的流程图
该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化,加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有(填序号)___ 。
a.温度 b.Cl-的浓度 c.溶液的酸度

固体混合物分离利用的流程图
该小组探究反应②发生的条件。D与浓盐酸混合,不加热,无变化,加热有Cl2生成,当反应停止后,固体有剩余,此时滴加硫酸,又产生Cl2。由此判断影响该反应有效进行的因素有(填序号)
a.温度 b.Cl-的浓度 c.溶液的酸度
您最近一年使用:0次
9-10高一下·北京朝阳·期末
解题方法
6 . 将影响反应速率条件的编号填在空格处。
A.温度 B.催化剂 C.固体的表面积 D.溶液的浓度
实 例 | 影 响 条 件 |
| 1.食物放在冰箱里能延长保质期 | |
| 2.实验室将块状药品研细,再进行反应 | |
| 3.用H2O2分解制O2时,加入MnO2 | |
| 4.实验室制取H2时,用较浓的硫酸与Zn粒反应 |
A.温度 B.催化剂 C.固体的表面积 D.溶液的浓度
您最近一年使用:0次
13-14高二·全国·课时练习
解题方法
7 . 氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率v(纵坐标)与反应时间t(横坐标)的关系如图所示,已知该反应速率随着溶液中c(H+)的增大而加快。

(1)反应开始时反应速率加快的原因是______ ;
(2)反应后期反应速率减慢的原因是______ 。

(1)反应开始时反应速率加快的原因是
(2)反应后期反应速率减慢的原因是
您最近一年使用:0次
9-10高一下·湖南长沙·阶段练习
8 . 在一块大理石(主要成分是CaCO3)上,先后滴加①1mol/LHCl溶液和②0.1mol/LHCl溶液反应快的是滴加了_______ 的(填序号,下同),先后滴加同浓度的③热盐酸和④冷盐酸,反应快的是滴加_______ 的,用⑤大理石块和⑥大理石粉分别跟同浓度的盐酸起反应,反应快的是用了_______ 的。
您最近一年使用:0次



