真题
解题方法
1 . 磷酸二氢钾在工农业生产及国防工业等领域都有广泛的应用。某研究小组用质量分数为85%的磷酸与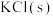 反应制备
反应制备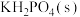 ,反应方程式为
,反应方程式为 一定条件下的实验结果如图1所示。
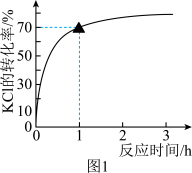
一定条件下的实验结果如图1所示。
回答问题:
(1)该条件下,反应至1h时KCl的转化率为_______ 。
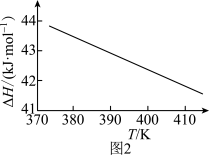
(2)该制备反应的 随温度变化关系如图2所示。该条件下反应为
随温度变化关系如图2所示。该条件下反应为_______ 反应(填“吸热”或“放热”),且反应热随温度升高而_______ 。
(3)该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化率的原因是:不使用稀磷酸_______ ;通入水蒸气_______ 。
(4)298K时,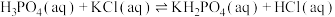 的平衡常数
的平衡常数
_______ 。(已知 的
的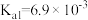 )
)
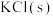 反应制备
反应制备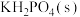 ,反应方程式为
,反应方程式为 一定条件下的实验结果如图1所示。
一定条件下的实验结果如图1所示。
回答问题:
(1)该条件下,反应至1h时KCl的转化率为
(2)该制备反应的
 随温度变化关系如图2所示。该条件下反应为
随温度变化关系如图2所示。该条件下反应为
(3)该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化率的原因是:不使用稀磷酸
(4)298K时,
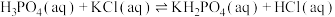 的平衡常数
的平衡常数
 的
的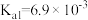 )
)
您最近一年使用:0次
2 . H2O2是一种重要的化学品,其合成方法不断发展。
(1)早期制备方法:Ba(NO3)2 BaO
BaO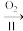 BaO2
BaO2
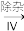 滤液
滤液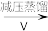 H2O2
H2O2
①I为分解反应,产物除BaO、O2外,还有一种红棕色气体。该反应的化学方程式是____ 。
②II为可逆反应,促进该反应正向进行的措施是____ 。
③III中生成H2O2,反应的化学方程式是____ 。
④减压能够降低蒸馏温度,从H2O2的化学性质角度说明V中采用减压蒸馏的原因:____ 。
(2)电化学制备方法:已知反应2H2O2=2H2O+O2↑能自发进行,反向不能自发进行,通过电解可以实现由H2O和O2为原料制备H2O2,如图为制备装置示意图。

①a极的电极反应式是____ 。
②下列说法正确的是____ 。
A.该装置可以实现电能转化为化学能
B.电极b连接电源负极
C.该方法相较于早期制备方法具有原料廉价,对环境友好等优点
(1)早期制备方法:Ba(NO3)2
 BaO
BaO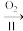 BaO2
BaO2
 滤液
滤液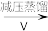 H2O2
H2O2①I为分解反应,产物除BaO、O2外,还有一种红棕色气体。该反应的化学方程式是
②II为可逆反应,促进该反应正向进行的措施是
③III中生成H2O2,反应的化学方程式是
④减压能够降低蒸馏温度,从H2O2的化学性质角度说明V中采用减压蒸馏的原因:
(2)电化学制备方法:已知反应2H2O2=2H2O+O2↑能自发进行,反向不能自发进行,通过电解可以实现由H2O和O2为原料制备H2O2,如图为制备装置示意图。

①a极的电极反应式是
②下列说法正确的是
A.该装置可以实现电能转化为化学能
B.电极b连接电源负极
C.该方法相较于早期制备方法具有原料廉价,对环境友好等优点
您最近一年使用:0次
2020-08-19更新
|
5446次组卷
|
9卷引用:2020年北京市高考化学试卷



